Caratteristiche degli enzimi caratteristici, meccanismi d'azione, esempi
- 3099
- 944
- Dott. Rodolfo Gatti
UN Enzima alosterico (Dal greco: allo, diversi + stereo, spazio tridimensionale) è una proteina in cui sono prodotte interazioni indirette tra siti topograficamente diversi, dall'unione di substrati e molecole regolatori (ligandi).
L'Unione di un ligando in un sito specifico è influenzata dall'unione di un altro ligando effettore (o ligando modulante) in un altro diverso sito (alosterico) dell'enzima. Questo è noto come interazioni alestheriche o interazioni cooperative.
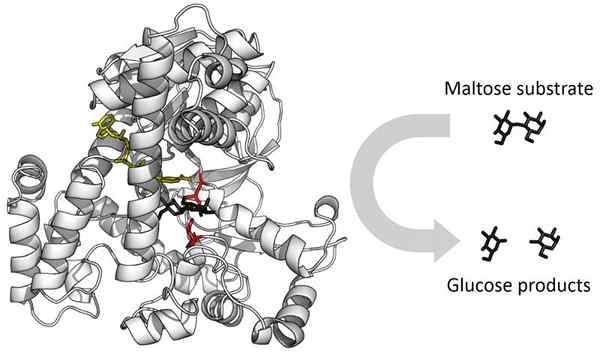
 Esempio di un enzima. Fonte: Thomas Shafee [CC BY-SA 4.0 (https: // creativeCommons.Org/licenze/by-sa/4.0)]
Esempio di un enzima. Fonte: Thomas Shafee [CC BY-SA 4.0 (https: // creativeCommons.Org/licenze/by-sa/4.0)] Quando il ligando effettore aumenta l'affinità dell'unione di un altro ligando all'enzima, la cooperativa è positiva. Quando l'affinità diminuisce la cooperativa è negativa. Se due ligandi uguali partecipano all'interazione cooperativa, l'effetto è omotropico e se i due ligandi sono diversi, l'effetto è eterotropico.
L'interazione cooperativa produce cambiamenti reversibili nella struttura molecolare dell'enzima, a livello della struttura terziaria e quaternaria. Questi cambiamenti sono noti come cambiamenti conformazionali.
[TOC]
Storia
Il concetto di interazione alestrica è emerso più di 50 anni fa. Si è evoluto nel tempo, vale a dire:
-Nel 1903 fu osservata la curva sigmoidale dell'emoglobina di ossigeno.
-Nel 1910, la curva sigmoidale dell'Unione di O2 L'emoglobina è stata matematicamente descritta dall'equazione di Hill.
-Nel 1954, Novick e Szilard mostrarono che un enzima situato all'inizio di una via metabolica era inibito dal prodotto finale di questa rotta, che è noto come feedback negativo.
-Nel 1956, Umbarger scoprì che il crepacuore della L-treonina, il primo enzima della biosintesi della L-isoleucina, era inibito dalla L-isoleucina e che non mostrava una cinetica tipica di Michaelis con una curva iperbolica, ma quella aveva fatto una curva sigmoidale.
-Nel 1963, Perutz et al., Hanno scoperto da x -raggi cambiamenti conformazionali alla struttura dell'emoglobina quando si legano all'ossigeno. Monod e Jacob hanno ribattezzato i siti regolamentari come "siti areetrici".
-Nel 1965, Monod, Wyman e Changeux propongono il modello simmetrico o il modello MWC (lettere iniziali di Monod, Wyman e Changeux) per spiegare le interazioni areestriche.
-Nel 1966, Koshland, Nemethy e Filmer propongono il modello di accoppiamento sequenziale o indotto, o modello KNF, per spiegare le interazioni areesteriche.
-Nel 1988, la struttura a raggi X dell'aspartato di transcarbamilasa ha dimostrato il modello simmetrico postulato da Monod, Wyman e Changexux.
-Negli anni '90, le mutazioni, le modifiche covalenti e le variazioni del pH sono state considerate effettori alosterici.
-Nel 1996, la struttura a raggi X Lac Transizioni dimostrate al teosterico.
Meccanismi d'azione ed esempi
-Caratteristiche dei modelli MWC e KNF della regolamentazione alosterica
Modello MWC
L'ipotesi del modello MWC originale ha proposto quanto segue (Monod, Wyman, Changex, 1965)
Può servirti: flora e fauna di entre ríos: specie rappresentativeLe proteine alosteriche sono oligomeri costituiti da protomeri simmetricamente correlati. I protomeri sono costituiti da subunità o catene polipeptidiche.
Gli oligomeri hanno almeno due stati di conformazione (R e T). Entrambi gli stati (della struttura quaternaria) stabiliscono spontaneamente un equilibrio, con o senza collegare insieme.
Quando si verifica la transizione da uno stato all'altro.
In questo modo, l'Unione cooperativa dei ligandi continua dall'interazione cooperativa tra le subunità.
Modello KNF
L'ipotesi del modello KNF ha proposto quanto segue (Koshland, Nemethy, film, 1966): The Binding Union produce un cambiamento nella struttura terziaria in una subunità. Questo cambiamento di conformazione colpisce le subunità vicine.
L'affinità di legame del ligando proteico dipende dal numero di ligandi che tengono insieme. Pertanto, le proteine teosteriche hanno più stati conformazionali che includono stati intermedi.
Negli ultimi cinque decenni, i modelli MWC e KNF sono stati valutati da studi biochimici e strutturali. È stato dimostrato che numerose proteine areestriche, compresi gli enzimi, sono conformi a ciò che viene proposto nel modello MWC, sebbene vi siano eccezioni.
Il modello MWC e gli enzimi astherici (o enzimi regolatori)
Gli enzimi alosterici sono spesso più grandi e più complessi rispetto agli enzimi non alestrici. La transcarbamilasi aspartato (aspcarbamilasa o atcasa) e fosfofructionA-1 (PFK-1) sono esempi classici di enzimi areetrici che soddisfano il modello MWC.
Atcasa di E. coli
L'ATCASA catalizza la prima reazione della biosintesi nucleotidica della pirimidina (CTP e UTP) e usa ASP come substrato. La struttura dell'Atcasa è costituita da subunità catalitiche e regolatori. Atcasa ha due stati conformazionali R e T. La simmetria tra questi due stati è conservata.
La cinetica di Atcasa (la velocità iniziale degli ATCA. Ciò indica che Atcasa ha un comportamento cooperativo.
ATCASA è inibito dal feedback CTP. La curva sigmoidea di Atcasa, in presenza di CTP, è a destra della curva sigmoidea di ATCA. Un aumento del valore della costante di Michaelis-Mindly (KM).
Cioè, in presenza di CTP, ATCAVMax), Rispetto ad Atcasa in assenza di CTP.
Può servirti: granulopoyesis: caratteristiche, ematologia, fasi e fattoriIn conclusione, il CTP è un effettore negativo eterotropico perché l'affinità di ATCASA da aspartato diminuisce. Questo comportamento è noto come cooperatività negativa.
PFK-1
Il PFK-1 catalizza la terza reazione del percorso della glicolisi. Questa reazione consiste nel trasferimento di un gruppo fosfato dall'ATP al fruttosio a 6-fosfato. La struttura del PFK-1 è un tetrametro, che presenta due stati conformazionali R e T. La simmetria tra questi due stati è conservata.
La cinetica del PFK-1 (la velocità iniziale con diverse concentrazioni di fruttosio a 6-fosfato) mostra una curva sigmoidea. Il PFK-1stá è soggetto a una complessa regolazione alostrica di ATP, AMP e Frutosa-2,6-bifosfato, vale a dire:
La curva sigmoidea del PFK-1, in presenza di un'alta concentrazione di ATP, è a destra della curva sigmoidea a bassa concentrazione di ATP (Figura 4). Un aumento del valore della costante di Michaelis-Mindly (KM).
In presenza di un'alta concentrazione di ATP, PFK-1 richiede una maggiore concentrazione di fruttosio a 6-fosfato per raggiungere la metà della velocità massima (VMax).
In conclusione, l'ATP, oltre ad essere un substrato, è un alostro eterotropico negativo.
La curva sigmoidea del PFK-1, in presenza di AMP, si trova a sinistra della curva sigmoidea del PFK-1 in presenza di ATP. Cioè, l'amplificatore elimina l'effetto dell'inibitore ATP.
In presenza di AMP, PFK-1 richiede una concentrazione di fruttosio a 6-fosfato inferiore per raggiungere la metà della velocità massima (VMax). Ciò si manifesta nel fatto che vi è una diminuzione del valore della costante di Michaelis -mente (KM).
In conclusione, l'AMP è un alostroarista eterotropico positivo perché l'affinità dell'Unione PFK-1 aumenta con il fruttosio a 6-fosfato. Frutosa-2,6-bifosfato (F2.6bp) è un potente attivatore alostrico del PFK-1 (Figura 5) e il suo comportamento è simile a quello dell'AMP.
Il modello MWC è comune, ma non universale
Delle strutture proteiche totali depositate in PDB (Banca dei dati delle proteine), la metà sono oligomer e l'altra metà sono monomeri. È stato dimostrato che la cooperatività non ha bisogno di ligandi multipli o di più subunità. Questo è il caso della glicoquinasi e di altri enzimi.
La glucochinasi è monomerica, ha una catena polipeptidica e presenta una cinetica sigmoidale in risposta all'aumento della concentrazione di glucosio nel sangue (Porter e Miller, 2012; Kamata et al., 2004).
Può servirti: parassitismo: concetto, tipi ed esempiEsistono diversi modelli che spiegano la cinetica cooperativa negli enzimi monomerici, vale a dire: modello mnemonico, modello di transizione indotto a lento lento, aggiunta randomizzata di substrati nelle reazioni biomolecolari, tipi di cambiamenti conformazionali lenti, tra gli altri.
Gli studi sulla struttura della glicoquinasi hanno supportato il modello mnemonico
La normale glicocinasi umana ha a KM 8 mm per il glucosio. Questo valore è vicino alla concentrazione di glucosio nel sangue.
Ci sono pazienti che soffrono di iperinsulinemia pessista dell'infanzia (acronimo in inglese, PHHI). La glicokinasi di questi pazienti ha a KM Per il glucosio con un valore inferiore rispetto alle normali glicocine e la cooperativa è importante.
Di conseguenza, questi pazienti hanno una variante di glicokinasi che è iperattiva, che nei casi gravi può essere letale.
Applicazioni di alosterismo
Alostería e la catalisi sono intimamente collegati. Per questo motivo, gli effetti areestrici possono influenzare le caratteristiche della catalisi come il legame del ligando, rilascio di ligando.
I siti dell'Unione alosterica possono essere bersagli di nuovi farmaci. Ciò è dovuto al fatto che l'effettore alcinale può influenzare la funzione dell'enzima. L'identificazione dei siti alosterici è il primo passo per la scoperta di farmaci che migliorano la funzione degli enzimi.
Riferimenti
- Changeux, J.P. 2012. Allostery e il modello Monod-Wyman-Changeux dopo 50 anni. Revisione annuale della biofisica e della struttura biomolecolare, 41: 103-133.
- Changeux, J.P. 2013. 50 anni di interazioni allosteriche: i colpi di scena dei modelli. Biologia cellulare molecolare, in Nature Recensioni, 14: 1-11.
- Goodey, n.M. e Benkovic, s.J. 2008. La regolazione e la catalisi allosterica emergono attraverso un percorso comune. Nature Chemical Biology, 4: 274-482.
- Kamata, k., Mitsuya, m., Nishimura, t., Eiki, Jun-Hichi, Nagata e. 2004. Base strutturali per la regolazione allosterica dell'enzima allosterico monomerico glucocinasi umana. Struttura, 12: 429-438.
- Koshland, d.E. Jr., Nemethy, g., Film, d. 1966. Confronto di dati di legame sperimentale e modelli teorici nei contoun di proteine. Biochimica, 5: 365-385.
- Monod, j., Wyman, J., Changeux, J.P. 1965. Sulla natura delle transizioni allosteriche: al modello plausibile. Journal of Molecular Biology, 12: 88-118.
- Nelson, d.L. e cox, m.M., 2008. Leynninger-Principles of Biochemistry. W.H. Freeman and Company, New York.
- Porter, c.M. e Miller, B.G. 2012. Cooperatività negli enzimi monomerici con singoli siti di legame ligando. Chimica bioorganica, 43: 44-50.
- Voet, d. e Voet, J. 2004. Biochimica. John Wiley and Sons, USA.
- « Funzione di bijective Cos'è, come è fatto, esempi, esercizi
- Teorie, processi ed esempi di evoluzione biologica »

