Divisibilità chimica
- 3708
- 88
- Zelida Gatti
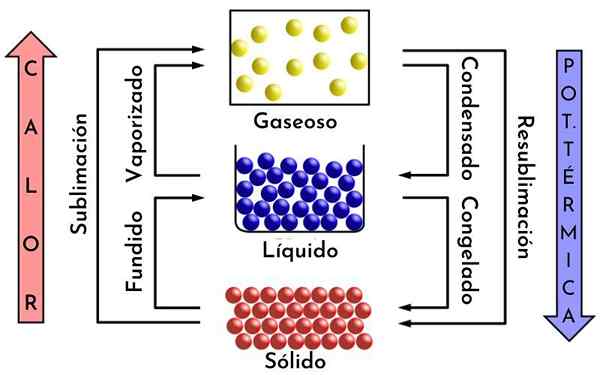
 Trasformazione della materia, un esempio di divisibilità in chimica. Fonte: Mikerun, CC BY-SA 4.0, Wikimedia Commons
Trasformazione della materia, un esempio di divisibilità in chimica. Fonte: Mikerun, CC BY-SA 4.0, Wikimedia Commons Cos'è la divisibilità chimica?
Possiamo definire il Divisibilità chimica come proprietà della materia che ti consente di separarsi in porzioni più piccole. Per capire il concetto che possiamo dare un esempio.
Se un cubetto di ghiaccio viene sciolto, diventa acqua e quando viene sottoposto a calore, viene trasformato in vapore. Questo vapore può essere diviso, a sua volta, in molecole e questi, in atomi.
La divisibilità chimica è, quindi, la possibilità di dividere in parti sempre più piccole.
Origine e concetto di divisibilità chimica
Per molto tempo è stato discusso se la questione fosse composta da particelle (ciò che sappiamo oggi come atomi), tuttavia, l'idea generale era che la questione era un continuum che poteva essere diviso.
Questo concetto generalizzato ha reso vittima di beffa a brillanti scienziati come James Clerk Maxwell (delle equazioni di Maxwell) e Ludwig Boltzman (dalla distribuzione di Boltzman) qualcosa che ha trascinato il primo a Madness e il secondo a Suicide.
Nel 5 ° secolo.C., Il filosofo greco Leucipo e il suo discepolo democrito hanno usato la parola atom.
Questa prima teoria atomica differiva dalle versioni successive, poiché includeva l'idea di un'anima umana composta da un tipo più raffinato di atomo distribuito attraverso il corpo.
La teoria atomica cadde in declino nel Medioevo, ma rianimò all'inizio della rivoluzione scientifica nel diciassettesimo secolo.
Isaac Newton, ad esempio, credeva che la materia consistesse in "particelle solide, massicce, dure, impenetrabili e mobili".
Può servirti: formula molecolare: come tirarlo fuori, esempi ed eserciziLa divisibilità può essere data con metodi diversi: la più comune è la divisibilità con metodi fisici, come tagliare una mela con un coltello.
Tuttavia, la divisibilità può anche essere data con metodi chimici, dove la materia sarebbe separata in molecole o atomi.
Esempi di divisibilità chimica
1. Sciogliere il sale
Quando un sale viene sciolto, ad esempio cloruro di sodio, in acqua, si verifica un fenomeno di solvatazione in cui vengono rotti i legami ionici del sale:
NaCl → Na+ + Cl-
Dissolvendo solo un granello di sale in acqua, sarà separato in miliardi di ioni di sodio e cloruro in soluzione.
2. Ossidazione dei metalli in mezzo acido
Tutti i metalli, ad esempio il magnesio o lo zinco, reagiscono con acidi, come acido cloridrico diluito, per dare bolle di idrogeno e una soluzione incolore di cloruro metallico.
Mg + hcl → mg2+ +Cl- + H2
Oxida in acido metallico separando i legami metallici per ottenere ioni in soluzione.
3. Idrolisi degli esteri
L'idrolisi è la rottura di un legame chimico per mezzo di acqua. Un esempio di idrolisi è l'idrolisi degli esteri, in cui sono divisi in due molecole, un alcool e un acido carbossilico.
4. Reazioni di eliminazione
Una reazione di eliminazione fa esattamente quello che dice: elimina gli atomi di una molecola. Questo viene fatto per creare un doppio legame di carbonio carbonio. Questo può essere fatto usando una base o un acido.
Può verificarsi in un unico passaggio concertato (l'astrazione del protone in Cα che si verifica contemporaneamente alla divisione del collegamento Cβ-X) o in due fasi (la divisione del collegamento Cβ-X si verifica prima per forma Un carbocalizzazione intermedia, che quindi "si spegne" dall'astrazione del protone nell'alfa-carbonio).
Può servirti: darmstadtio: scoperta, struttura, proprietà, usi5. Reazione enzimatica aldolasi
Nella fase preparativa della glicolisi, una molecola di glucosio è divisa in due molecole di gliceraldeide 3-fosfato (G3P) usando 2 ATP.
L'enzima responsabile di quell'incisione è l'aldolasi, che attraverso una condensazione inversa, divide la molecola di fruttosio 1.6-bifosfato in una molecola G3P e una molecola di diidrossicetone fosfato, che viene successivamente isomerizzata per formare un'altra molecola di G3P.
6. Degrado delle biomolecole
Non solo la glicolisi, ma tutta la degradazione delle biomolecole nelle reazioni del catabolismo, sono esempi di divisibilità chimica.
Ciò è dovuto al fatto che grandi molecole come carboidrati, acidi grassi e proteine per produrre molecole più piccole, come l'acetil COA, che entrano nel ciclo di Krebs per produrre energia sotto forma di ATP.
7. Reazioni di combustione
Questo è un altro esempio di divisibilità chimica, poiché molecole complesse, come il propano o il butano, reagiscono con l'ossigeno per produrre CO₂ e acqua:
C3H8 + 5 °2 → 3co2 + 4h2O
Il degrado delle biomolecole si potrebbe dire che si tratta di una reazione di combustione, poiché i prodotti finali sono CO₂ e acqua, tuttavia, questi si verificano in molti passaggi con diversi intermediari.
8. Centrifugazione del sangue
La separazione dei diversi componenti del sangue è un esempio di divisibilità. Nonostante sia un processo fisico, l'esempio è interessante, poiché i componenti per differenza di densità sono separati dalla centrifugazione.
I componenti più densi, il siero con i globuli rossi, rimarranno nella parte inferiore del tubo di centrifuga, mentre il meno denso, il plasma, rimarrà nella parte superiore.
Può servirti: atomo neutro9. Tampone bicarbonato
Bicarbonato di sodio, HCO3-, È il modo principale di trasporto di CO₂ nel prodotto corporeo delle reazioni di degradazione metabolica.
Questo composto reagisce con un protone medio per produrre acido carbonico, che è successivamente diviso in CO₂ e acqua:
HCO3- + H+ D h2Co3 D co₂ + h₂o
Poiché le reazioni sono reversibili, questo è un modo in cui il corpo ha, attraverso la respirazione, per controllare il pH fisiologico per evitare i processi di alcalosi o acidosi.
10. Atomo nucleare o divisione di fissione
Nel caso in cui un nucleo massiccio (come l'uranio-235) sia rotto (Fissioni), porterà a una performance energetica netta. Questo perché la somma delle masse dei frammenti sarà inferiore alla massa del nucleo di uranio.
Nel caso in cui la massa dei frammenti sia uguale o maggiore di quella del ferro nel picco della curva di energia di collegamento, le particelle nucleari saranno più strettamente legate rispetto al nucleo dell'uranio e che la diminuzione della massa si verifica in forma di energia secondo la forma di energia all'equazione di Einstein.
Per elementi più leggeri del ferro, la fusione produrrà energia. Questo concetto ha portato alla creazione della bomba atomica e dell'energia nucleare.
Riferimenti
- Reazioni di acidi. BBC recuperato.co.UK.
- Foist, l. (S.F.). Reazioni di eliminazione nella chimica organica. Studio recuperato.com.
- Fision nucleare (s.F.). Recuperato dall'iperfisica.

