Struttura di dimetilanilina, proprietà, sintesi, usi
- 3101
- 989
- Dante Morelli
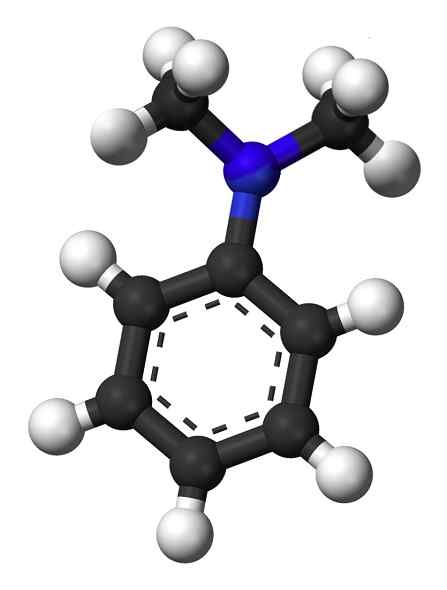
IL dimetilanilina o La dimetilfenillamina è un composto organico che è formato da un anello di benzene con un gruppo amminico sostituito con due gruppi metilici. La sua formula chimica è C8HundiciN.
È anche noto come N, N-dimetilanilina, in quanto è un derivato di Anylin in cui gli idrogeni del gruppo amminico sono sostituiti da due gruppi metilici. Questo lo rende un'ammina terziaria.
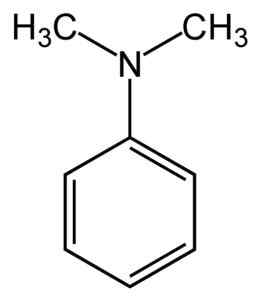 Struttura di N, N-dimetilanilina. Nessun autore leggibile dalla macchina fornita. Mysid assunto (basato su reclami di copyright). [CC BY-SA 3.0 (http: // creativeCommons.Org/licenze/by-sa/3.0/]]. Fonte: Wikipedia Commons.
Struttura di N, N-dimetilanilina. Nessun autore leggibile dalla macchina fornita. Mysid assunto (basato su reclami di copyright). [CC BY-SA 3.0 (http: // creativeCommons.Org/licenze/by-sa/3.0/]]. Fonte: Wikipedia Commons. N, la N-dimetilanilina è un liquido oleoso da giallo pallido a marrone con l'odore caratteristico delle ammine. È un composto di base e reagisce con acido nitroso che forma un nitrosocposto. Se esposto all'aria diventa marrone.
È usato nella produzione di coloranti per i dipinti. Viene anche usato come attivatore di catalizzatori di polimerizzazione e nelle miscele utilizzate per la registrazione delle immagini. A sua volta, è stato usato nella sintesi di composti antibatterici o antibiotici come alcune cefalosporine derivate dalla penicillina. N, la N-dimetilanilina è anche una base per ottenere altri composti chimici.
È un liquido combustibile e quando viene riscaldato fino a quando la decomposizione emette vapori tossici. L'esposizione acuta dell'essere umano alla N, N-dimetilanilina può portare a effetti negativi come mal di testa, vertigini, diminuzione dell'ossigeno nel sangue e colorazione della pelle bluastra, tra gli altri sintomi.
[TOC]
Struttura
La figura seguente mostra la struttura spaziale di N, N-dimetilanilina:
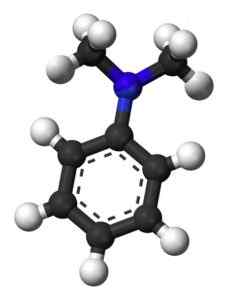 Struttura spaziale di N, N-dimetilanilina. Esquilo [dominio pubblico]. Fonte: Wikipedia Commons.
Struttura spaziale di N, N-dimetilanilina. Esquilo [dominio pubblico]. Fonte: Wikipedia Commons. Nomenclatura
- N, N-dimetilanilina
- Dimetilanilina
- Dimetilfenillamina
- N, N-dimetil Bencenamina
N viene inserito nel nome per indicare che i due gruppi metilici (-Ch3) sono attaccati all'azoto (N) e non all'anello Benncénico.
Proprietà
Stato fisico
Liquido da palmo a marrone.
Peso molecolare
121,18 g/mol.
Può servirti: anione: formazione, caratteristiche e tipiPunto di fusione
3 ºC.
Punto di ebollizione
194 ºC.
Punto d'infiammabilità
63 ºC (metodo di coppa chiusa). È la temperatura minima a cui si può attivare i vapori se viene passata una fiamma.
Pressione del vapore
0,70 mm Hg a 25 ºC.
Temperatura di autorezione
371 ºC. È la temperatura minima a bruciare spontaneamente la pressione atmosferica, senza una fonte esterna di calore o fiamma.
Densità
0,9537 g/cm3 a 20 ºC.
Indice di rifrazione
Da 1.5582 a 20 ºC.
Solubilità
In acqua è molto poco solubile: 1.454 mg/l a 25 ºC.
Liberamente solubile in alcol, cloroformio ed etere. Solubile in acetone, benzene e solventi ossigenati e clorurati.
Costante di basicità
KB 11.7, che indica la facilità con cui questo composto accetta uno ione idrogeno di acqua.
Proprietà chimiche
N, la N-dimetilanilina è un composto di base. Reagisce con l'acido acetico per dare acetato di N, n-dimetilanilinio.
Il gruppo -n (scegli3)2 della N, N-dimetilanilina è un potente attivatore di sostituzione aromatica nella posizione per dell'anello di benzene.
Reagisce con il nitrito di sodio (nano2) In presenza di acido cloridrico (HCl) che forma P-nitroso-N, N-dimetilanilinina. Anche con acido nitroso genera lo stesso nitrosado composto in posizione per.
Quando si reagiscono la N, la N-dimetilanilina con il cloruro di benzezonium, in un mezzo delicatamente acido, esiste un tipo AR-N = N-AR azococoposto, dove AR è un gruppo aromatico. Le molecole con gruppi Azo sono composti fortemente colorati.
Rischi
Quando riscaldato alla sua decomposizione emette vapori altamente tossici di ossidi di azoto noX.
È un liquido combustibile.
Si decompone lentamente in acqua esposta alla luce solare. Non è biodegrado.
È volatilizzato da terreno bagnato e superfici dell'acqua. Non evaporare il terreno secco e muoverti attraverso questo. Non si accumula nei pesci.
Può servirti: solfuro di ferro (ii): proprietà, rischi e usiPuò essere assorbito dalla pelle. Viene anche rapidamente assorbito dall'inalazione. L'esposizione dell'essere umano a N, N-dimetilanilina può ridurre il contenuto di ossigeno del sangue con conseguente colore della pelle bluastra.
L'inalazione acuta di questo composto può portare a effetti negativi per il sistema nervoso centrale e il sistema circolatorio, con mal di testa, cianosi e vertigini.
Sintesi
Può accadere in diversi modi:
- Da anilina e metanolo sotto pressione in presenza di catalizzatori acidi, come H2SW4. Si ottiene il solfato, che diventa la base aggiungendo idrossido di sodio.
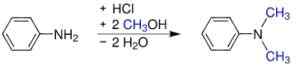 Sintesi S, N-dimetilani. Werderkli - proprio lavoro. Dominio pubblico. Fonte: Wikipedia Commons.
Sintesi S, N-dimetilani. Werderkli - proprio lavoro. Dominio pubblico. Fonte: Wikipedia Commons. - Passando un vapore di anilina e dimetil etere sull'ossido di alluminio attivato.
- Riscaldando una miscela di anilina, cloruro di anilinium e metanolo sotto pressione e quindi distillazione.
Applicazioni
Nel settore da colorare
Per la proprietà di reagire con il cloruro di Bencenodiazonium che forma azocompiestos, la N-dimetilanilina viene utilizzata come intermediario nella produzione da colorare.
È materia prima nella sintesi dei coloranti della famiglia Viola Metil.
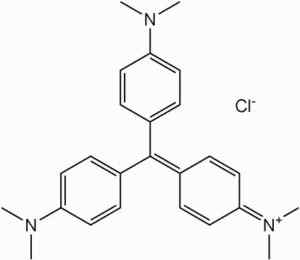 Colorazione di metil viola. Nessun autore leggibile dalla macchina fornita. Shaddack assunto (basato su reclami di copyright). [Dominio pubblico]. Fonte: Wikipedia Commons
Colorazione di metil viola. Nessun autore leggibile dalla macchina fornita. Shaddack assunto (basato su reclami di copyright). [Dominio pubblico]. Fonte: Wikipedia Commons Nella produzione di miscele fotocreenti
La N, N-dimetilanilina fa parte di una miscela fotocurabile che sperimenta la reazione di cura a seguito di un'elevata sensibilità alla luce visibile o a un infrarosso vicino, in modo che possa essere utilizzato per la registrazione di immagini o materiali di fotografia.
N, la N-dimetilanilina è uno dei componenti della miscela che causano consapevolezza delle lunghezze d'onda, in modo che la composizione sia curata con la luce della lunghezza d'onda a bassa energia.
Può servirti: derivati del benzeneSi stima che la funzione di N, N-dimetilanilina sia probabilmente quella di sopprimere la reazione di terminazione della polimerizzazione radicale causata dall'ossigeno.
Nella produzione in fibra di vetro
N, la N-dimetilanilina viene utilizzata come stresster catalitico in alcune resine in fibra di vetro.
Nella sintesi antibiotica
N, la N-dimetilanilina partecipa alla sintesi di cefalosporine basate sulle penicilline.
La penicillina solfossidi viene convertita in cefemi quando riscaldati in presenza di catalizzatori di base come N, N-dimetilanilina.
Queste cefalosporine presentano attività antibatteriche contro gli organismi Gram-positivi e gram-negativi, nonché contro gli stafilococchi resistenti alla penicillina.
 Antibiotici. Alina Kuptsova. Fonte: Pixabay.
Antibiotici. Alina Kuptsova. Fonte: Pixabay. Tuttavia, va notato che N, N-dimetilanna rimane in quegli antibiotici come impurità.
Sulle reazioni chimiche
N, la N-dimetilanilina viene utilizzata nell'attivazione dei catalizzatori di polimerizzazione olefina.
È usato insieme al pentafluorofenolo (c6F5OH) con cui forma il composto ionico [HNPHME2"+[H (OC6F5)2"-. Questo composto ionico ha uno o due protoni attivi che attivano il catalizzatore basato su un metallo di transizione.
Inoltre, nella produzione di resine, la N-dimetilanilina è stata utilizzata come acceleratore o promotore di polimerizzazione per le resine in poliestere. La sua azione genera una rapida indurimento della resina.
In diverse applicazioni
È usato nella sintesi di altri composti chimici, ad esempio vanillina e come intermediario per i farmaci.
Viene anche usato come solvente, come agente alchilante, come stabilizzatore e per produrre dipinti e rivestimenti.
Riferimenti
- S. Biblioteca nazionale di medicina. (2019). N, N-dimetilanilina. Recuperato da: pubchem.NCBI.Nlm.NIH.Gov
- Morrison, r.T. e boyd, r.N. (2002). Chimica organica. 6a edizione. Prentice-Hall.
- (2000). N, N-dimetilanilina. Riepilogo. Estratto dall'EPA.Gov
- Zanaboni, p. (1966). Composizione resinosa in poliestere insatura della stabilità HAVH e rapida cura a basse temperature usando una miscela di dimetilanil, trenhanolamina e difenilammina. O.S. Brevetto n. 3.236.915. 22 febbraio 1966.
- Nudelman, a. e McCaully, r.J. (1977). Processo per il riarrangiamento delle penicilline in cefalosporine e i loro compons intermedi. O.S. Brevetto n. 4.010.156. 1 marzo 1977.
- Kouji Inaishi (2001). Composizione fotocurabile. O.S. Brevetto n. 6.171.759 B1. 9 gennaio 2001.
- Luo, l. et al. (2012). Acido ionico Bransted. O.S. Brevetto n. 8.088.952 B2. 3 gennaio 2012.

