Diidrossicetone fosfato (DHAP) Caratteristiche e applicazioni
- 1233
- 61
- Lino Lombardi
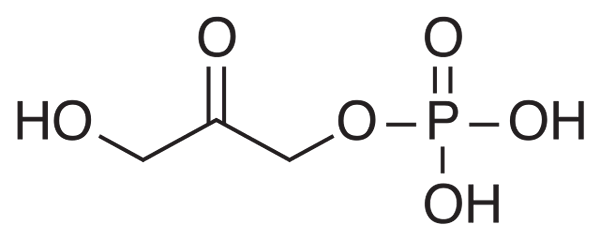
IL Diidrossicetone fosfato È un composto chimico abbreviato sotto l'acronimo DHAP. È un intermediario in alcune rotte metaboliche degli organismi viventi, come la degradazione glicolitica o la glicolisi, nonché nel ciclo di Calvin nelle piante.
Biochimicamente, il DHAP è il prodotto dell'azione di un enzima aldolasi su fruttosio-1,6-bifosfato (FBP), che provoca una rottura aldolitica che si traduce in due composti di tre carboni: DHAP e Glyceraldehyde 3-fosfato (GAP).
 Fonte: David T. MacPherson [dominio pubblico]
Fonte: David T. MacPherson [dominio pubblico] Nel ciclo di Calvin l'aldolasi esegue la reazione inversa, condensando molecole DHAP con molecole gap per formare un esoso.
[TOC]
Caratteristiche
Il DHAP è classificato all'interno delle molecole note come ketotriosa. Questi sono monosaccaridi costituiti da una catena a tre carbonio (triosa) con il gruppo carbonilico nel carbonio centrale (C2).
Il divario e i DAHP sono isomeri funzionali e costituiscono i carboidrati più semplici all'interno delle molecole organiche biologicamente attive.
Sebbene la struttura chimica di molti carboidrati comuni come GAP e DHAP siano aldeidi e chetoni, sono conferiti dal termine di carboidrati, per fare riferimento a derivati diretti dei saccaridi.
Dhap nella glicolisi
Nella glicolisi una serie di reazioni degrada il glucosio al piruvato. Questo degrado si verifica progressivamente in 10 passaggi consecutivi, in cui sono coinvolti diversi enzimi e sono prodotti una varietà di intermediari, che sono tutti fosforilati.
Il DHAP appare nella glicolisi nella quarta reazione di questo processo, che consiste nella rottura dell'FBP in due carboidrati di tre carbonio (triosasia), di cui solo il divario continua la sequenza della glicolisi, mentre il DHAP deve essere trasformato in Gap per seguire questo percorso.
Può servirti: enantiomeriQuesta reazione è catalizzata da un aldolasi (fruttosio biphat.
Questa reazione si verifica solo se l'aso da diviso ha un gruppo carbonilico in C2 e un idrossile in C4. Per questo motivo, l'isomerizzazione del glucosio-6-fosfato (G6P) in fruttosio 6-fosfato (F6P) si verifica precedentemente.
Nella quinta reazione della glicolisi, il DHAP è anche coinvolto, nel caso dell'isomerizzazione gap da parte dell'isomesso a tre fasi o dell'enzima fosfato di Tim. Con questa reazione è completata la prima fase di degradazione del glucosio.
Reazione aldolasi
Sulla rottura aldolica ci sono due intermediari, in cui il DHAP per il 90% della miscela di equilibrio.
Esistono due tipi di aldlasasi: a) Le cellule di tipo I di tipo I sono presenti nelle cellule animali e vegetali ed è caratterizzato dalla formazione di una base Schiff tra il sito attivo enzimatico e il carbonile FBP. b) Il tipo II aldolasi si trova in alcuni batteri e funghi, ha un metallo sul sito attivo (di solito Zn).
La rottura aldolica inizia con l'adesione del substrato al sito attivo e la rimozione di un protone del gruppo β-idrossile, formando la base Schiff proton (IMINIO CATION). La rottura dei carboni C3 e C4 produce il rilascio del divario e la formazione di un intermediario chiamato In Love.
L'enamina viene successivamente stabilizzata, quindi si forma un catione di iminio che viene idrolizzato, che alla fine rilascia il DHAP e quindi rigenera l'enzima libero.
Può servirti: acido maleico: struttura, proprietà, ottenimento, usiNelle cellule con aldosos di tipo II2+, Quello che stabilizza l'intermediario si innamora di essere in grado di rilasciare il DHAP.
Tim Reaction
Come accennato, la concentrazione di bilanciamento DHAP è maggiore di quella di GAP.
Questa trasformazione si verifica grazie all'enzima Tim. Questa è la quinta reazione del processo di degradazione glicolitica e in esso i carboni C1 e C6 diventano i carboni C3 del divario, mentre i carboni C2 e C5 diventano C2 e C3 e C4 del glucosio si trasformano nel C1 del C1 SPACCO.
L'enzima Tim è considerato "enzima perfetto" perché la diffusione controlla la velocità della reazione, il che significa che il prodotto si forma rapidamente come il sito attivo dell'enzima e il suo substrato insieme.
Nella reazione di trasformazione DHAP a GAP, si forma un intermediario chiamato eNediolo. Questo composto è in grado di dare i protoni dei gruppi di idrossilli a un residuo dal sito attivo dell'enzima Tim.
Dhap nel ciclo di Calvin
Il ciclo di Calvin è il ciclo di riduzione fotosintetica del carbonio (PCR) che costituisce la fase scura del processo di fotosintesi delle piante. In questa fase, i prodotti (ATP e NADPH) ottenuti nella fase luminosa del processo vengono utilizzati per produrre carboidrati.
Può servirti: cycopropane (C3H6)In questo ciclo, si formano sei molecole di gap, di cui due si trasformano in DHAP mediante isomerizzazione, grazie all'azione dell'enzima Tim, in una reazione inversa a quella che si è verificata nella degradazione della glicolisi. Questa reazione è reversibile, sebbene l'equilibrio, nel caso di questo ciclo e, a differenza della glicolisi, sia spostato per la conversione del gap in DHAP.
Queste molecole DHAP possono quindi seguire due modi, si è una condensa aldolica catalizzata da un'aldolasi, in cui si condensa con una molecola gap per formare FBP.
L'altra reazione che può prendere uno dei DHAP è un'idrolisi fosfato catalizzata da una bifosfatasi beheptula. In quest'ultimo percorso reagisce con un erithro per formare 1.7-bifosfato.
DHAP nella gluconeogenesi
Nella gluconeogenesi alcuni composti non glucidici come piruvato, lattato e alcuni aminoacidi vengono convertiti in glucosio. In questo processo, il DHAP appare nuovamente dall'isomerizzazione di una molecola di gap mediante l'azione di Tim, e quindi attraverso una condensa aldica per diventare FBP.
Riferimenti
- Bailey, p. S., & Bailey, C. A. (1998). Chimica organica: concetti e applicazioni. Ed. Pearson Education.
- Devlin, t. M. (1992). Libro di testo di biochimica: con correlazioni cliniche. John Wiley & Sons, Inc.
- Garrett, r. H., & Grisham, C. M. (2008). Biochimica. Ed. Thomson Brooks/Cole.
- Nelson, d. L., & Cox, m. M. (2006). Lechinger Principles of Biochemistry 4th Edition. Ed Omega. Barcellona.
- Rawn, j. D. (1989). Biochimica (NO. 577.1 crudo). Ed. Inter-American-McGraw-Hill
- Voet, d., & Voet, J. G. (2006). Biochimica. Ed. Pan -American Medical.
- « Storia di Fenaquistiscopio, caratteristiche, operazioni
- Discovery Java, caratteristiche fisiche e sociali »

