Difenilammina
- 1029
- 289
- Lino Lombardi
Qual è la defilamina?
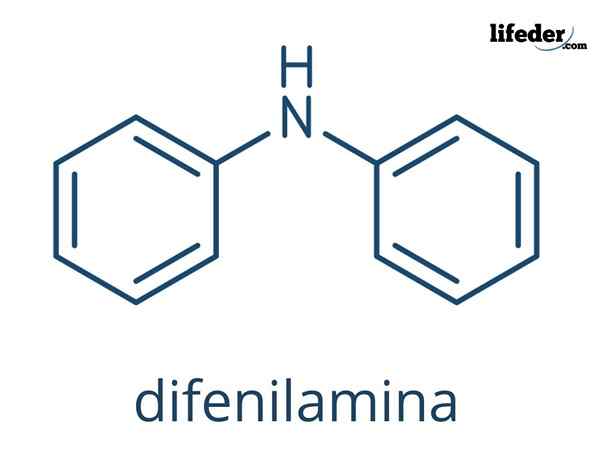
IL Difenilammina È un composto organico la cui formula chimica è (c6H5)2NH. Il suo nome indica che è un'ammina, così come la sua formula (-nh2). D'altra parte, il termine "diffenico" si riferisce alla presenza di due anelli aromatici legati all'azoto. Di conseguenza, la definizione è un'ammina aromatica.
Nel mondo dei composti organici, la parola aromatica non è necessariamente correlata all'esistenza dei suoi odori, ma alle caratteristiche che definiscono i loro comportamenti chimici contro alcune specie.
Nel caso della difenilammina, la sua aromaticità e il fatto che il loro solido presente un aroma distintivo coincide. Tuttavia, la fondazione o i meccanismi che governano le sue reazioni chimiche possono essere spiegate dal suo carattere aromatico, ma non per il suo piacevole aroma.
La sua struttura chimica, basicità, aromaticità e interazioni intermolecolari sono le variabili responsabili delle sue proprietà: dal colore dei suoi cristalli alla sua applicabilità come agente antiossidante.
Struttura chimica di Decilamina

Nelle immagini superiori sono rappresentate le strutture chimiche della diffenilamina. Le sfere nere corrispondono agli atomi di carbonio, agli atomi di idrogeno e al blu all'atomo di azoto.
La differenza tra le due immagini è il modello di come rappresentano graficamente la molecola. Nella parte inferiore evidenzia l'aromaticità degli anelli con le linee punteggiate in nero e, anche la geometria piatta di questi anelli è evidenziata.
Nessuna delle due immagini mostra la coppia solitaria di elettroni non condivisi sull'atomo di azoto. Questi elettroni "camminano" attraverso il sistema π coniugato dei doppi legami negli anelli. Questo sistema forma una sorta di cloud circolante che consente interazioni intermolecolari; cioè, con altri anelli di un'altra molecola.
Può servirti: termometro di laboratorio: caratteristiche, a cosa serve, uso, esempiQuanto sopra significa che la coppia di azoto non condivisa sta camminando attraverso entrambi gli anelli, distribuendo in questi la sua densità elettronica, e poi tornano in azoto, per ripetere di nuovo il ciclo.
In questo processo, la disponibilità di questi elettroni diminuisce, con conseguente diminuzione della basicità della dipelamina (la sua tendenza a donare gli elettroni come base di Lewis).
Usi/applicazioni di dipenilammina
La difenilammina è un agente ossidante in grado di svolgere una serie di funzioni, e tra queste sono le seguenti:
- Durante la loro conservazione, le mele e le pere sperimentano un processo fisiologico chiamato scandalgamento, legato alla produzione di Trienos coniugati, che porta al danno cutaneo dei frutti. L'azione della dipenilammina consente di aumentare il periodo di conservazione, riducendo il danno alla frutta al 10 % di ciò che si osserva in loro assenza.
- Quando si combattono l'ossidazione, la difenilammina e i suoi derivati estendono il funzionamento dei motori evitando l'ispessimento dell'olio usato.
- La difenilammina viene utilizzata per limitare l'azione dell'ozono nella produzione di gomma.
- La difenilammina viene utilizzata nella chimica analitica per il rilevamento dei nitrati (no3-), Clorati (CLO3-) e altri agenti ossidanti.
- È un indicatore utilizzato nei test di rilevamento dell'avvelenamento da nitrati.
- Quando l'RNA viene idrolizzato per un'ora, reagisce con la defilamina; Ciò consente la sua quantificazione.
- Nella medicina veterinaria, la popolamina dipe viene utilizzata topicamente nella prevenzione e nel trattamento delle manifestazioni del verme boreride negli animali da riproduzione.
- Alcuni dei derivati della duelamina appartengono alla categoria di farmaci antinfiammatori non steroidei. Possono anche avere effetti farmacologici e terapeutici come antimicrobici, analgesici, anticonvulsivanti e attività anticancro.
Preparazione di dipenilammina
Naturalmente, la decilamina viene prodotta nella cipolla, nei colantro, nelle foglie del tè verde e nero, e nei gusci dei frutti di agrumi. Sinteticamente, ci sono molti percorsi che portano a questo composto, come:
Deaminazione termica di anilina
È preparato mediante deaminazione termica di anilina (c6H5NH2) In presenza di catalizzatori ossidanti.
Se l'anilina in questa reazione non incorpora un atomo di ossigeno alla sua struttura, perché si ossida? Perché l'anello aromatico è un gruppo di attrattori di elettroni, a differenza dell'atomo H, che dona la sua bassa densità di azoto elettronico nella molecola.
2 c6H5NH2 => (C5H5)2 NH+NH3
Inoltre, l'anilina può reagire con il sale di cloridrato di anilina (c6H5NH3+Cl-) sotto un riscaldamento di 230 ºC per venti ore.
C6H5NH2 + C6H5NH3+Cl- => (C5H5)2 NH
Reazione di fenotiazina
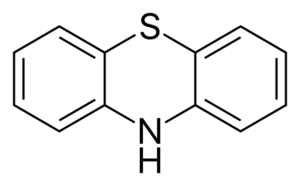
La dipenilammina ha origine diversi derivati se combinati con reagenti diversi. Uno di questi è la fenotiazina, che, sintetizzante con zolfo è un precursore di derivati con azione farmaceutica.
(C6H5)2Nh +2s => s (c6H4) NH +H2S

Proprietà di dipenilammina
La dipenilammina è un solido cristallino bianco che, a seconda delle sue impurità, può acquisire toni bronchneali, ambra o gialli. Ha un piacevole aroma di fiori, ha un peso molecolare 169,23 g/mol e una densità di 1,2 g/ml.
Le molecole di questi solidi interagiscono dalle forze di van der Waals, tra cui i ponti idrogeno formati da atomi di azoto (NH-NH) e lo stacking di anelli aromatici, appoggiando le loro "nuvole elettroniche" una sull'altra.
Può servirti: zinco solfuro (ZNS)Mentre gli anelli aromatici occupano molto. Quanto sopra fa sì che il solido non abbia un punto di fusione molto elevato (53 ºC).
Tuttavia, in stato liquido le molecole sono più separate e l'efficacia dei ponti idrogeno migliora. Allo stesso modo, la defilamina è relativamente pesante, che ha bisogno di molto calore per spostarsi in una fase gassosa (302 ºC, il suo punto di ebollizione). Ciò è dovuto anche in parte al peso e alle interazioni degli anelli aromatici.
Solubilità e basicità
È molto insolubile in acqua (0,03 g/100 g di acqua) a causa del carattere idrofobo dei suoi anelli aromatici. Invece, è molto solubile in solventi organici come benzene, tetracloruro di carbonio (CCL4), acetone, etanolo, piridina, acido acetico, ecc.
La sua costante di acidità (PKA) è 0,79, che si riferisce all'acidità del suo acido coniugato (C6H5NH3+). Il protone aggiunto all'azoto ha la tendenza a separarsi, perché la coppia di elettroni con cui è collegato può attraversare gli anelli aromatici. Pertanto, alta instabilità C6H5NH3+ Riflette la bassa basicità della diffenilamina.
Riferimenti
- The Lubrizol Corporation. (2018). Antiossidanti difenilammina. Recuperato da Lubrizol.com
- Arun Kumar Mishra, Arvind Kumar. (2017). Applicazioni farmacologiche della difenilammina e il suo derivato come potente composto bioattivo: una revisione. Composti bioattivi attuali, volume 13.
- Prepchem. (2015-2016). Preparazione della difenilammina. Recuperato da Prepchem.com
- PUBCHEM. (2018). Difenilammina. Recuperato da Pubchem.NCBI.Nlm.NIH.Gov.
- Wikipedia. (2018). Difenilammina. Recuperato da.Wikipedia.org

