Denaturazione proteica cosa è, fattori, conseguenze
- 4753
- 1118
- Kayla Serr
Qual è la denaturazione delle proteine?
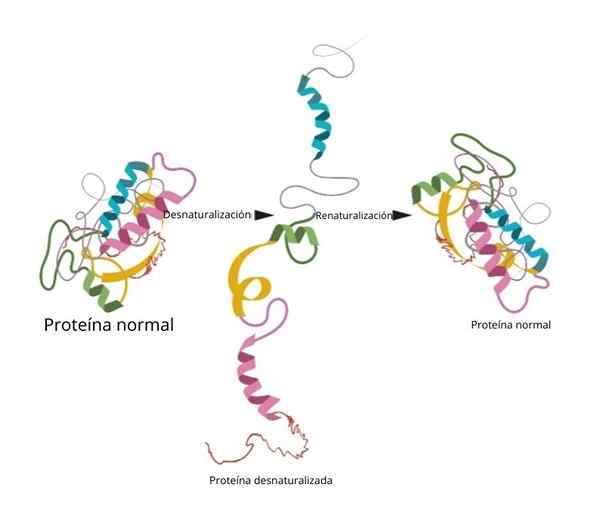
IL denaturazione delle proteine Consiste nella perdita di struttura tridimensionale a causa di diversi fattori ambientali, come temperatura, pH o determinati agenti chimici. La perdita della struttura provoca la perdita della funzione biologica associata a quella proteina, tra l'altro sia enzimatico, strutturale, trasportatore.
La struttura della proteina è altamente sensibile ai cambiamenti. La destabilizzazione di un singolo ponte idrogeno essenziale può denaturalizzare la proteina. Allo stesso modo, ci sono interazioni che non sono strettamente essenziali per svolgere la funzione proteica e, in caso di destabilizzazione, non ha alcun effetto sul funzionamento.
Struttura proteica
Per comprendere i processi di denaturazione delle proteine, dobbiamo sapere come sono organizzate le proteine. Questi hanno struttura primaria, secondaria, terziaria e quaternaria.
Struttura primaria
È la sequenza di aminoacidi che compongono questa proteina. Gli aminoacidi sono i blocchi fondamentali che costituiscono queste biomolecole e ci sono 20 tipi diversi, ciascuno con particolari proprietà fisiche e chimiche. Si uniscono per mezzo di un collegamento peptidico.
Struttura secondaria
In questa struttura questa catena lineare di aminoacidi inizia ad essere piegata da ponti idrogeno. Esistono due strutture secondarie di base: l'elica α, a forma di spirale; e la foglia pieghevole β, quando due catene lineari sono allineate in parallelo.
Struttura terziaria
Coinvolge altri tipi di forze che si traducono in una piegatura specifica della forma tridimensionale.
Le catene R dei residui di aminoacidi che compongono la struttura della proteina possono formare ponti disolfuro e le parti idrofobiche delle proteine sono raggruppate all'interno, mentre l'idrofila rivolta all'acqua. Le forze di Van der Waals fungono da stabilizzatore delle interazioni descritte.
Può servirti: isoleucina: caratteristiche, funzioni, biosintesi, ciboStruttura quaternaria
È costituito da aggregati di unità proteiche.
Quando una proteina viene denaturata, perde la struttura quaternaria, terziaria e secondaria, mentre il primario rimane intatto. Le proteine ricche di collegamenti disolfuro (struttura terziaria) forniscono una maggiore resistenza alla denaturazione.
Fattori che causano denaturazione
Qualsiasi fattore che destabilizza i legami non covalenti responsabili del mantenimento della struttura nativa della proteina può produrre la sua denaturazione. Tra i più importanti che possiamo menzionare:
ph
A valori di pH molto estremi, media acida o base, la proteina può perdere la sua configurazione tridimensionale. L'eccesso henes h+ e oh- nel mezzo destabilizza le interazioni proteiche.
Questo cambio di modello ionico produce denaturazione. La denaturazione del pH può essere reversibile in alcuni casi e in altri irreversibili.
Temperatura
La denaturazione termica si verifica aumentando la temperatura. Negli organismi che vivono in condizioni ambientali medie, le proteine iniziano a destabilizzare a temperature superiori a 40 ° C. Chiaramente, le proteine dell'organismo termofilo possono supportare questi intervalli di temperatura.
Gli aumenti della temperatura vengono tradotti in aumento dei movimenti molecolari che colpiscono i ponti idrogeno e altri legami non covalenti, con conseguente perdita di struttura terziaria.
Questi aumenti di temperatura portano alla velocità di reazione, se stiamo parlando di enzimi.
Sostanze chimiche
Le sostanze polari - come l'urea - ad alte concentrazioni colpiscono i ponti idrogeno. Allo stesso modo, le sostanze non polari possono avere conseguenze simili.
I detergenti possono anche destabilizzare la struttura proteica; Tuttavia, non è un processo aggressivo e sono per lo più reversibili.
Può servirti: scarafaggio tedesco: caratteristiche, riproduzione, ciboRiducendo gli agenti
Il β-mercaptoetanolo (Hoch2Ch2sh) è un agente chimico di uso frequente in laboratorio per denaturalizzare le proteine. È responsabile della riduzione dei ponti disolfuro tra i rifiuti di aminoacidi. Può destabilizzare la struttura terziaria o quaternaria della proteina.
Un altro agente riducente con funzioni simili è Ditiotreitol (DTT). Inoltre, altri fattori che contribuiscono alla perdita di struttura nativa nelle proteine sono metalli pesanti ad alte concentrazioni e radiazioni ultraviolette.
Conseguenze del denaturazione delle proteine
Quando si verifica la denaturalizzazione, la proteina perde la sua funzione. Le proteine funzionano in modo ottimale quando sono nel loro stato nativo.
La perdita della funzione non è sempre associata a un processo di denaturazione. Un piccolo cambiamento nella struttura proteica può portare alla perdita di funzione senza destabilizzare l'intera struttura tridimensionale.
Il processo può o meno essere irreversibile. In laboratorio, se le condizioni sono invertite che la proteina ritorna alla sua configurazione iniziale.
Renaturalizzazione
Uno degli esperimenti più famosi e conclusivi sulla rinascita è stato evidenziato nel ribonucleasi a.
Quando i ricercatori hanno aggiunto agenti denaturati come urea o β-mercaptanolo, la proteina è stata denaturata. Se questi agenti fossero rimossi, la proteina è tornata alla loro conformazione nativa e potrebbe svolgere la propria funzione con un'efficienza del 100 %.
Una delle conclusioni più importanti di questa ricerca è stata dimostrare sperimentalmente che la conformazione tridimensionale della proteina è data dalla sua struttura primaria.
In alcuni casi, il processo di denaturalizzazione è totalmente irreversibile. Ad esempio, quando cuociamo un uovo stiamo applicando il calore nelle proteine (il principale è l'albumina) che lo costituisce, il chiaro prende un aspetto solido e biancastro. Intuitivamente può concludere che, sebbene lo raffreddiamo, non tornerà alla sua forma iniziale.
Può servirti: ovogenesi: fasi, caratteristiche negli animali e nelle pianteNella maggior parte dei casi, il processo di denaturalizzazione è accompagnato dalla perdita di solubilità. Anche la viscosità, la velocità di diffusione è ridotta e cristallizza più facilmente.
Proteine Chaperonas
Chaperonas o chaperonin Proteins sono responsabili della prevenzione della denaturazione di altre proteine. Reprimono anche alcune interazioni che non sono adeguate tra le proteine per garantire una corretta piegatura di esse.
Quando la temperatura media aumenta, queste proteine aumentano la loro concentrazione e agiscono prevenendo la denaturazione di altre proteine. Questo è il motivo per cui sono anche chiamati "proteine di shock termico" o HSP per il suo acronimo in inglese (Proteine di shock termico).
I chaperonine sono analoghi a una gabbia o canna che protegge la proteina di interesse all'interno.
Queste proteine che rispondono alle situazioni di stress cellulare sono state riportate in vari gruppi di organismi viventi e sono altamente conservate. Esistono diversi tipi di chaperonine e sono classificati in base al loro peso molecolare.

