Bowman Capsule Structure, istologia, funzioni
- 2490
- 548
- Silvano Montanari
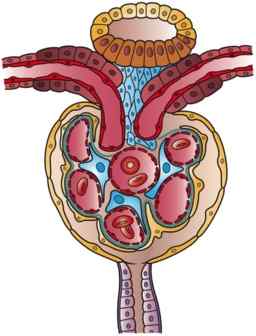
IL Bowman Capsule Rappresenta il segmento iniziale della componente tubulare del nefrone, unità anátomo funzionale del rene in cui vengono eseguiti i processi destinati alla produzione di urina e con cui il rene contribuisce alla conservazione dell'omeostasi dell'organismo.
Fu nominato in onore dell'oftalmologo inglese e anatomista medico Sir William Bowman, che scoprì la sua esistenza e pubblicò la sua descrizione istologica per la prima volta nel 1842.
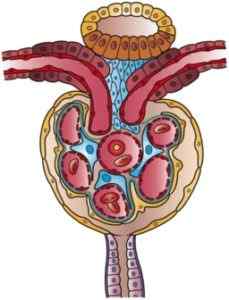 Illustrazione di un nefrone (fonte: opere d'arte di Holly Fischer [CC di 3.0 (https: // creativeCommons.Org/licenze/di/3.0)] via Wikimedia Commons)
Illustrazione di un nefrone (fonte: opere d'arte di Holly Fischer [CC di 3.0 (https: // creativeCommons.Org/licenze/di/3.0)] via Wikimedia Commons) C'è una certa confusione in letteratura in relazione alla nomenclatura dei segmenti iniziali del nefrone, tra cui la capsula Bowman è inclusa. A volte è descritto come una parte diversa del glomerulo e costituisce con esso il corpuscolo renale, mentre per altri ha una funzione come membro del glomerulo.
Indipendentemente dal fatto che nelle descrizioni anatomiche la capsula faccia parte del glomerulo, il fatto è che entrambi gli elementi sono così intimamente associati nella sua struttura e funzione, che il termine glomerulo si sveglia in chi pensa l'idea di una sferico Navi.
In caso contrario, la capsula sarebbe semplicemente un ricettacolo in cui il fluido filtrato nel glomerulo viene versato, ma non avrebbe una parte nello stesso processo di filtrazione glomerulare. Il che non è così, poiché lei, come si vede, fa parte di quel processo a cui contribuisce in modo speciale.
[TOC]
Struttura e istologia
La capsula di Bowman è come una piccola sfera il cui muro è invaginato nel settore vascolare. In questa invaginazione, la capsula viene penetrata dallo snack dei capelli, che ha origine nell'arteriola afferente e che porta anche il sangue al glomerulo, dove esce anche l'arteriola eferente che toglie il sangue dal glomerulo.
L'estremità opposta della capsula, chiamata polo urinario, è presentata come se la parete della sfera avesse un foro a cui è collegata la fine del primo segmento che inizia la funzione tubolare stessa.
Questa parete esterna della capsula è un epitelio piatto ed è chiamata epitelio parietale della capsula Bowman. Cambia la struttura quando si effettua la transizione verso l'epitelio del tubulo prossimale nel polo urinario e verso l'epitelio viscerale nel polo vascolare.
Può servirti: papille funghiformiL'epitelio invaggato è chiamato viscerale perché avvolge i capillari glomerulari come se fossero un viscero. È formato da cellule chiamate podociti che abbracciano, che li coprono, ai capillari e che hanno caratteristiche molto particolari.
I podociti sono organizzati in un singolo strato, emettendo prolungazioni che interrogavano con le estensioni dei podociti vicini, lasciando spazi tra loro chiamati pori in schisi o filtrazioni e che sono soluzioni di continuità per la fase del filtraggio.
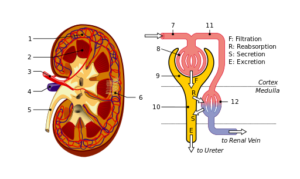 Struttura renale e nefron: 1. Corteccia renale; 2. Midollo; 3. Arteria renale; 4. Vene renali; 5. Uretere; 6. Nefroni; 7. ARTERIOLA AFFERE; 8. Glomerulus; 9. Bowman Capsule; 10. Tubuli e hanle; undici. Capillari peritubulari (Fonte: File: Physiology_OF_Nephron.SVG: Madhero88File: KidneysRurtures_Piom.SVG: Piotr Michał Jaworski; PIOM in PLDERivative Work: Daniel Sachse (Antares42) [CC BY-SA 3.0 (https: // creativeCommons.Org/licenze/by-sa/3.0)] via Wikimedia Commons)
Struttura renale e nefron: 1. Corteccia renale; 2. Midollo; 3. Arteria renale; 4. Vene renali; 5. Uretere; 6. Nefroni; 7. ARTERIOLA AFFERE; 8. Glomerulus; 9. Bowman Capsule; 10. Tubuli e hanle; undici. Capillari peritubulari (Fonte: File: Physiology_OF_Nephron.SVG: Madhero88File: KidneysRurtures_Piom.SVG: Piotr Michał Jaworski; PIOM in PLDERivative Work: Daniel Sachse (Antares42) [CC BY-SA 3.0 (https: // creativeCommons.Org/licenze/by-sa/3.0)] via Wikimedia Commons) Podociti e cellule endoteliali che coprono una membrana basale su cui supportano e hanno anche soluzioni di continuità per il passaggio dell'acqua e delle sostanze. Le cellule endoteliali sono fenestradas e consentono anche la filtrazione.
Quindi questi tre elementi: endotelio capillare, membrana basale ed epitelio viscerale della capsula Bowman, costituiscono insieme la membrana o la barriera di filtrazione.
Funzioni
La capsula è associata al processo di filtrazione glomerulare. Da un lato, perché fa parte della copertura epiteliale dei podociti che circonda i capillari glomerulari. Contribuisce anche la sintesi della membrana basale su cui è supportato questo epitelio e l'endotelio capillare glomerulare.
Queste tre strutture: endotelio capillare, membrana basale e epitelio viscerale della capsula Bowman, costituiscono la membrana così chiamata o la barriera di filtrazione e ognuno di essi ha le sue caratteristiche di permeabilità che contribuiscono alla selettività globale di quella barriera.
Inoltre, il volume del fluido che penetra nello spazio di Bowman, insieme al grado di rigidità che la parete esterna capsulare si oppone, determina la genesi di una pressione intracapsulare che aiuta a modulare l'effettiva pressione di filtrazione e ad aumentare il liquido attraverso il tubulo associato.
Può servirti: periosteo: caratteristiche, funzioni e istologiaDeterminanti della grandezza della filtrazione glomerulare
Una variabile che raccoglie l'entità del processo di filtrazione glomerulare è il volume di filtrazione glomerulare così chiamata (VFG), che è il volume del liquido che viene filtrato in tutti i glomeruli nell'unità temporale. Il suo valore normale medio è di circa 125 ml/min o 180 L/giorno.
L'entità di questa variabile è determinata dal punto di vista fisico da due fattori, vale a dire il coefficiente di filtrazione o ultrafiltrazione (KF) così chiamata (KF) e la pressione di filtrazione effettiva (PEFF). Cioè: vfg = kf x peff (equazione 1)
Coefficiente di filtrazione (KF)
Il coefficiente di filtrazione (KF) è il prodotto della conducibilità idraulica (LP), che misura la permeabilità dell'acqua di una membrana in ml/min per unità di area e unità di pressione di attuazione, da parte della superficie (a) della membrana del filtro, Vale a dire kf = lp x a (equazione 2).
L'entità del coefficiente di filtrazione indica il volume del fluido filtrato per unità di tempo e per unità di trasmissione effettiva. Sebbene sia molto difficile da misurare direttamente, può essere ottenuto dall'equazione 1, dividendo VFG/PEFF.
Il KF nei capillari glomerulari è di 12,5 ml/min/mmHg per c/100 g di tessuto, valore circa 400 volte superiore al KF di altri sistemi capillari del corpo, dove è possibile filtrare circa 0,01 ml/min/mm Hg per 100 g di tessuto. Confronto che mostra l'efficienza del filtro glomerulare.
Pressione di filtrazione efficace (PEFF)
La pressione effettiva di filtrazione rappresenta il risultato della somma algebrica delle diverse forze di pressione che favoriscono o si oppongono alla filtrazione. Esiste un gradiente di pressione idrostatica (ΔP) e un'altra pressione osmotica (oncotica, Δп) determinata dalla presenza di proteine nel plasma.
Il gradiente di pressione idrostatica è la differenza di pressione tra l'interno del capillare glomerulare (PCG = 50 mm Hg) e lo spazio della capsula Bowman (PCB = 12 mm Hg). Come visto, questo gradiente è diretto dal capillare alla capsula e promuove lo spostamento del fluido al riguardo.
Può servirti: scheletro appendicolare: funzioni e ossaIl gradiente di pressione osmotica muove il liquido inferiore a una pressione osmotica più elevata. Solo le particelle che non filtrano esercitano questo effetto. Le proteine non filtrano. Il suo пcb è 0 e nel capillare glomerulare пcg è 20 mm Hg. Questo gradiente muove il liquido dalla capsula al capillare.
La pressione effettiva può essere calcolata applicando PEFF = ΔP-Δп; = (PCG-PCB)-(пcg -;cb); = (50-12)-(20-0); = 38-20 = 18 mm Hg. Vi è quindi una pressione di filtrazione efficace o netta di circa 18 mm Hg che determina un VFG di circa 125 ml/min.
Indice di filtrazione (if) delle sostanze presenti nel plasma
È un indicatore della facilità (o della difficoltà) con cui una sostanza presente nel plasma può attraversare la barriera di filtrazione. L'indice si ottiene dividendo la concentrazione della sostanza in filtraggio (FX) tra la sua concentrazione nel plasma (PX), cioè: IFX = FX/ PX.
L'intervallo di valori IF è compreso tra un massimo di 1 per quelle sostanze che filtrano liberamente e 0 per quelle che non filtrano nulla. I valori intermedi sono per particelle con difficoltà intermedie. Più vicino a 1 il valore, migliore è la filtrazione. Più vicino a 0, più difficile da filtrare.
Uno dei fattori che determina l'IF è la dimensione della particella. Quelli che hanno diametri inferiori a 4 nm filtra liberamente (if = 1). Man mano che la dimensione cresce e si avvicina a quella dell'albumina, la FE è ridotta. Le particelle di dimensioni dell'albumina, o più grandi, hanno 0 IFS di 0.
Un altro fattore che aiuta a determinare l'IF è carichi elettrici negativi sulla superficie molecolare. Le proteine hanno un sacco di carico negativo, che viene aggiunto alla loro dimensione per ostacolare la loro filtrabilità. Il motivo è che i pori hanno cariche negative che respingono quelle delle proteine.
Riferimenti
- Ganong WF: funzione renale e minzione, in Revisione della fisiologia medica, 25 ° ed. New York, McGraw-Hill Education, 2016.
- Guyton AC, Hall JI: The U urinary System, in Libro di testo di fisiologia medica , 13 ° ED, AC Guyton, JE Hall (a cura di). Filadelfia, Elsevier Inc., 2016.
- Lang F, Kurtz A: Niere, in Physiologie des Menschen AcHyophysiologie, 31 ° ED, RF Schmidt et al (eds). Heidelberg, Springer Medizin Verlag, 2010.
- Silbernagl S: die funkction der nieren, in Fisiologia, 6 ° ed; R Klinke et al (Eds). Stuttgart, Georg Thieme Verlag, 2010.
- Stahl Rak et al: Niere UNDOITENDE HARNWEGE, IN Klinche Pathophysiologie, 8 ° ed, W Siegenthaler (ed). Stuttgart, Georg Thieme Verlag, 2001.
- « Quali sono le articolazioni fibrose? Tipi e caratteristiche
- Origine Baragonnosia, concetto, test, disturbi correlati »

