Cloruro di calcio (CACL2)
- 3399
- 812
- Ruth Cattaneo
Spieghiamo cosa cloruro di calcio, struttura, proprietà fisiche e chimiche, come è sintetizzato e le sue applicazioni sono
Cos'è il cloruro di calcio?
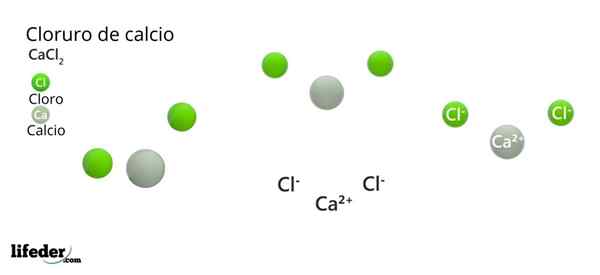
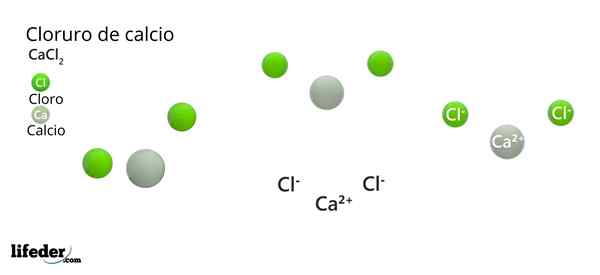
Lui Cloruro di calcio (Cacl2) È un sale inorganico composto da calcio, metallo alcalino e cloro alogeno. In quel composto ci sono diverse interazioni elettrostatiche che definiscono l'aspetto esterno dei loro cristalli e il resto delle sue proprietà fisiche.
È anche accompagnato da molecole d'acqua, formando cocl formula generale idrati2· XH2Oppure, con x = 0, 1, 2, 4 e 6. Quando x = 0, il sale manca di acqua ed è anidrid, come indicato dalla sua formula chimica sopra menzionata.
Nell'immagine superiore sono illustrate alcune parti solide di CACL2. In condizioni di poca umidità, è possibile.
Formula
La sua formula chimica è CACL2: Lo esprime per ogni ca ione2+ Ci sono due ioni cl- che neutralizzano il carico positivo. Il gruppo di calcio in metallo 2 della tabella periodica (SR. Scholambara)- produce i suoi due elettroni ad ogni atomo di cloro, elemento di gruppo 17.
Struttura del cloruro di calcio
Nell'immagine superiore è illustrata la struttura CACL2 anidride. Le sfere verdi corrispondono agli ioni cl-, mentre bianco agli ioni ca2+. Queste sfere sono fissate in un parallelepiped, che non è altro che la cellula ortorrombica unitaria dei cristalli.
La struttura può dare la falsa idea che il calcio predomina; Tuttavia, se sono riprodotte più ripetizioni della cella unitaria, la maggiore abbondanza delle sfere verdi sarebbe chiara: gli ioni cl-.
D'altra parte, ca ioni2+ Hanno radio ioniche più piccole rispetto agli ioni Cl-. Questo perché, quando perdono elettroni, i nuclei degli atomi esercitano una maggiore forza attraente sugli strati elettronici esterni, il che riduce il raggio ionico.
Nel caso del CL-, Questo ha un ulteriore elettrone che non può essere attratto dalla stessa forza, aumentando così il suo raggio ionico.
Può servirti: soluzioni acquoseGeometria molecolare e complessi acquosi di calcio
Al centro del parallelepiped la CA2+ È circondato da sei cl-. Quattro di questi si trovano in un piano quadrato e gli altri due si trovano perpendicolarmente (le sfere verdi più remote della sfera bianca).
Come risultato della disposizione di questi ioni, intorno alla CA2+ Un octaedro è "arma", assegnando così una geometria molecolare ottaedrica.
Considerando come sono disposte le sfere verdi, una molecola d'acqua può sostituire una di queste, che si verifica con la corsa2· H2O, forse nel piano quadrato. Questo fatto modifica la struttura cristallina e, poiché l'acqua sostituisce le sfere verdi, la disposizione degli ioni cambia di più.
Quando tutti gli ioni cl- Sono sostituiti da molecole d'acqua, si forma il cacl idrato2· 6h2O. A questo punto l'ettaedro è "acquoso" e le molecole sono ora in grado di interagire tra loro con i ponti idrogeno (CA2+ Oh-h-oh2).
Consecutivamente, il calcio può accettare ancora più molecole d'acqua senza alterare la proporzione stabilita. Ciò significa che il CACL2· 6h2O può adottare altre strutture complesse, al punto da considerare polimeri cristallini di calcio e acqua.
Tuttavia, queste strutture sono meno stabili di quelle erette dalle interazioni elettrostatiche (CA2+ e cl-) dal sale anidride.
Usi/applicazioni di cloruro di calcio
Le principali applicazioni del cloruro di calcio sono:
- Evita il congelamento dell'acqua durante l'inverno. Il cloruro di calcio genera molto calore durante la dissoluzione e quindi, aumentando la temperatura, si verifica la fusione del ghiaccio. Per questo motivo viene utilizzato per ridurre il rischio di circolazione di persone e veicoli durante la stazione fredda.
- Aiutare a controllare la polvere su strade non asfaltate.
- Accelerare la velocità di asciugatura del cemento una volta versato.
- Fluidi di cachl2 L'efficienza della perforazione per l'estrazione del gas dai loro depositi sotterranei aumenta, così come il petrolio.
- Le piscine vengono aggiunte per ridurre l'erosione subita dal cemento delle sue pareti. Il calcio sedimentato svolge questa funzione.
- Poiché si tratta di un sale igroscopico, il cloruro di calcio può essere usato come dissuazione, essendo in grado di abbassare l'umidità dell'aria circostante e, quindi, dalle sostanze a contatto con quell'aria.
- È usato come conservante in alcuni alimenti, nonché ad additivo in diversi, come bevande energetiche utilizzate da atleti, formaggi, birre, ecc.
- Nella pratica medica ha anche utilità nel trattamento della depressione causata da un sovradosaggio di solfato di magnesio, nonché nell'avvelenamento da piombo.
Sintesi di cloruro di calcio
Le fonti naturali di questo composto sono le salmueras estratte dai mari o dai laghi.
Tuttavia, la sua fonte principale deriva dal processo di Solvay, in cui il calcare (Caco3) subire una serie di trasformazioni fino a derivare nel cloruro di calcio per -prodotto:
2NACL (AQ) + Caco3(s) NA2Co3(s) + cacl2(AC)
Il prodotto di interesse di questo processo è in realtà carbonato di sodio, Na2Co3.
Proprietà del cloruro di calcio
Proprietà fisiche e prelibatezze
È un solido bianco, toilette e igroscopico. Questa tendenza ad assorbire l'umidità dell'ambiente è dovuta alla basicità degli ioni CA2+.
Basicità di che tipo: di Lewis o Bronsted? Lewis, perché la specie positiva è in grado di accettare elettroni. Questi elettroni sono donati, ad esempio, da atomi di ossigeno di molecole d'acqua.
Il solido assorbe l'umidità al grado di dissoluzione nella stessa acqua che bagna i suoi cristalli. Questa proprietà è conosciuta come DelicueScencia.
La sua densità è 2,15 g/ml. Mentre incorpora l'acqua nella sua struttura, il cristallo viene "dilatato", aumentando il suo volume e, di conseguenza, diminuendo la densità. Solo il CACL2· H2O Break con questa tendenza, mostrando una maggiore densità (2,24 g/mL).
Il peso molecolare del sale anidrid è di circa 111 g/mol e per ogni molecola d'acqua nella sua struttura questo peso aumenta 18 unità.
Solubilità
Il cacl2 È molto solubile in acqua e in alcuni solventi polari, come etanolo, acido acetico, metanolo e altri alcoli.
Calore calore
Quando il processo viene sciolto in acqua, è esotermico e, quindi, riscalda la soluzione e l'ambiente circostante.
Può servirti: da dove viene la plastica? Storia e tipiQuesto perché il complesso acquoso stabilizza meglio gli ioni CA2+ in soluzione che le interazioni elettrostatiche con ioni cl-. Poiché il prodotto è più stabile, il solido rilascia energia sotto forma di calore.
Decomposizione elettrolitica
Il cacl2 Il fuso può essere sottoposto a elettrolisi, processo fisico che consiste nella separazione di un composto nei suoi elementi dall'azione di una corrente elettrica. Nel caso di questo sale, i prodotti sono calcio metallico e cloro gassoso:
Cacl2(l) → Ca (s) + CL2(G)
Gli ioni ca2+ Sono ridotti nel catodo, mentre ioni cl- Sono ossidati all'anodo.
Riferimenti
- Wikipedia. (2018). Cloruro di calcio. Recuperato da.Wikipedia.org
- SHIVER & ATKINS. (2008). Chimica inorganica. Negli elementi del gruppo 2. (Quarta edizione., P. 278). Mc Graw Hill.
- PUBCHEM. (2018). Cloruro di calcio. Recuperato da Pubchem.NCBI.Nlm.NIH.Gov.
- Oxychem. Cloruro di calcio: una guida alle proprietà fisiche. Oxy recuperato.com
- Carole Ann. Usi comuni di cloruro di calcio. Hunker si è ripreso.com