Caratteristiche, sviluppo e funzione del citotrofoblasti
- 4879
- 1114
- Zelida Gatti
Lui citotrofoblasto O Langhani cellule, è la porzione della membrana basale del trofoblasto composto da cellule mononucleate. Questa porzione corrisponde alla popolazione di cellule staminali, da cui derivano gli altri trofoblasti.
Questo strato cellulare dal punto di vista mitotico è molto attivo, producendo cellule che si legano al sincitiotrofoblasto. Il citotrofoblasto ha origine nel periodo di impianto della blastocisti nello sviluppo embrionale dei mammiferi. Durante questa fase di sviluppo, le cellule trofoblastiche proliferano lasciando il posto all'invasione nell'epitelio endometriale.
 Fonte: Henry Vandyke Carter [dominio pubblico]
Fonte: Henry Vandyke Carter [dominio pubblico] [TOC]
Caratteristiche
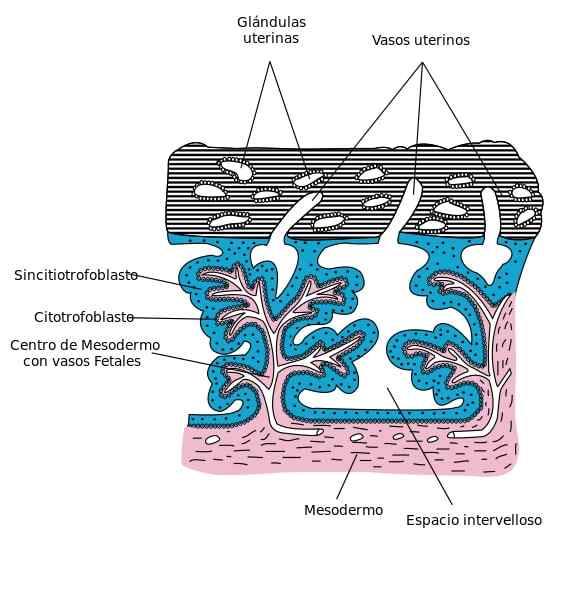
Uno strato di cellule mononucleate costituisce il citotrofoblasto, sul lato interno del trofoblasto. Queste cellule si trovano nei villi corionici e sono coperte dal sincitiotrofoblasto. Il citotrofoblasto è caratterizzato da un'elevata differenziazione cellulare e capacità di proliferazione e bassa attività funzionale.
Durante la fase o la finestra dell'impianto dell'embrione, le cellule di citotrofoblasti hanno origine, diventando cubica e pallida con una buona immagine nucleare e ben differenziate l'una dall'altra.
La proliferazione delle cellule citotrofoblastiche si verifica mediante moltiplicazione delle cellule continue. Si stima che almeno la metà delle cellule in questo strato stia eseguendo il ciclo cellulare. Oltre alla proliferazione, esiste un'elevata differenziazione cellulare che genera la laica di sincitiotrofoblasto.
Citofoblasto extravelllositario
Il citofoblasto estraying si trova esternamente su villi corionici. Questo strato cellulare prolifera rapidamente invasore lo stroma uterino e le arterie a spirale dell'endometrio, riducendo la resistenza delle pareti vascolari. Sono differenziati due tipi di citofoblasti extravelllosir esserici: l'interstiziale e l'endovascolare.
Nell'interstiziale, le cellule invadono il miometrio per fondersi e diventare grandi cellule placentali. Queste cellule non invadono le pareti vascolari.
Può servirti: PachyneL'endovascolare d'altra parte, invade le pareti vascolari che distruggono le cellule lisce dello strato medio del vaso sanguigno, con un materiale fibrinoide invece. La diffusione di molecole che simulano un fenotipo endoteliale consente di sostituire l'endotelio dei vasi sanguigni materni con una nuova superficie interna.
L'attività del citotrofoblasto è regolata da fattori genetici, di trascrizione, crescita, ormonale e chimica (come la concentrazione di ossigeno molecolare).
Sviluppo e funzione
Nei mammiferi, dopo la fecondazione dell'ovule da parte di uno sperma, vengono eseguite una serie di divisioni cellulari fino a quando non si forma la blastocisti, che è una sfera cellulare vuota in cui lo strato cellulare periferico dà origine al trofoblasto, mentre il cluster ha origine i tessuti dell'embrione, chiamando l'embriblasto.
La blastocisti è fissata all'endometrio durante l'implementazione. Le cellule trofoblastiche iniziano a diffondersi quando entrano in contatto con l'endometrio, differenziando così il citotrofoblasto e il sincitotrofoblasto.
Nella specie umana l'implementazione si verifica approssimativamente al sesto giorno dopo l'ovulazione e la fecondazione di ovule.
In alcuni mammiferi, questa fase viene posticipata per giorni, settimane o addirittura mesi, al fine di evitare l'arrivo di una nuova razza in un momento non beneficale, come nei periodi in cui le risorse diminuiscono o mentre la madre allatta un altro allevamento.
In animali come orsi, testamenti, foche e cammelli si verifica un ritardo della finestra di impianto noto come diapausa embrionale.
La blastocisti rimane in quello stato, senza proliferazione di cellule citotrofoblastiche, mediante azione ormonale. Questo meccanismo è innescato in risposta a fattori ambientali o all'allattamento al seno prolungato nella madre.
Può servirti: cosa sono i cromoplasti?Formazione di placenta
La placenta è responsabile di mantenere il feto in sviluppo e deriva da corion (porzione fetale) e deciduo basale. In esso si verificano, si verificano scambi di gas e metaboliti tra circolazioni materne e fetali. Questo organo si sviluppa quando origina da villi differenziabili.
Quando le cellule del citotrofoblasto e con lo sviluppo del mesentere corionico e dei vasi sanguigni si stanno formando, si formano villi corionici primari, secondari e terziari.
Il citotrofoblasto prolifera rapidamente, passando le sue cellule a lagune nel sangue all'interno del sincitiotrofoblasto, formando villi corionici primari.
Successivamente, questi villi sono invasi dal mesenchima embrionale del corione che rimane all'interno e circondato dal citotrofoblasto, per formare i villi secondari che copre il sacco corionico.
I villi terziari sono formati con la comparsa di vasi sanguigni all'interno del mesenchima dei villi secondari.
Mentre i villi terziari, i fili o le cellule cupcaked del citotrofoblasto sono formati all'esterno attraverso il sincitioTroplasto.
In questo modo, vari agglomerati cellulari vanno all'estero e si uniscono, coprendo il sincitiotrofoblasto con una copertura citotrofoblastica. Questa copertura viene interrotta dove i vasi sanguigni materni vanno negli spazi inter-velllositari.
Interfaccia materna-fetale
La prima fase dell'interfaccia materna-fetale è costituita dall'invasione del citofoblasto extravelllositario (situato al di fuori dei villi della placenta) nelle arterie a spirale uterina, conferendo a queste arterie le caratteristiche di essere di alto livello e avere una bassa resistenza al flusso. In questo modo viene mantenuta la perfusione adeguata per la crescita fetale.
Nella seconda fase, le cellule di citotrofoblasti si combinano, annullando le loro membrane cellulari, per dare origine allo strato multinucleato del sincitiotrofoblasto. Quest'ultimo avvolge i villi differenziati della placenta.
Può servirti: epar will solfato: funzioni, sintesi, relazione con malattieIl corretto sviluppo di queste due fasi dell'interfaccia, garantisce la placentazione corretta e quindi uno sviluppo fetale di successo e un progresso sicuro dello stato di gravità.
La barriera placentare separa il sangue materno e fetale
Una barriera placentare, essenzialmente formata dagli strati del tessuto fetale, è responsabile della separazione del sangue dal feto del sangue materno. Nell'uomo, dal quarto mese di sviluppo, questa barriera diventa molto sottile, facilitando il trasferimento di prodotti attraverso di essa.
La degenerazione del guscio o della copertura citotrofoblastica è la causa della perdita di peso della barriera placentare, nel cui stato degenerato è composto da sincitiotrofoplasto, citotrofofoblastica di copertura discontinua di tro -trofoblasto, foglio di velusity mesenchima Capillari placentare Fetale dei villi terziari.
La barriera placentare, oltre a separare il sangue dalla madre e dal sangue fetale, è responsabile dello scambio di ossigeno e dell'anidride carbonica e dei metaboliti tra circolazioni materne e fetali.
Riferimenti
- Hernández-Valencial, m., Valencia-Ortega, J., Ríos-Castillo, b., Cruz-Cruz, p. D. R., & Vélez-Sánchez, D. (2014). Elementi di impianto e placenta: aspetti clinici e melecolari. Rivista di medicina di riproduzione messicana, 6 (2), 102-16.
- Hill, r. W., Wyse, g. A., Anderson, m., & Anderson, M. (2004). Animale di fisiologia (Vol. 2). Sunderland, MA: Sinauer Associates.
- Kardong, k. V. (1995). Vertebrati: anatomia comparativa, funzione, evoluzione. Ed. McGraw Hill.
- Rodríguez, m., Couve, c., Egaña, g., & Chamy, V. (2011). Apoptosi placentare: meccanismi molecolari nella genesi della precslampsia. Rivista per ostetricia cilena e ginecologia, 76 (6), 431-438.
- Ross, m. H., & Pawlina, W. (2007). Istologia. Ed. Pan -American Medical.
- Welsch, u., & Sobotta, J. (2008). Istologia. Ed. Pan -American Medical.
- « Caratteristiche di sincitiotrofoplasti, funzione, apoptosi placentare
- Caratteristiche dei basofili, morfologia, funzioni, malattie »

