Struttura dell'acido maleico, proprietà, ottenimento, usi
- 3674
- 1183
- Ruth Cattaneo
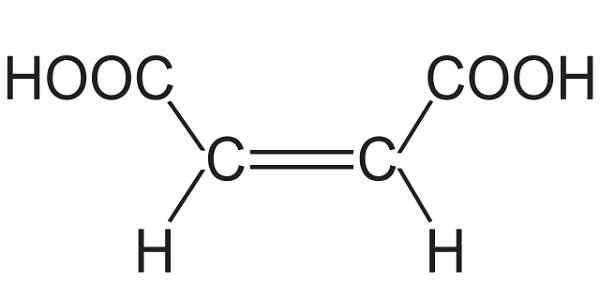
Lui Acido maleico È un composto organico acido la cui formula chimica è hooc-ch = ch-cooh. È un acido dicarbossilico. È anche noto come acido Cis-Acido butenodioico, caleinico, acido malnico e acido tossil.
L'acido maleico si trova naturalmente in tabacco, ginseng e bevande come birra e vino. Si trova anche nel fumo di sigaretta e nei gas di fuga delle auto.
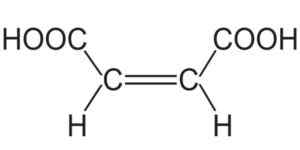 Acido maleico. Ninomia [dominio pubblico]. Fonte: Wikipedia Commons.
Acido maleico. Ninomia [dominio pubblico]. Fonte: Wikipedia Commons. Il suo doppio legame e i due gruppi: lo rendono suscettibile a diverse reazioni chimiche, quindi serve a sintetizzare molti altri composti, materiali e prodotti.
È anche molto utile per l'elaborazione tessile come cotone, lana e seta. Ti consente di ottenere colla, resine e oli sintetici. È usato per evitare l'ossidazione di grassi e oli. A loro volta, molti dei suoi derivati sono utilizzati nelle applicazioni mediche e veterinarie.
Secondo alcune indagini, è uno dei componenti delle bevande fermentate che stimola la secrezione di acido gastrico.
[TOC]
Struttura
La molecola di acido maleico è formata da uno scheletro di 4 atomi di carbonio, di cui i due delle estremità formano gruppi carbossilici -cooh e i due centrali formano un doppio legame c = c = c.
I gruppi -cooh si trovano in posizione Cis Per quanto riguarda il doppio legame. L'ossigeno e gli idrogeni del -cooh sono ospitati in modo che un idrogeno si trovi tra ossigeno.
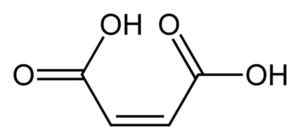 Struttura dell'acido maleico. Benjah-BMM27 [dominio pubblico]. Fonte: Wikipedia Commons.
Struttura dell'acido maleico. Benjah-BMM27 [dominio pubblico]. Fonte: Wikipedia Commons. Nomenclatura
- Acido maleico
- Acido Cis-Butenodioico
- Acido tossilico
- Acido maleinico
- Acido mallenico
Proprietà
Stato fisico
Solido cristallino incolore, cristalli monoclinici.
 Cristalli di acido maleico. Lhchem [CC BY-SA 3.0 (https: // creativeCommons.Org/licenze/by-sa/3.0)]. Fonte: Wikipedia Commons.
Cristalli di acido maleico. Lhchem [CC BY-SA 3.0 (https: // creativeCommons.Org/licenze/by-sa/3.0)]. Fonte: Wikipedia Commons. Peso molecolare
116,07 g/mol
Punto di fusione
130,5 ºC
Punto di ebollizione
135 ºC (decomposti)
Peso specifico
1.609
Solubilità
Molto solubile in acqua: 79 g/100 g H2O 20 ºC
Costanti di dissociazione
K1 = 1000 x 10-5
K2 = 0,055 x 10-5
Proprietà chimiche
L'acido maleico presenta due gruppi -coh e un doppio legame C = C centrale come siti reattivi.
La sua anidrid è una molecola ciclica di 5 atomi, i cui prodotti sono instabili verso l'idrolisi, in particolare i prodotti di reazione con gruppi amino -NH2.
Può servirti: allotropi di carbonioQuesto lo rende come gruppi reversibili di gruppi -nh2 per mascherarli temporaneamente e impedire loro di reagire quando vengono fatte altre reazioni.
Ciò è utile per molteplici scopi, in particolare per modificare le proteine a livello di laboratorio.
Ottenimento
Industrialmente ottenuto dall'ossidazione catalitica del benzene in presenza di vanadio pentossido.
Anche per l'ossidazione della fase del vapore N-butano o n-butilenico con aria, in presenza di un catalizzatore solido.
Può anche essere ottenuto dall'idrolisi dell'anidride malleica.
Si ottiene anche come sottoprodotto durante la produzione di anidride ftalica a partire dal naftalene.
Usi dell'acido maleico
Nella produzione di altri composti chimici
L'acido maleico consente molti altri composti chimici. È usato nella sintesi di acido aspartico, malico, tartarico, succinico, lattico, malonico, propionico e acrilico.
Come intermediario chimico, l'acido maleico trova l'uso in quasi tutti i campi della chimica industriale.
In diverse applicazioni
L'acido maleico consente di ottenere colla sintetica, coloranti, resine alquidiche e oli sintetici.
I suoi derivati sali di malato sono usati nelle formulazioni antistaminiche e farmaci simili.
È usato come conservante in grassi e oli perché serve a ritardare la comparsa di rancidità.
È usato negli inibitori della corrosione e nei prodotti anti-care. Funziona anche come agente per regolare il pH.
Nel settore tessile
È usato nella lavorazione della lana, seta e cotone.
L'ottenimento di oligomeri (polimeri di poche unità) dell'acido maleico è stato studiato per essere utilizzato come agente di finitura per ottenere cotone permanente in stirpe, in modo da non usare polimeri di formaldeide.
In questo caso, la polimerizzazione dell'acido maleico viene eseguita in mezzo acquoso in presenza di NAH2Po2 e un iniziatore radicale come Na2S2O8. L'oligomero dell'acido maleico ha gruppi carbossilici -Cooh uniti al -ch2- adiacente al tuo scheletro molecolare.
Si applica al tessuto di cotone come agente di formazione della griglia e viene eseguito il processo di cura.
In questo modo l'oligomero dell'acido maleico è efficace nell'attraversare la cellulosa di cotone e impartire alti livelli di resistenza alle rughe ai tessuti di cotone.
Inoltre, i tessuti trattati con polimeri di acido maleico non hanno mostrato giallo e hanno mostrato una maggiore ritenzione di resistenza o resistenza rispetto ai trattati con polimeri di formaldeide.
Può servirti: vetro pyrex Autore: Steve Buissinne. Fonte: Pixabay.
Autore: Steve Buissinne. Fonte: Pixabay. In medicina
Esistono diversi composti basati sull'acido maleico che vengono utilizzati nel trattamento del cancro.
Sunitinib (Sutent) Hex è un farmaco anti -cancro che agisce in diversi modi per inibire la proliferazione delle cellule tumorali e dell'angiogenesi.
È approvato per il trattamento del carcinoma a cellule renali e il tumore gastrointestinale resistente ad altri farmaci. La sua attività è studiata nel carcinoma epatecellulare e nel cancro delle cellule polmonari. È fornito per via orale in capsule.
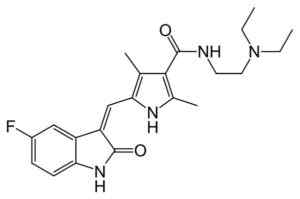 Molecola sunitinib. Fvasconcellos (talk · contribus) [dominio pubblico]. Fonte: Wikipedia Commons.
Molecola sunitinib. Fvasconcellos (talk · contribus) [dominio pubblico]. Fonte: Wikipedia Commons. Secondo uno studio condotto nel 2015, le nanoparticelle sono state preparate con un copolimero acido di picco che si è unito al collegamento di tipo estere dal farmaco paclitaxel usato per il trattamento del cancro per il trattamento del cancro.
Queste nanoparticelle hanno mostrato una maggiore ritenzione nel plasma e nel tumore, inibendo la crescita di quest'ultimo con il miglioramento dell'effetto dell'apoptosi (morte) delle cellule tumorali.
Non hanno mostrato tossicità negli organi principali, nei tessuti e nel sistema ematologico.
Per questi motivi sono proposti come sistema alternativo di distribuzione o rilascio del farmaco nei tumori solidi
In odontoiatria
Secondo alcune indagini, l'acido maleico del 10% riduce la perdita minerale dei denti quando applicato nei trattamenti dentali.
Viene usato per erodere delicatamente la superficie dentale e quindi favorire l'adesione di altri materiali.
È riferito che può produrre pari forze dell'Unione o dell'adesione che con il 37% di acido ortofosfato.
Nella medicina veterinaria
Il malleato accettivo è usato come tranquillante in medicina veterinaria per la sedazione degli animali prima dell'anestesia. Questo composto protegge dagli effetti delle aritmie dell'anestesia.
 Autore: Arvydas Lakacouskas. Fonte: Pixabay.
Autore: Arvydas Lakacouskas. Fonte: Pixabay. Potenziale uso come disinfettante
È stato trovato di recente (2018) che l'acido maleico può inibire la resistenza al batterio Listeria monocytogenes ad acidi che lo rendono suscettibile all'azione di questi se usati per disinfettare nelle industrie alimentari.
Si ritiene che agisca su un enzima che favorisce la resistenza di questi microrganismi agli acidi, disattivandolo. È stato anche osservato che l'acido maleico elimina i batteri della bici.
Può servirti: regola degli ottettiQueste caratteristiche sono fatte da un potenziale candidato per la disinfezione dei team nel settore alimentare.
Effetti dell'acido di salute contenuti in bevande fermentate come birra e vino
Studi condotti con esseri umani che ingerivano soluzioni di glucosio fermentato hanno scoperto che gli acidi dicarbossilici come l'acido maleico sono potenti acido gastrico stimolanti.
Secondo i ricercatori, è molto probabile che ciò si verifichi nel caso di bevande fermentate come birra, champagne e vino, ma non in bevande alcoliche distillate come whisky e cognac.
Questo perché l'effetto stimolante dell'acido gastrico è causato da acidi dicarbossilici come l'acido maleico e non dall'alcool (etanolo).
Rischi
Il contatto dell'acido sanitario con gli occhi o la pelle provoca irritazione e può causare dermatite da contatto prolungata. La sua inalazione produce irritazione al naso e alla gola. Può esercitare un effetto dannoso sui reni.
Se esposto al calore o alla fiamma, si verifica la sua combustione e i gas o i fumi prodotti causano irritazione.
Se l'acido maleico viene rilasciato, l'ambiente dovrebbe essere frazionario o decomposto dai microrganismi. Non si accumula negli organismi acquatici.
Riferimenti
- O.S. Biblioteca nazionale di medicina. (2019). Acido maleico. Recuperato da: pubchem.NCBI.Nlm.NIH.Gov.
- Hermanson, g.T. (2013). Target funzionali per la bioconjugation. In Bioconiugate Techniques (terza edizione). Recuperato da ScienceDirect.com.
- Teyssen, s. et al. (1999). L'acido maleico e l'acido succinico nelle bevande di alcol fermentato sono gli stimolanti della secrezione di acido gastrico. J. Clin. Investire. 1999; 103 (5): 707-713. Recuperato da JCI.org.
- Flecknell, p. et al. (2015). Pre -sthesia, anestesia, analgesia ed eutanasia. In laboratorio di medicina animale (terza edizione). Recuperato da ScienceDirect.com.
- Chen, d. et al. (2005). Polimerizzazione acquatica di acido maleico e reticolazione di cellulos di cotone. Ind. Eng. Chimica. Manzo. 2005, 44, 7921-7927. Recuperato dai pub.sindrome coronarica acuta.org.
- Carver, J.R. (2011). Gestione degli effetti collaterali cardiaci e polmonari correlati al trattamento. In oncologia di supporto. Recuperato da ScienceDirect.com.
- Serdarüsümez, Nejaterverdi. (2010). Adesivi e legame in ortodonzia. In attuale terapia in ortodonzia. Recuperato da ScienceDirect.com.
- Dalela, m. et al. (2015). Nanoparticelle biocompatibili a pH di poli (acido stirene-co-malato) sensibili al paclitaxel per la consegna di antitumo. Interfacce ACS Appl Mater. 9 dicembre 2015; 7 (48): 26530-48. NCBI recuperato.Nlm.NIH.Gov.
- Paudyal, r. et al. (2018). Un nuovo approccio nella disinfezione acida attraverso l'inibizione di meccanismi resistenti agli acidi; L'inibizione mediata dall'acido maleico dell'attività della decarbossilasi del glutammato migliora la sensibilità acida di Listeria monocytogenes. Cibo mycrobiol. 2018 febbraio. 69: 96-104. NCBI recuperato.Nlm.NIH.Gov.
- « Caratteristiche, elementi ed esempi del paesaggio urbano
- Magnetizzazione Orbitale e Spin Magnetic Moment, Esempi »

