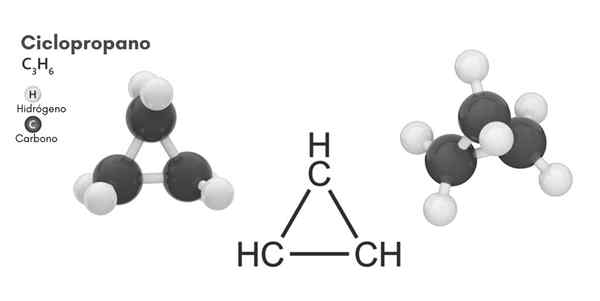
Cycopropan (C3H6)
- 3930
- 638
- Benedetta Rinaldi
Cos'è il ciclopropano?
Lui Ciclismo È una molecola ciclica che ha la formula molecolare C3H6, e questo consiste in tre atomi di carbonio uniti insieme sotto forma di un anello. In chimica c'è una famiglia di idrocarburi saturi che hanno uno scheletro formato da atomi di carbonio uniti da semplici legami ad anello.
Questa famiglia è costituita da un numero vario di molecole (che differiscono per la lunghezza della sua catena gassata principale) e sono note per avere punti di fusione e ebollizione più rapidi rispetto a quelli delle catene alte, oltre a una maggiore reattività di questi.
Cycropoto fu scoperto nel 1881 da un chimico austriaco chiamato August Freund, che era determinato a sapere quale fosse l'elemento tossico in etilene e che venne a pensare che fosse lo stesso ciclopropano.
Anche così, non è stato fino agli anni '30 che ha iniziato a essere prodotto a livello industriale, quando hanno scoperto i loro usi come anestesia, perché prima di quel momento non erano un'attrazione commerciale.
Struttura chimica
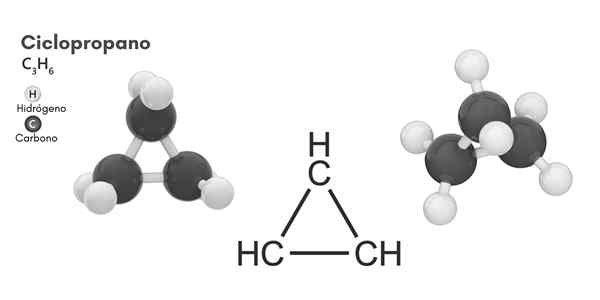
 Struttura molecolare del ciclopropano
Struttura molecolare del ciclopropano Formula ciclistica, molecolare C3H6, È costituito da tre piccoli atomi di carbonio che si legano in una configurazione in modo tale che si forma un anello, lasciando una simmetria molecolare di d3h In ogni carbonio della catena.
La struttura di questa molecola richiede che gli angoli di collegamento che si formano da circa 60º, molto meno di quelli di 109,5º che sono osservati tra gli ibridi SP atomi3, che è un angolo più stabile termodinamicamente.
Ciò porta all'anello che soffre di una tensione strutturale più significativa rispetto ad altre strutture di questo tipo, oltre a una tensione torsionale naturale che ha dalla conformazione eclissata dei suoi atomi di idrogeno.
Può servirti: cinetica enzimaticaPer lo stesso motivo, i legami che si formano tra atomi di carbonio in questa molecola sono considerevolmente più deboli rispetto agli alcani comuni.
In un modo peculiare e diverso da altri collegamenti in cui la vicinanza tra due molecole simboleggia una maggiore energia di collegamento, i legami tra i carboni di questa molecola hanno la peculiarità di avere una lunghezza inferiore agli altri alcani (a causa della loro geometria) e allo stesso modo tempo sono più deboli dei sindacati tra quelli.
Inoltre, il ciclopropano.
Proprietà cicloni
Punto di ebollizione
Rispetto all'altro cicloalcano più comuni, il ciclopropano.
D'altra parte, rispetto al propano lineare, il ciclopropano.
Punto di fusione
Il punto di fusione del ciclopropano è inferiore a quello degli altri cicloalcani, sciogliendosi a una temperatura di 128 ºC in meno di zero. Anche così, non è l'unico cicloalcano che si scioglie a una temperatura inferiore a zero, essendo in grado di osservare questo fenomeno anche nel ciclobutano, nel ciclopentano e nel cicloeptano.
Quindi, nel caso del propano lineare, si scioglie a una temperatura inferiore a 187 ºC sotto lo zero.
Densità
Il cycropopano ha la più alta densità tra i cicloalcani, essendo più di due volte al ciclo comune più denso (1.879 g/L per ciclopropano, superando il ciclodecano con 0,871).
Può servirti: ossido di alluminio: struttura, proprietà, usi, nomenclaturaC'è anche una densità più elevata nel ciclopropano che nel propano lineare. La differenza nei punti di ebollizione e di fusione tra alcani lineari e cicloalcani è dovuta alle maggiori forze di Londra, che aumentano a causa della forma ad anello che consente di essere maggiore area di contatto tra gli atomi interni.
Reattività
La reattività del ciclopropano.
Grazie a ciò, il ciclopropano può essere separato più facilmente e può comportarsi come Alqueno in alcune reazioni. In effetti, l'estrema reattività delle miscele ciclopropane-ossigeno può diventare un pericolo di esplosione.
Usi/applicazioni
L'uso commerciale di ciclopropano per eccellenza è come agente anestetico, studiando questa proprietà per la prima volta nel 1929.
Cyclo -Wown è un potente agente anestetico di rapida azione, che non irrita il tratto respiratorio o presenta un cattivo odore. È stato usato per diversi decenni insieme all'ossigeno ai pazienti con sonno durante gli interventi chirurgici, ma hanno iniziato ad essere osservati effetti collaterali indesiderati come "shock ciclopropano".
Insieme ai costi dei costi e dell'alta infiammabilità, stava attraversando un processo di scarto e sostitutivo da parte di altri agenti anestetici più sicuri.
Sebbene abbia continuato a far parte dei composti utilizzati nell'induzione dell'anestesia, oggi non fa parte degli agenti utilizzati nelle applicazioni mediche.
Rischi
- Il ciclopropano è un gas altamente infiammabile, che produce gas tossici quando viene a contatto con una fiamma. Inoltre, può reagire con agenti ossidanti come perossidi, perossidi, permanganati, nitrati e alogeni, causando incendi e/o esplosioni.
Può servirti: acido clorogenico- Il ciclismo ad alti livelli può causare mal di testa, vertigini, nausea, perdita di coordinamento, sensazione di svenimento e/o sbiadimento.
- Può anche generare irregolarità nella frequenza cardiaca o nell'aritmia, difficoltà respiratorie, coma e persino morte.
- Il ciclopropa liquefatto può causare congelamento della pelle a causa della sua temperatura considerevolmente inferiore a zero.
- Essendo un gas in condizioni ambientali, questo composto può facilmente entrare nel corpo attraverso l'aria e diminuisce anche il livello di ossigeno nell'aria.