Ciclo (C5H10) Struttura, proprietà e usi
- 1270
- 25
- Zelida Gatti
Lui Ciclopentano Questo è idrocarburo ciclico, in particolare un cicloalcano. A sua volta, è un composto organico la cui formula molecolare è C5H10. Può essere visualizzato come versione chiusa del N-Pentano, catena aperta, in cui le sue estremità si sono unite per la perdita di due atomi di idrogeno.
Nell'immagine inferiore è mostrato lo scheletro del ciclopentano. Nota come si indossa il geometrico lo scheletro, formando un anello pentagonale. Tuttavia, la sua struttura molecolare non è piatta, ma presenta pieghe che cercano di stabilizzare e ridurre la tensione all'interno dell'anello. Il ciclismo è un liquido altamente volatile e infiammabile, ma non tanto quanto il N-Pentano.
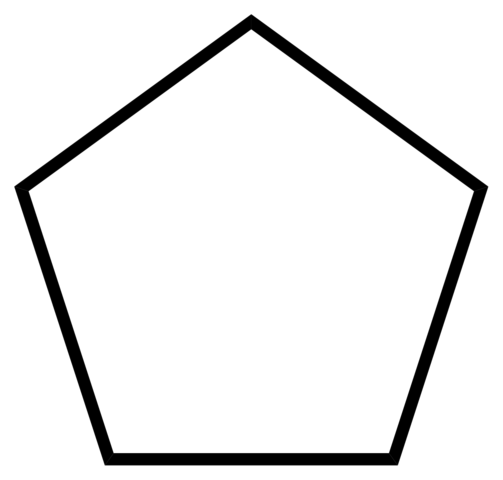 Scheletro di carbonio del ciclopentano. Fonte: Ccroberts [dominio pubblico]
Scheletro di carbonio del ciclopentano. Fonte: Ccroberts [dominio pubblico] A causa della sua capacità di solvente, il ciclopentano è uno dei solventi più utilizzati nelle industrie chimiche. Non sorprende che molti prodotti di forte odore lo contengano tra la loro composizione, quindi essendo infiammabili. Viene anche usato come agente di espansione per schiume poliuretaniche utilizzate nei frigoriferi.
[TOC]
Struttura Ciclipentano
Interazioni intermolecolari
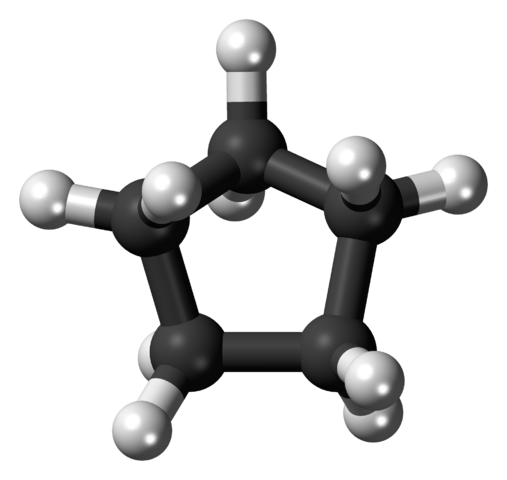
 Struttura molecolare del ciclopentano rappresentato da un modello di sfere e barre. Fonte: Jynto [CC0]
Struttura molecolare del ciclopentano rappresentato da un modello di sfere e barre. Fonte: Jynto [CC0] Nella prima immagine è stato mostrato lo scheletro del ciclopentano. Adesso vediamo che è più di un semplice Pentagono: ai suoi bordi, gli atomi di idrogeno (sfere bianche) si distinguono, mentre gli atomi di carbonio costituiscono l'anello pentagonale (sfere nere).
Avendo solo legami C-C e C, il suo momento di dipolo è insignificante, quindi le molecole di ciclopentano non possono interagire tra loro attraverso le forze dipolo-dipolo. Invece, rimangono coesi grazie alle forze dispersive di Londra, con gli anelli che cercano di impilarne uno sopra l'altro.
Questo stack offre una determinata area di contatto rispetto alle molecole lineari di N-Pentano. Di conseguenza, il ciclopentano ha un punto di ebollizione più grande del N-Pentano, oltre a una pressione a vapore inferiore.
Può servirti: 7 pratiche di laboratorio di chimica (semplice)Le forze dispersive sono responsabili del ciclopentano forma un cristallo molecolare quando si congelano a -94 ºC. Sebbene non ci siano molte informazioni sulla sua struttura cristallina, questa è polimorfica e ha tre fasi: I, II e III, essendo la fase II una miscela disordinata di I e III.
Conformazione e tensione anularia
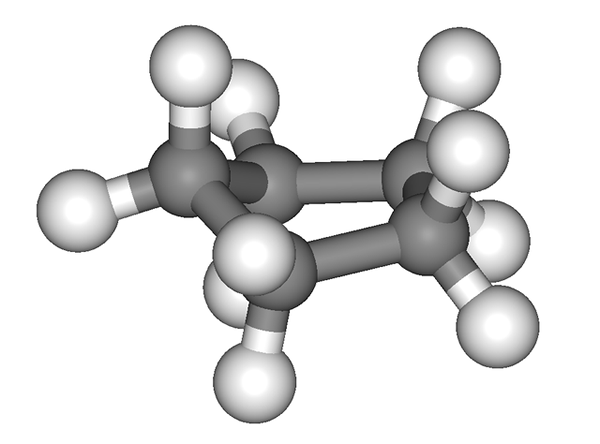 L'anello Ciclopentano non è totalmente piatto. Fonte: Edgar181 [dominio pubblico]
L'anello Ciclopentano non è totalmente piatto. Fonte: Edgar181 [dominio pubblico] L'immagine precedente dà la falsa impressione che il ciclo sia piatto; Ma non è così. Tutti i loro atomi di carbonio hanno ibridazione SP3, Quindi i loro orbitali non si trovano nello stesso piano. Allo stesso modo, come se ciò non bastasse, gli atomi di idrogeno sono molto vicini l'uno all'altro, respingendo fortemente quando vengono eclissi.
Pertanto, si parla di conformazioni, una delle quali è la sedia a metà (immagine superiore). Da questo punto di vista, è chiaro che l'anello Ciclopentano presenta pieghe, che aiutano a ridurre i suoi tumori annullati a causa dei loro atomi di carbonio così vicini l'uno all'altro.
Questa tensione è dovuta al fatto che i legami C-C hanno angoli inferiori a 109'5º, il valore ideale per il prodotto ambientale tetraedrico delle loro ibridazioni SP3.
Tuttavia, nonostante questa tensione, il ciclo è un composto più stabile e meno infiammabile del Pentan. Questo può essere verificato confrontando i suoi rombi di sicurezza, in cui l'innesto del ciclo ne ha 3, mentre quella del pentan, 4.
Proprietà Ciclipentano
Aspetto fisico
Liquido incolore con un odore morbido simile all'olio.
Può servirti: fasi di chimicaMassa molare
70,1 g/mol
Punto di fusione
-93,9 ºC
Punto di ebollizione
49,2 ºC
punto d'infiammabilità
-37,2 ºC
Temperatura di autorezione
361 ºC
Calore di vaporizzazione
28,52 kJ/mol a 25 ºC
Sostanza vischiosa
0,413 mpa · s
Indice di rifrazione
1.4065
Pressione del vapore
45 kPa a 20 ° C. Questa pressione corrisponde a circa 440 atm, tuttavia, di quello del N-Pentano: 57.90 kPa.
Qui si manifesta l'effetto della struttura: l'anello ciclopentano consente interazioni intermolecolari più efficaci, che coesive e mantengono le sue molecole più all'interno del liquido rispetto alle molecole lineari delle molecole lineari del N-Pentano. Pertanto, quest'ultimo ha una maggiore pressione del vapore.
Densità
0,751 g/cm3 a 20 ºC. D'altra parte, i suoi vapori sono 2,42 volte più densi dell'aria.
Solubilità
In un litro di acqua a 25 ºC, 156 mg di ciclopentano dissolto, a causa del suo carattere idrofobo. Tuttavia, è miscibile in solventi apolari come altre paraffine, eterici, benzene, tetracloruro di carbonio, acetone ed etanolo.
Coefficiente di partizione ottanolo/acqua
3
Reattività
Il ciclismo è stabile se è archiviato correttamente. Non è una sostanza reattiva perché i suoi collegamenti C-H o C-C non sono facili da rompere, anche quando porterebbe al rilascio di energia causata dalla tensione dell'anello.
In presenza di ossigeno, brucerà in una reazione di combustione, sia completa che incompleta. Poiché il ciclo è un composto molto volatile, deve essere conservato in luoghi in cui non può essere esposto a nessuna fonte di calore.
Nel frattempo, in assenza di ossigeno il ciclopentano subirà una reazione di pirolisi, decomponendo in molecole più piccole e insature. Uno di questi è il 1-pentene, che dimostra che il calore rompe l'anello ciclopentano per originare un alchene.
Può servirti: metil salicilatoD'altra parte, il ciclopentano può reagire con il bromo sotto radiazione ultravioletta. In questo modo, uno dei suoi legami C-H è sostituito da C-Br, che a sua volta può essere sostituito da altri gruppi; E quindi, emergono derivati ciclopentani.
Applicazioni
Solvente industriale
Il carattere idrofobico e apolare del ciclopentano è realizzato con un solvente di laurea, accanto agli altri solventi paraffinici. Per questo motivo, di solito fa parte delle formulazioni di molti prodotti, come colla, resine sintetiche, dipinti, adesivi, tabacco e benzina.
Fonte di etilene
Quando il ciclopentano è soggetto a pirolisi, una delle sostanze più importanti che genera è l'etilene, che ha innumerevoli applicazioni nel mondo dei polimeri.
Schiume isolanti in poliuretano
Uno degli usi più eccezionali di Cycopentano è come agente di espansione per la produzione di schiume isolanti in poliuretano; Cioè, i vapori Ciclopentano, a seguito della loro grande pressione, espandi il materiale polimerico fino a quando non gli danno una schiuma con proprietà benefiche da utilizzare nel telaio di frigoriferi o congelatori.
Alcune aziende hanno scelto di sostituire gli HFC con Ciclopentano nella produzione di materiali isolanti, poiché non contribuisce al deterioramento dello strato di ozono e riduce anche il rilascio di gas serra nell'ambiente.
Riferimenti
- Graham Solomons t.W., Craig b. Frigorifero. (2011). Chimica organica. (10th Edizione.). Wiley Plus.
- Carey f. (2008). Chimica organica. (Sesta edizione). Mc Graw Hill.
- Wikipedia. (2020). Ciclopentano. Recuperato da: in.Wikipedia.org
- Centro nazionale per le informazioni sulla biotecnologia. (2020). Ciclopentano. Database PubChem, CID = 9253. Recuperato da: pubchem.NCBI.Nlm.NIH.Gov
- Elsevier b.V. (2020). Ciclopentano. Scienceirect. Estratto da: ScienceDirect.com
- GE Appliances. (11 gennaio 2011). Riduzione delle emissioni di gas serra presso gli impianti di produzione del frigorifero GE. Recuperato da: sala stampa.Geapplicances.com
- « Processo di emulsione emulsionante, aspetti molecolari, applicazioni
- Città industriale Come è nato, struttura, conseguenze, problemi »

