Struttura, proprietà, sintesi e usi cicloesenici

- 1799
- 381
- Dante Morelli
Lui Cicloesen È un alchene o un'olefina ciclica la cui formula molecolare è C6H10. È costituito da un liquido incolore, insolubile in acqua e miscibile con molti solventi organici. È caratterizzato dall'essere infiammabile e in natura si trova di solito in Hulla Tar.
Il cicloesen è sintetizzato dall'idrogenazione parziale del benzene e dalla disidratazione dell'alcool cicloesanolo; Cioè, un modo più ossidato. Come altri cicloalqueni, sperimenta l'aggiunta elettrofila e i radicali liberi; Ad esempio, reazione di alogenazione.
 Molecola cicloesenica. Fonte: Neurotoger.
Molecola cicloesenica. Fonte: Neurotoger. Questa ciclica (immagine superiore) forma miscele aceotropiche (non separabili per distillazione), con alcoli inferiori e acido acetico. Non è molto stabile nello stoccaggio prolungato, poiché si decompone sotto l'azione della luce solare e delle radiazioni ultraviolette.
Il cicloesen è usato come solvente e quindi ha numerose applicazioni, come: stabilizzatore ad alto contenuto di benzina di ottano ed estrazione di petrolio.
Ma la cosa più importante è che il cicloesice funge da intermediario e materia prima per ottenere numerosi composti di grande utilità, tra cui: cicloesanone, acido adipico, acido maleico, cicloesano, butyne, acido cicloesilcarbossilico, ecc.
[TOC]
Struttura cicloesenica
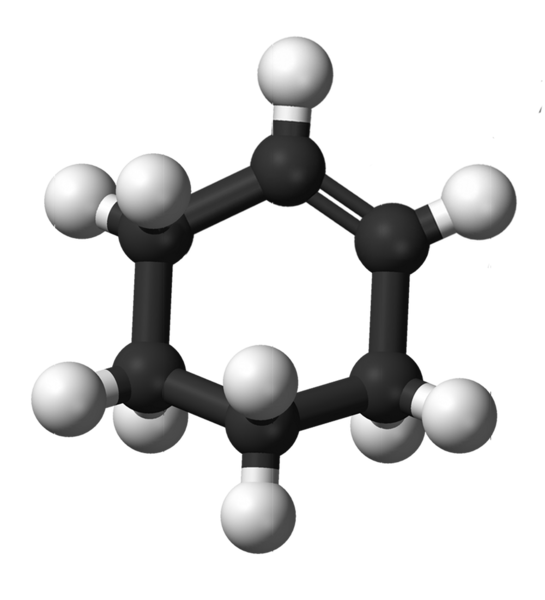 Struttura cicloesenica. Fonte: Kemikungen [dominio pubblico]
Struttura cicloesenica. Fonte: Kemikungen [dominio pubblico] L'immagine superiore mostra la struttura del cicloesen con un modello di sfere e barre. Puoi notare l'anello a sei carbonio e il doppio legame, entrambi insaturazione del composto. Da questa prospettiva, sembra che l'anello sia piatto; Ma non è affatto.
Per iniziare, i carboni a doppio legame hanno ibridazione SP2, che dà loro una geometria trigonale piatta. Pertanto, questi due carboni e quelli adiacenti ad essi si trovano nello stesso piano; Mentre i due carboni all'estremità opposta (al doppio legame), sono al di sopra e sotto detto piano.
Può servirti: gravità specificaL'immagine inferiore illustra perfettamente i nuovi spiegati.
 Vista frontale della struttura cicloesica. Fonte: Ben Mills.
Vista frontale della struttura cicloesica. Fonte: Ben Mills. Si noti che la striscia nera è composta da quattro carboni: i due del doppio legame e gli altri adiacenti ad essi. La prospettiva esposta è quella che sarebbe ottenuta se uno spettatore avesse messo l'occhio proprio di fronte al doppio collegamento. Si può quindi vedere che un carbonio è alto e sotto questo piano.
Poiché la molecola cicloesa non è statica, i due carboni verranno scambiati: uno scenderà mentre l'altro si alzerà sopra il piano. Quindi ci si aspetterebbe che comporti questa molecola.
Interazioni intermolecolari
Il cicloesen è un idrocarburo e, pertanto, le sue interazioni intermolecolari si basano sulle forze di dispersione di Londra.
Questo perché la molecola è apolare, senza dipolo permanente, e il suo peso molecolare è il fattore che la maggior parte contribuisce a mantenerlo coeso nel liquido.
Allo stesso modo, il doppio legame aumenta il grado di interazione, poiché non può muoversi con la stessa flessibilità di quello degli altri carboni, e questo favorisce l'interazione tra le molecole vicine. È per questo motivo che il cicloesen ha un punto di ebollizione leggermente più grande (83 ° C) di quello del cicloesano (81 ° C).
Proprietà
Nomi chimici
Ciclohexen, tetraidribenzene.
Peso molecolare
82.146 g/mol.
Aspetto fisico
Liquido incolore.
Odore
Odore dolce.
Punto di ebollizione
83 ºC a 760 mmHg.
Punto di fusione
-103,5 ºC.
punto di accensione
-7 ºC (tazza chiusa).
Solubilità dell'acqua
Praticamente insolubile (213 mg/L).
Solubilità nei solventi organici
Manibile con etanolo, benzene, tetracloruro di carbonio, etere di petrolio e acetone. Si prevede che sia in grado di dissolvere i composti apolari, come alcuni degli alotropi del carbone.
Può servirti: Torio: struttura, proprietà, ottenimento, usiDensità
0,810 g/cm3 a 20 ° C.
Densità del vapore
2,8 (con relazione aerea presa come uguale a 1).
Pressione del vapore
89 mmHg a 25 ° C.
Auto-direzione
244 ºC.
Decomposizione
Si decompone in presenza di sali di uranio, sotto l'azione della luce solare e delle radiazioni ultraviolette.
Sostanza vischiosa
0,625 mpascal a 25 ° C.
Calore a combustione
3.751,7 kJ/mol a 25 ºC.
Calore di vaporizzazione
30,46 kJ/mol a 25 ºC.
Tensione superficiale
26,26 mn/m.
Polimerizzazione
Può polimerizzare in determinate condizioni.
Soglia di odore
0,6 mg/m3.
Indice di rifrazione
Da 1.4465 a 20 ºC.
ph
7-8 a 20 ° C.
Stabilità
Cyclohexen non è molto stabile durante la conservazione a lungo termine. L'esposizione alla luce e all'aria può causare la produzione di perossidi. È anche incompatibile con forti agenti ossidanti.
Reazioni
-I cicloalques sperimentano principalmente reazioni di addizione, sia elettrofili che radicali liberi.
-Reagisce con il bromo per formare 1.2-dibromocicloesano.
-Si ossida rapidamente in presenza di permanganato di potassio (KMNO4).
-È in grado di produrre un epossido (ossido di cicloesen) in presenza di acido peroxibenzoico.
Sintesi
Il cicloesto è prodotto dalla catalisi acida cicloesanolo:
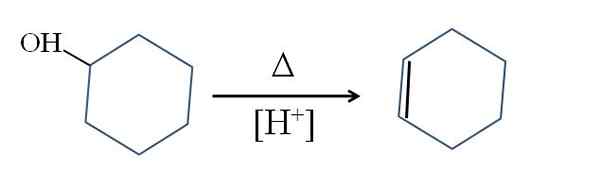 Disidratazione del cicloesanolo. Fonte: Gabriel Bolívar.
Disidratazione del cicloesanolo. Fonte: Gabriel Bolívar. Il simbolo Δ rappresenta il calore necessario per promuovere l'output del gruppo OH come molecola d'acqua in un mezzo acido (-OH2+).
Il cicloesto si verifica anche mediante idrogenazione parziale del benzene; Cioè, due dei suoi doppi legami aggiungono una molecola di idrogeno:
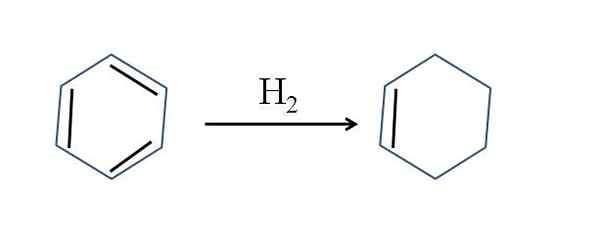 Idrogenazione parziale del benzene. Fonte: Gabriel Bolívar.
Idrogenazione parziale del benzene. Fonte: Gabriel Bolívar. Sebbene la reazione sembri semplice, richiede un grande h2 e catalizzatori.
Applicazioni
-Ha utilità come solvente organico. Inoltre, è una materia prima per la produzione di acido adipico, aldeide adipico, acido maleico, cicloesano e acido cicloesilcarbossilico.
Può servirti: radioattività-Viene utilizzato nella produzione di cloruro cicloesano, composto usato come intermediario della preparazione di prodotti farmaceutici e di sfregamento additivo.
-Il cicloesen è anche usato nella sintesi di cicloesanone, materia prima per la produzione di medicinali, pesticidi, profumi e coloranti.
-Cyclohexen interviene nella sintesi di aminocicloesanolo, un composto che viene usato come tensioattivo ed emulsionante.
-Inoltre, Cyclohexen può essere utilizzato per la preparazione nel laboratorio Butadieno. Quest'ultimo composto viene utilizzato nella produzione di gomma sintetica, nell'elaborazione dei pneumatici per auto, ed è anche utilizzato nell'elaborazione delle materie plastiche acriliche.
-Ciclohexen è materia prima per sintesi di lisina, fenolo, resina di polyciloolefin e additivi in gomma.
-Viene usato come stabilizzatore di benzoline ad alto numero di ottani.
-Interviene nella sintesi di rivestimenti impermeabili, film resistenti alle crepe e cartelle di rilegatura per i rivestimenti.
Rischi
Il cicloesen non è un composto molto tossico, ma può causare un arrossamento della pelle e degli occhi. La sua inalazione può produrre tosse e sonnolenza. Inoltre, la sua ingestione può causare sonnolenza, difficoltà a respirare e nausea.
Il cicloesen è poco assorbito nel tratto gastrointestinale, quindi non sono previsti gravi effetti sistemici a causa della sua ingestione. La massima complicazione è la sua aspirazione per il sistema respiratorio, che può produrre polmonite chimica.
Riferimenti
- Joseph f. Chiang e Simon Harvey Bauer. (1968). Struttura molecolare del cicloesene. J. SONO. Chimica. Soc. 1969, 91, 8, 1898-1901.
- Karry Barnes. (2019). Cicloesene: pericoli, sintesi e struttura. Studio. Recuperato da: studio.com
- Morrison, r. T. E boyd, r. N. (1987). Chimica organica. (5ta Edizione.). Editoriale Addison-Wesley IberoAmericana.
- PUBCHEM. (2019). Cicloesene. Recuperato da: pubchem.NCBI.Nlm.NIH.Gov
- Libro chimico. (2019). Cicloesene. Recuperato da: chimico.com
- Rete di dati tossicologici. (2017). Cicloesene. Txnet. Recuperato da: txnet.Nlm.NIH.Gov
- Chemossi. (S.F.). La formula strutturale per il cicloesene è. Recuperato da: Chemossi.com

