Carbonio anomerico cosa è, caratteristiche, esempi
- 4863
- 809
- Cosetta Messina
Lui Carbonio anomerico È uno stereocentro presente nelle strutture cicliche dei carboidrati (mono o polisaccaridi)). Essere uno stereocentro, più esattamente un epimero, ne deriva due diastereoisomeri, designati con lettere α e β; Questi sono gli anomeri e fanno parte dell'ampia nomenclatura nel mondo degli zuccheri.
Ogni anomero, α o β, differisce nella posizione del gruppo OH del carbonio Anómerico rispetto all'anello; Ma in entrambi, il carbonio anomerico è lo stesso e si trova nello stesso luogo della molecola. Gli anomeri sono emiacetali ciclici, prodotto di una reazione intramolecolare nella catena aperta di zuccheri; essere aldose (aldeide) o ketosas (chetoni).
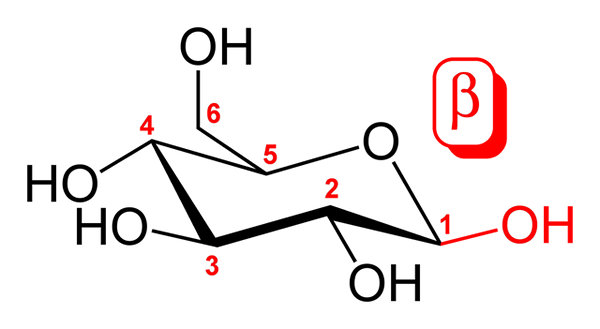
 Conformazione in sedia per β-D-glucopiranosio. Fonte: Commons Wikimedia.
Conformazione in sedia per β-D-glucopiranosio. Fonte: Commons Wikimedia. L'immagine superiore mostra la conformazione della sedia per β-D-glucopiranosio. Come si può vedere, è costituito da un anello di sei membri, incluso un atomo di ossigeno tra i carboni 5 e 1; Quest'ultimo, o meglio, il primo, è il carbonio Anóberico, che forma due semplici legami con due atomi di ossigeno.
Se viene osservato in dettaglio, il gruppo 1 OH Carbon 1 è orientato sopra l'anello esagonale, nonché il gruppo CH2Oh (Carbon 6). Questo è l'anomero β. L'anomero α, d'altra parte, differirebbe solo in questo gruppo OH, che sarebbe situato lungo l'anello, come se fosse un transtereoisomero.
Emiacetali
È necessario approfondire un po 'di più nel concetto di emiaceti per comprendere meglio e distinguere il carbonio anomerico. Gli emiacetali sono il prodotto di una reazione chimica tra un alcol e un aldeide (aldosio) o un chetone (chetosas).
Questa reazione può essere rappresentata con la seguente equazione chimica generale:
Può servirti: polivinilpirrolidone: struttura, proprietà, usi, effetti collateraliRoh + r'cho => roch (oh) r '
Come si può vedere, un alcol reagisce con un'aldeide per formare l'emiacetal. Cosa succederebbe se sia R che R 'appartengono alla stessa catena? In tal caso, ci sarebbe un emiacetal ciclico e l'unico modo possibile in cui si può formare è che entrambi i gruppi funzionali, -oh e -cho, sono presenti nella struttura molecolare.
Inoltre, la struttura deve consistere in una catena flessibile e con collegamenti capaci per facilitare l'attacco nucleofilo di OH verso il carbonio carbonilico del gruppo CHO. Quando ciò accade, la struttura si chiude in un anello di cinque o sei membri.
Emiacetal ciclico
 Formazione emiacetale ciclica. Fonte: Alejandro Porto [CC BY-SA 3.0 (https: // creativeCommons.Org/licenze/by-sa/3.0)]
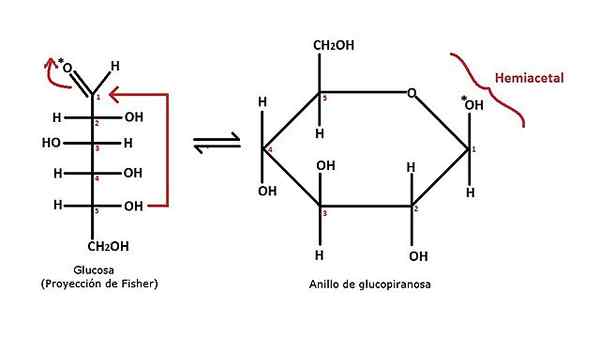
Formazione emiacetale ciclica. Fonte: Alejandro Porto [CC BY-SA 3.0 (https: // creativeCommons.Org/licenze/by-sa/3.0)] Nell'immagine superiore è mostrato un esempio della formazione di un emiacetale ciclico per il monosaccaride di glucosio. Si può vedere che consiste in un aldosa, con un gruppo di aldeide (Carbon 1). Questo è attaccato dal gruppo OH di Carbon 5, come indicato dalla freccia rossa.
La struttura passa dall'essere una catena aperta (glucosio), a un anello pirano (glucopofato). Inizialmente potrebbe esserci alcuna relazione tra questa reazione e la recente spiegazione per l'emiacetal; Ma se l'anello è attentamente osservato, in particolare nella sezione C5-O-c1(Oh) -c2, Sarà apprezzato che ciò corrisponde allo scheletro previsto per un emiacetal.
I carboni 5 e 2 arrivano a rappresentare rispettivamente r e r 'dell'equazione generale. Poiché questi fanno parte della stessa struttura, è allora un emiacetal ciclico (e l'anello è sufficiente per essere evidente).
Caratteristiche del carbonio anomerico e come riconoscerlo
Dov'è il carbonio anomerico? In glucosio, questo è il gruppo CHO, che può subire l'attacco nucleofilo di OH sotto o sopra. A seconda dell'orientamento dell'attacco, si formano due diversi anomeri: α e β, come già accennato.
Può servirti: fenomeni chimici: caratteristiche ed esempiPertanto, una prima caratteristica che questo carbonio possiede è che nella catena di zucchero aperto è quella che subisce l'attacco nucleofilo; Cioè, è il gruppo CHO, per gli aldos o il gruppo R2C = o, per i chetus. Tuttavia, una volta formata l'emiacetal ciclica o l'anello, questo carbonio può dare l'impressione di essere scomparso.
È qui dove ci sono altre caratteristiche più specifiche per individuarlo in qualsiasi piranoso o anello furioso di ogni carboidrato:
-Il carbonio anomerico è sempre a destra o sinistra dell'atomo di ossigeno che forma l'anello.
-Ancora più importante, questo è collegato non solo a questo atomo di ossigeno, ma anche al gruppo OH, da Cho o R2C = O.
-È asimmetrico, cioè ha quattro diversi sostituenti.
Con queste quattro caratteristiche, è facile riconoscere il carbonio anomerico che osserva qualsiasi "struttura dolce".
Esempi
Esempio 1
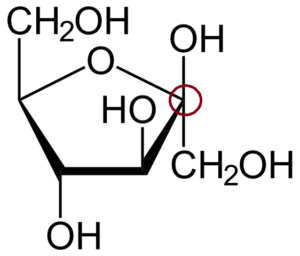 β-D-frucofuranosa. Fonte: Neurotoger (Talk • Contribs) [dominio pubblico]
β-D-frucofuranosa. Fonte: Neurotoger (Talk • Contribs) [dominio pubblico] Su.
Per identificare il carbonio anomerico, devi prima osservare i carboni sul lato sinistro e destro dell'atomo di ossigeno che forma l'anello. Quindi, quello che è legato al gruppo OH è il carbonio anomerico; che in questo caso, è già bloccato in un cerchio rosso.
Questo è l'anomero β perché l'OH del carbonio anomerico è sopra l'anello, proprio come il chip2OH.
Esempio 2
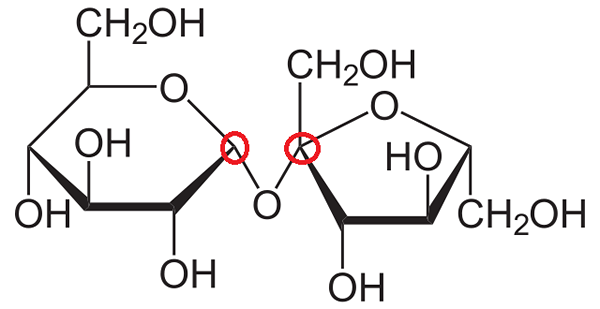 Saccarosio. Fonte: Neurotoger via Wikipedia.
Saccarosio. Fonte: Neurotoger via Wikipedia. Ora, si cerca di spiegare cosa sono i carboni anomerici nella struttura del saccarosio. Come si può vedere, è costituito da due monosaccaridi collegati in modo covalente da un legame glicosidico, -O-.
Può servirti: permanganato di sodio (namno4): proprietà, rischiL'anello destro è esattamente lo stesso recentemente commentato: β-d-frucofuranosa, solo che è "girato" a sinistra. Il carbonio anomerico rimane lo stesso per il caso precedente e soddisfa tutte le caratteristiche che ci si aspetterebbero.
D'altra parte, l'anello a sinistra è α-D-glucopiranose.
Ripetendo la stessa procedura di riconoscimento del carbonio anomerico, guardando i due carboni a sinistra e a destra dell'atomo di ossigeno, si scopre che il carbonio destro è collegato al gruppo OH; che partecipa al legame glucosidico.
Pertanto, entrambi i carboni anomerici sono collegati da -o- ed è per questo che sono bloccati in cerchi rossi.
Esempio 3
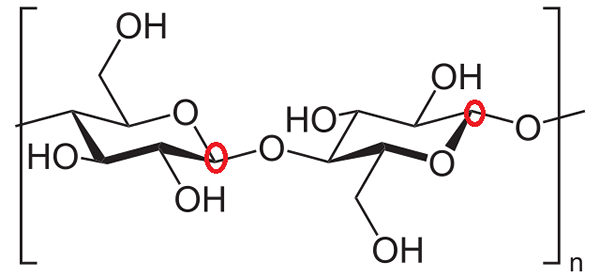 Cellulosa. Fonte: Neurotoger [dominio pubblico]
Cellulosa. Fonte: Neurotoger [dominio pubblico] Infine, si propone di identificare i carboni anomerici di due unità di glucosio nella cellulosa. Ancora una volta, i carboni si osservano attorno all'ossigeno all'interno dell'anello e si scopre che nell'anello di glucosio a sinistra il carbonio anomerico partecipa al legame glucosidico (bloccato nel cerchio rosso).
Nell'anello di glucosio sulla destra, tuttavia, il carbonio anomico è alla destra dell'ossigeno ed è facilmente identificato perché è legato all'ossigeno del legame glucosidico. Pertanto, entrambi i carboni anomerici sono completamente identificati.
Riferimenti
- Morrison, r. T. e Boyd, r, n. (1987). Chimica organica. 5ta Edizione. Editoriale Addison-Wesley Inter-American.
- Carey f. (2008). Chimica organica. (Sesta edizione). Mc Graw Hill.
- Graham Solomons t.W., Craig b. Frigorifero. (2011). Chimica organica. Ammine. (10th Edizione.). Wiley Plus.
- Rendina g. (1974). Tecniche di biochimica applicate. Inter -American, Messico.
- Chang s. (S.F.). Una guida al carbonio anomerico: cos'è un carbonio anomerico? [PDF]. Recuperato da: Chem.Ucla.Edu
- Gunawardena G. (13 marzo 2018). Carbone anomerico. Chimica librettexts. Recuperato da: Chem.Librettexts.org
- Foist l. (2019). Carbonio anomerico: definizione e panoramica. Studio. Recuperato da: studio.com

