Caratteristiche di autofagia, tipi, funzioni, studi
- 4250
- 1112
- Zelida Gatti
IL Autofagia È un sistema di degradazione intracellulare che si verifica in modo conservato nei lisosomi di tutte le cellule eucariotiche (e i vacuoli dei lieviti). La parola è generalmente usata per fare riferimento al degrado dei componenti del citosol o alle "parti" della cella che sono "obsolete" o che hanno smesso di funzionare correttamente.
Il termine autofagia è stato coniato nel 1963 alla Rockefeller University da Duve, che ha anche osservato e descritto i processi di endocitosi cellulare. Letteralmente, la parola autofagia significa "consumare se stessi", sebbene alcuni autori la descrivano come un "cannibalismo auto".
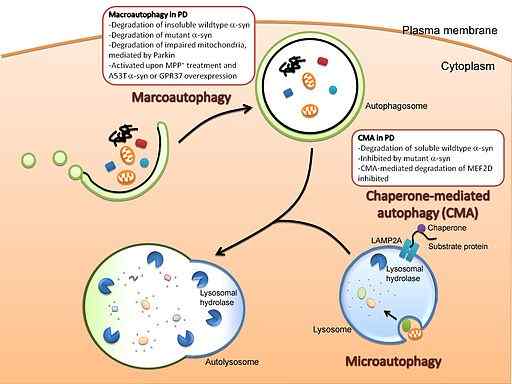
 Rappresentazione grafica di macroautofagi e microanofagia (fonte: Cheung e IP [CC di 3.0 (https: // creativeCommons.Org/licenze/di/3.0)] via Wikimedia Commons)
Rappresentazione grafica di macroautofagi e microanofagia (fonte: Cheung e IP [CC di 3.0 (https: // creativeCommons.Org/licenze/di/3.0)] via Wikimedia Commons) Questo sistema differisce dal degrado mediato dalla degradazione.
Nonostante questa fagocitosi non selettiva, diverse ricerche hanno dimostrato che l'autofagia ha numerose implicazioni fisiologiche e patologiche. Poiché viene attivato durante i periodi di adattamento alla fame, durante lo sviluppo, per l'eliminazione di microrganismi invasori, durante la morte cellulare programmata, per l'eliminazione dei tumori, la presentazione di antigeni, ecc.
[TOC]
Caratteristiche
L'autofagia, come detto, è un processo mediato da un organello citoplasmatico noto come lisosoma.
Il processo di "autofagia" inizia con l'incapsulamento dell'organello che sarà degradato da una doppia membrana, formando un corpo membranoso noto come autofagosoma. La membrana autofagosoma si scioglie, in seguito, con la membrana lisosomiale o con un endosoma tardivo.
Ognuno di questi passaggi tra rapimento, degradazione e liberazione di aminoacidi o altri componenti per gli esercizi di riciclaggio diverse funzioni in diversi contesti cellulari, il che rende l'autofagia un sistema altamente multifunzionale.
L'autofagia è un processo abbastanza controllato, poiché solo i componenti cellulari marcati sono diretti verso questo percorso di degradazione e si verificano la marcatura, in generale, durante i processi di rimodellamento delle cellule.
Ad esempio, quando una cellula epatica stabilisce una risposta di disintossicazione in risposta a farmaci solubili a grasso, il suo reticolo endoplasmatico liscio prolifera considerevolmente e quando lo stimolo generato dal farmaco diminuisce, l'eccesso di reticolo endoplasmatico liscio viene rimosso.
Induzione autofagica
Uno degli eventi che più comunemente innesca i processi autofagici è la fame.
Può servirti: esocitosi: processo, tipi, funzioni ed esempiA seconda dell'organismo considerato, diversi tipi di nutrienti essenziali possono innescare questo sistema di "riciclaggio". Nei lieviti, ad esempio, sebbene la mancanza di carbonio di alcuni aminoacidi e acidi nucleici possa indurre l'autofagia, la mancanza di azoto è lo stimolo più efficiente, che è valido anche per le cellule vegetali.
Sebbene non sia stato completamente compreso, le cellule hanno "sensori" speciali per determinare quando un nutriente o un aminoacido essenziali si trovano in condizioni molto basse e quindi scatenano l'intero processo di riciclaggio attraverso i lisosomi.
Nei mammiferi, alcuni ormoni partecipano alla regolazione (positiva o negativa) dell'autofagia nelle cellule appartenenti a determinati organi, come l'insulina, alcuni fattori di crescita o interleuchine, ecc.
Ragazzi
Esistono tre tipi principali di autofagia tra gli eucarioti: macroautofagia, microanophagia e autofagia mediate da chaperones. Se non specificato, il termine autofagia si riferisce ai macroutofagi.
Sebbene i tre tipi di autofagia siano morfologicamente diversi, tutti finiscono nel trasporto di sostanze ai lisosomi per il loro degrado e riciclaggio.
Macroautofago
Questo è un tipo di autofagia che dipende dall'allenamento di novo di vescicole fagocitiche note come autofagosomi. La formazione di queste vescicole è indipendente dalla formazione di "tuorli" di membrana, poiché sono formati dall'espansione.
Nei lieviti, la formazione di autofagosomi inizia in un luogo particolare noto come PAS, mentre nei mammiferi si verificano molti diversi siti di citosol, probabilmente legati al reticolo endoplasmatico attraverso strutture note come "omegasomi".
La dimensione degli autofagosomi è molto variabile e dipende dall'organismo e dal tipo o dalla molecola di organulum che è fagocita. Può variare da 0.4-0.9 μm di diametro in lieviti fino a 0.5-1.5 μm nei mammiferi.
Quando membrane autofagosoma e lisosoma Mel. Questo organello è quindi noto come autolisosoma.
Per alcuni autori, i macroautofagi possono essere sottoclassificati, a sua volta, nell'autofagia indotta e nell'autofagia basale. I macroutofagi indotti vengono utilizzati per produrre aminoacidi dopo un periodo prolungato di fame.
Macroautofagi basali.
Può servirti: zattere lipidiche: caratteristiche, tipi, funzioniMicroanophagia
Questo tipo di autofagia si riferisce al processo in cui il contenuto citoplasmatico viene introdotto al lisosoma attraverso invaginazioni che si verificano nella membrana di detto organello.
Una volta introdotte nel lisosoma, le vescicole prodotte da queste invaginazioni galleggiano liberamente nel lume fino a quando non sono elencate e il loro contenuto viene rilasciato e degradato da enzimi specifici.
Autofagia mediata dal chaperone
Questo tipo di autofagia è stato riportato solo per le cellule dei mammiferi. A differenza della macroautofagia e della microanophagia, dove alcune porzioni citosoliche sono non specifiche di fagocithe.
Alcuni ricercatori hanno stabilito che questo motivo pentapéptide è correlato alla sequenza KFERQ e che è in oltre il 30% delle proteine citosoliche.
Si chiama "chaperonas mediata" poiché le proteine di chaperone sono responsabili del mantenimento di questo motivo conservato per facilitare il loro riconoscimento ed evitare il ripiegamento della proteina su di essa.
Le proteine con questa etichetta sono traslocate nel lume lisosomiale e sono degradate. Molti dei substrati di degradazione sono enzimi glicolitici, fattori di trascrizione e loro inibitori, proteine dell'Unione del calcio o lipidi, subunità proteosoma e alcune proteine coinvolte nel traffico vescicolare.
Così come gli altri due tipi di autofagia, autofagia mediata da chaperon.
Funzioni
Una delle funzioni principali dell'autofago.
Grazie all'osservazione delle microfotografie elettroniche dei lisosomi nelle cellule di mammifero, in questi è stata rilevata la presenza di perossisomi e mitocondri.
In una cellula epatica, ad esempio, il tempo medio di vita di un mitocondria è di 10 giorni, dopo di che questo organello è fagocato dai lisosomi, dove è degradato e i suoi componenti sono riciclati per diversi scopi metabolici.
A bassa concentrazione di sostanze nutrizionali, le cellule possono innescare la formazione di autofagosomi per "catturare selettivamente" le porzioni di citosol, nonché i metaboliti digeriti in questi autofagosomi possono aiutare le cellule a sopravvivere quando le condizioni esterne sono limitanti dal punto di vista nutrizionale.
Può servirti: eritropoiesi: fasi e le sue caratteristiche, regolazione, stimolantiFunzioni in salute e sviluppo
L'autofagia ha importanti funzioni nella ristrutturazione delle cellule nel processo di differenziazione, poiché partecipa a scartare porzioni citosoliche che non sono richieste in momenti specifici.
Ha anche importanti implicazioni nella salute cellulare, in quanto fa parte dei meccanismi di difesa contro i virus e invasori batteri.
Yoshinori Ohsumi Studies
Yoshinori Ohsumi, un ricercatore giapponese nel 2016 con il premio Nobel in fisiologia e medicina, ha descritto i meccanismi molecolari dell'autodifesa nei lievi.
Nelle sue opere, Ohsumi non solo ha identificato le proteine e le rotte coinvolte nel processo, ma ha anche dimostrato come la via dell'autofagia è regolata grazie all'azione delle proteine in grado di "censurare" diversi stati metabolici.
Il suo lavoro è iniziato con precise osservazioni microscopiche durante gli eventi di degradazione intensi. I vacuole sono considerati come i siti di conservazione di "immondizia" e i rifiuti cellulari dai lieviti.
Osservando lieviti con genotipi mutanti difettosi per geni diversi o ipoteticamente correlati correlati all'autofagia (noti come geni Atg), Questo ricercatore e i suoi collaboratori sono riusciti a descrivere il sistema di lievito autofagico a livello genetico.
Successivamente, questo gruppo di ricercatori ha determinato le principali caratteristiche genetiche delle proteine codificate da questi geni e hanno dato un contributo significativo sulla loro interazione e sulla formazione dei complessi responsabili dell'inizio e dell'esecuzione dell'autofase nei lieviti.
Grazie alle opere di Yoshinori Ohsumi, oggi comprendiamo meglio gli aspetti molecolari dell'autofagia, nonché le sue importanti implicazioni nel corretto funzionamento delle cellule e degli organi che ci compongono.
Riferimenti
- Alberts, b., Johnson, a., Lewis, J., Morgan, d., Raff, m., Roberts, k., & Walter, P. (2015). Biologia della cellula molecolare (6 ° ed.). New York: Garland Science.
- Klionsky, d. J., & EMR, s. D. (2000). L'autofagia come via regolata di degradazione cellulare. Scienza, 290, 1717-1721.
- Mizushima, n. (2007). Autofagia: processo e funzione. Geni e sviluppo, ventuno, 2861-2873.
- Mizushima, Noboru e Komatsu, M. (2011). Autostrada: rinnovamento di cellule e tessuti. Cellula, 147, 728-741.
- Rabinowitz, J. D., E bianco, e. (2010). Autofagia e metabolismo. Scienza, 330, 1344-1348.
- « Caratteristiche del Maggio, habitat, riproduzione, controllo biologico
- Caratteristiche della tarantola, habitat, specie, comportamento »

