Alotropi di carbonio
- 3765
- 31
- Brigitta Ferrari
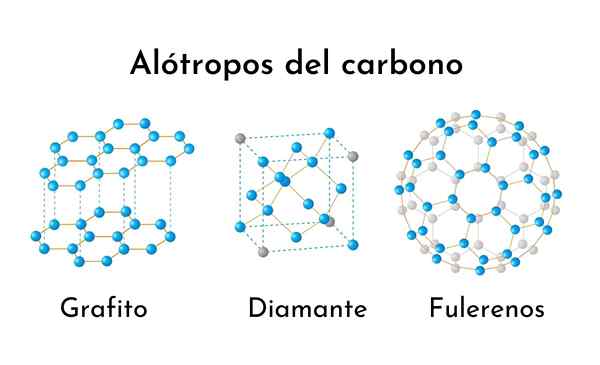
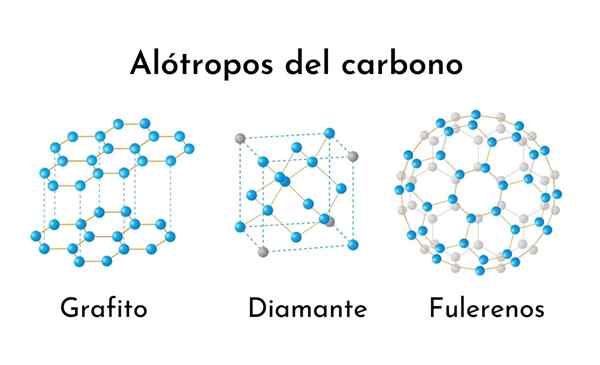 Tre dei più comuni alotropi di carbonio
Tre dei più comuni alotropi di carbonio Cosa sono gli alotropi del carbonio?
La parola alotropica si riferisce alle diverse forme molecolari in cui può essere presentato un elemento chimico. Pertanto, gli alotropi di carbonio sono tutte forme, naturali o no, poiché l'elemento di carbonio puro può essere presentato.
Nonostante abbia esattamente la stessa composizione, gli alotropi possono avere proprietà completamente diverse.
Ciò è particolarmente noto nel caso di Alotropi di carbonio. Come vedremo più avanti, uno degli alotropi, il diamante, si forma perfettamente trasparente e incredibilmente duri, mentre altri sono sostanze morbide e fragili.
Successivamente, tutti gli Alotrop di carbonio sono descritti finora, insieme alle loro proprietà più eccezionali e alle loro applicazioni:
Diamante
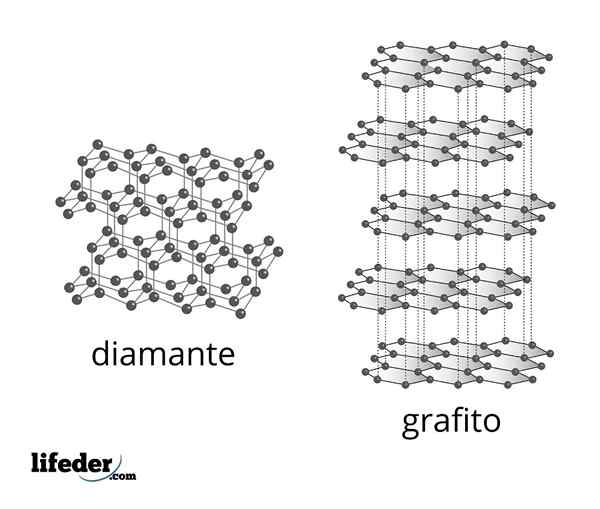 Struttura microscopica di diamante e grafite
Struttura microscopica di diamante e grafite Il diamante è la forma più stabile di carbonio ed è uno dei due alotropi più noti di quell'elemento. È composto da atomi di carbonio tetraedrico con ibridazione SP3 collegato per mezzo di semplici legami covalenti C-C in una rete covalente tridimensionale.
Questo alotropo di carbonio è naturalmente o può essere prodotto industrialmente dalla grafite con elevate pressioni.
Proprietà
- È costituito da un solido cristallino trasparente e incolore che può essere lucidato ad alta luminosità.
- È il minerale più difficile conosciuto dall'uomo. Ciò significa che un diamante è in grado di graffiare la superficie di qualsiasi altro materiale e può essere graffiato solo con un altro diamante.
- È uno degli elementi naturali più costosi al mondo.
- È il miglior conduttore termico noto, con una conducibilità termica tra 1300 e 2300 p/m.K.
- Non conduce elettricità.
- Ha un coefficiente di espansione termica molto bassa.
- Ha un coefficiente di attrito molto basso.
Applicazioni
- Il suo uso quotidiano più noto è nei gioielli.
- A causa della sua durezza è un eccellente materiale abrasivo, quindi viene aggiunto alla superficie di strumenti di taglio e lucidatura di metalli, rocce, ecc.
- A causa delle sue proprietà termiche viene utilizzato nella produzione di dissipatori di calore.
- È utilizzato nella produzione di micro cuscinetti a basso attrito.
Grafite
È un altro degli alotropi del carbonio più noti. È un materiale molto comune che ha una struttura formata da fogli di atomi di carbonio impilati sopra l'altro.
Tutti gli atomi di carbonio in grafite hanno ibridazione SP2, Quindi hanno una struttura trigonale piatta. Ogni carbonio è collegato ad altri tre carboni vicini che formano esagoni simili al benzene, con un sistema di elettroni che Pi hamocato sulla superficie di ciascun foglio, il che rende l'elettricità di condotta di grafite.
Proprietà
- È un materiale nero solido a temperatura ambiente.
- È carburante, quindi puoi bruciare in presenza di ossigeno.
- La grafite è un buon conduttore elettrico.
- Ha un punto di fusione elevato.
- È un materiale morbido che dà l'impressione di essere scivoloso.
- Ha un coefficiente di attrito basso.
- È un buon conduttore termico.
Applicazioni
- Viene spesso usato nella produzione di matite da scrivere o per il disegno.
- Viene spesso usato come lubrificante secco.
- A causa della sua conduttività elettrica e della bassa reattività chimica, viene spesso utilizzato nei contatti elettrici in diversi dispositivi elettronici.
- È usato negli elettrodi per l'analisi chimica.
Grafene
 Struttura del grafene
Struttura del grafene Il grafene non è altro che un foglio di grafite isolata. È definito come un cristallo bidimensionale ed è ottenuto separando gli strati di grafite con nastro adesivo. Il grafene ha proprietà uniche che lo distinguono dalla grafite, nonostante assomigli molto alla struttura.
Può servirti: legge della birra-lambeProprietà
- Alta conducibilità elettrica e termica.
- È un materiale elastico e flessibile, ma allo stesso tempo con alta durezza e resistenza.
- Per avere un singolo spessore dell'atomo di carbonio, è un materiale completamente trasparente.
- Può generare elettricità per esposizione alla luce solare.
Applicazioni
- Schermi flessibili.
- Circuiti elettronici flessibili.
- COPERNI ANTIRROSIVI.
- Pannelli solari molto efficienti.
- Sistemi di sequenziamento del DNA.
- Biosensori ad alta precisione.
Ragazzi o nanocarbonio
I ragazzi sono strutture molecolari chiuse formate solo da atomi di carbonio in cui sono presentate le disposizioni sotto forma di anelli da 4 a 7 membri.
A seconda delle loro dimensioni e forma, diversi tipi di ragazzi sono generalmente distinti:
Buckminsterflerane (c60)
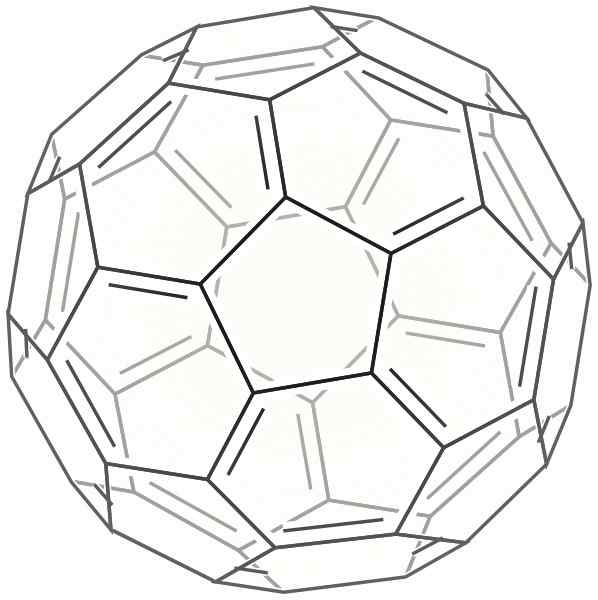 2d Buckminsterflera Skeletro
2d Buckminsterflera Skeletro Questo è a forma di una sfera molto simile a un pallone da calcio. Si chiama anche Bucky Ball.
Proprietà
- Alta conducibilità elettrica e termica
- Alta resistenza alla tensione.
- Formano un materiale molto duttile.
- Sono relativamente inerti alle reazioni chimiche.
Applicazioni
- Antivirali
- Antiossidanti
- Sistemi di amministrazione del farmaco
Nanotubi di carbonio
 Struttura di un nanotubo di carbonio in cui tutti gli atomi di carbonio sono uniti per mezzo di legami covalenti non polari
Struttura di un nanotubo di carbonio in cui tutti gli atomi di carbonio sono uniti per mezzo di legami covalenti non polari Questi formano la base e l'inizio della nanotecnologia. Sono colpi lunghi con forma tubolare e sono uno dei materiali più studiati oggi dalle innumerevoli applicazioni delle loro proprietà uniche.
Proprietà
Hanno le stesse proprietà di base delle palline bucky, ma quando sono allungate, sono migliori conducenti di elettricità in direzione assiale.
Applicazioni
- Nella produzione di materiali nanococosti con proprietà meccaniche, termiche ed elettriche uniche.
- Sistemi elettronici molecolari.
- Biosensori ad alta sensibilità.
- Sistemi di accumulo di energia.
Grafenilene
Questo alotropico ha una struttura di vetro bidimensionale molto simile al grafene, ma formata da unità bifenilene con anelli di quattro membri intervallati tra gli anelli di sei, invece di contenere solo accordi esagonali.
Grafite AA '
Questa è una forma di carbonio scoperta nel 2008. È un tipo speciale di grafite che differisce solo nel modo in cui i fogli di grafite sono impilati sopra l'altro. È una forma di grafite metastabile che può spiegare la formazione e le proprietà di alcuni nanotubi di carbonio di diversi strati.
Grafenilene
Il grafenilene è un nuovo carbrotropico recentemente scoperto. Sono costituiti da una forma di diamante bidimensionale che si ottiene comprimendo la grafite a pressioni molto elevate. Questo fa sì che fogli di grafite si collegino tra loro, formando un diamante di solo pochi atomi di carbonio spessi.
Carbonio amorfo
In genere consiste in una miscela di diverse forme di carbonio in proporzioni diverse. I nanotubi possono contenere o altri tipi di ragazzi, grafite, ecc. Si trova in campioni naturali come minerali o carbone causato dalla pirolisi del legno.
È usato principalmente come combustibile per riscaldamento, generazione di energia o cottura alimentare.
Carbonio vitreo
È una forma di carbonio ottenuta riscaldando alcuni precursori organici ad alte temperature. È un materiale molto resistente alle alte temperature e all'attacco chimico da acido e ossigeno. È anche impermeabile ai gas.

