Alilo Alilic Unit, Carbocation, Radical, Esempi

- 3219
- 582
- Zelida Gatti
Lui Alilo oppure 2-prig. è un gruppo organico o un sostituente la cui formula strutturale è Cho2= Ch-ch2-. È costituito da un frammento di vinile, CH2= Ch- e un gruppo di metilene, -CH2-. È costituito da un gruppo alchenile, specificamente derivato dal propeno, Cho2= Ch-ch3.
Il termine "Alilo" è dovuto al nome botanico usato per fare riferimento all'aglio: Allium sativum, i cui oli nel 1892 furono isolati il quadrante composto di disolfuro, h2C = chch2Ssch2Ch = ch2, responsabile in parte dei suoi odori caratteristici. In effetti, molti composti alilici, cioè quelli che hanno il gruppo Alilo, si trovano in aglio e verdure.
 Gruppo Alilo
Gruppo Alilo L'immagine superiore mostra la formula scheletrica del gruppo Alilo. Oltre le sinuosità a destra abbiamo il resto della molecola; Se questo è Alquilica, sarà rappresentato con il simbolo R.
È facile riconoscere Alilo perché assomiglia molto al gruppo in vinile. Tuttavia, Alilo può anche essere ciclico, che passa inosservato in composti come Ciclope.
Un esempio di un composto allilico è alcool alleato, h2C = chch2OH. Gli igeni del frammento di vinile possono essere sostituiti e rimangono un Alilo. Pertanto, il 3-metil-2-bunt-1-ol, (Cho3)2C = chch2Oh, è anche un alcol alteico. Pertanto, è possibile l'esistenza di Alilos ciclici.
[TOC]
Unità allyica e le sue parti
Più importante del gruppo Alilo, è l'unità allyica che è la stessa per tutti i composti allic. Questo è: c = c-c. L'estremità c = c corrisponde ai carboni in vinile. Tutti gli atomi legati a questi due carboni riceveranno anche il nome di sostituenti in vinile. Ad esempio, se sono idrogeni, Cho2= CH, parliamo di idrogeni in vinile.
Nel frattempo, d'altra parte, Extreme -C corrisponde al carbonio allic. Tutti gli atomi o i gruppi collegati a questo carbonio saranno chiamati sostituenti Allic. Pertanto, i composti altiici sono esattamente tutti coloro che hanno un gruppo funzionale (OH, S, F, COOH, ecc.) Carbonio allegato collegato.
Può servirti: citrato di sodio (c6h5o7na3): struttura, usi, proprietàI carboni in vinile hanno ibridazione SP2, Quindi sono più elettronegativi del carbonio allyic, spo3. Questa differenza di elettronegatività aumenta l'acidità degli idrogeni altiici, essendo probabile la formazione di carbani altiico. Ma più redditizio in termini di sintesi organica, è il carbocalizzazione allilica, che verrà spiegato di seguito.
Carbocalizzazione
Strutture di risonanza
 Strutture di risonanza di carbocalizzazione allyic. Fonte: dissoluzione/cc by-s (https: // creativecommons.Org/licenze/by-sa/3.0)
Strutture di risonanza di carbocalizzazione allyic. Fonte: dissoluzione/cc by-s (https: // creativecommons.Org/licenze/by-sa/3.0) Nell'immagine superiore, viene mostrato il carbocalizzazione di Ally. Si noti che il carico positivo, (+), appare per primo su Allic Carbon. Tuttavia, immediatamente gli elettroni a doppio legame saranno attratti da questo carico, quindi si muoveranno nella direzione dell'atomo di carbonio allyic.
Di conseguenza, abbiamo due strutture di risonanza (a sinistra dell'immagine). Ora, il carico positivo si trova su uno dei carboni in vinile. Ancora una volta, gli elettroni del doppio legame del lato Allico saranno nuovamente attratti dal carico positivo e torneranno alla loro posizione iniziale. Questo viene ripetuto ancora e ancora, a velocità inimmaginabili.
Il risultato: il carico positivo, +1, viene trasferito o disperso tra i tre atomi dell'unità Allic; ma concentrandosi solo sui due carboni delle estremità. Pertanto, uno dei carboni in vinile conserva un carico di 1/2 +, mentre il carbonio allilico rimane con l'altra metà del carico, aggiungendo +1.
Un modo più appropriato per rappresentare il carbocalizzazione alteico è attraverso il suo ibrido di risonanza (a destra dell'immagine). Pertanto, si osserva che il carico positivo è distribuito in tutta l'unità Allic.
Può servirti: cloruro di alluminio (ALCL3)Stabilità e distribuzione del carico positivo
La democazione del carico positivo fornisce carbocalizzazione alteica di stabilità. È così tanto che è equiparato a un carbocalizzazione secondaria in termini di stabilità.
Nell'immagine, poiché è solo l'unità AllLIC, si presume che la distribuzione del carico positivo sia equivalente a entrambi i carboni (+1/2 per ciascuno). Ma questo non è soddisfatto per tutti i composti Allic. Pertanto, ci saranno carbocazioni più o meno positive; Ciò significa che saranno più o meno reattivi.
Considera, ad esempio, il catione Alilo:
H2C = CH-CH2+ ↔ h2C+-Ch = ch2
Le due strutture di risonanza sono equivalenti distribuendo il carico positivo. Non accade lo stesso, tuttavia, con il catione 1.1-dimetill:
H2C = CH-C+(Ch3)2 ↔ h2C+-CH = C (CH3)2
Nella struttura della sinistra, il carico positivo è più stabilizzato dalla presenza dei due gruppi metilici, che donano parte della loro densità di alleato negativa.
Nel frattempo, gli idrogeni in vinile non contribuiscono al carico positivo sul carbonio in vinile. Pertanto, la struttura della sinistra contribuirà maggiormente all'ibrido di risonanza di questo catione alilico.
È fondamentale tenere presente che sono ibridi di risonanza che sono più vicini allo stato reale di queste carbocazioni e non le loro strutture separatamente.
Radicale
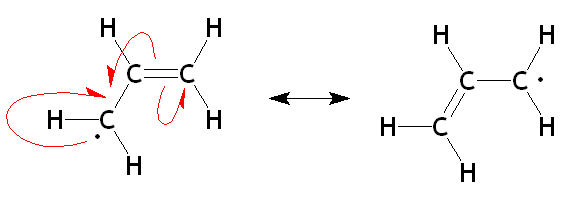 Strutture di risonanza radicale Alilo. Fonte: OrganAute/CC BY-SA (https: // creativeCommons.Org/licenze/by-sa/3.0)
Strutture di risonanza radicale Alilo. Fonte: OrganAute/CC BY-SA (https: // creativeCommons.Org/licenze/by-sa/3.0) Nell'immagine superiore, sono ora mostrate le due strutture di risonanza del radicale allyico nella rispettiva unità allilica. Si noti che la natura del suo sviluppo è la stessa del carbocalizzazione: l'elettrone scomparso (·) è democalizzato tra i due carboni delle estremità. Pertanto, ognuno avrà "mezzo elettronico" (1/2 ·).
Può servirti: cationi: formazione, differenze con l'anione ed esempiCiò che viene spiegato per il carbocalizzazione e quelli allitici radicali si applica anche al rispettivo Carbanion, in cui ciascuno dei due atomi di carbonio menzionati avrà un carico a metà negativo (-1/2).
Esempi di composti alilici
Saranno menzionati per finire diversi esempi di composti alilici. In ognuno di essi sarà presente l'unità Allic:
-Alilo cloruro, h2C = CH-CH2-Cl
-Metil solfuro alliico, h2C = CH-CH2-S-ch3 (Un altro composto responsabile dell'odore dell'aglio)
-Alicina, h2C = CH-CH2-S (o) -s -ch2-Ch = ch2
-Alcool crotilico, Cho3Ch = ch --ch2OH (si noti che uno degli idrogeni in vinile è sostituito da un metile)
-Alilo acetato, h2C = CH-CH2-OC (O) CH3
-Alilo Bromide, H2C = CH-CH2-Br
-Alilamina, h2C = CH-CH2-NH2 (Unità di base per alilamine più complesse che vengono utilizzate come antifungidi)
-Dimetilalil pirofosfato, (CH3)2C = CH-CH2-OPO2-O-PO3
Nella prossima coppia di alilamine, flunarizina e naftifina, entrambe con effetti farmacologici, possiamo apprezzare il gruppo Alilo:
 Formule strutturali di due alilamine. Fonte: HBF878 / CC0.
Formule strutturali di due alilamine. Fonte: HBF878 / CC0. In entrambi è sulla destra: quel doppio legame archiviato tra gli anelli di piperina (l'esagonale con due atomi di azoto) e il benzene. Si noti che per identificare Alilo è essenziale.
Riferimenti
- Morrison, r. T. e Boyd, r, n. (1987). Chimica organica. 5a edizione. Editoriale Addison-Wesley Inter-American.
- Carey f. (2008). Chimica organica. (Sesta edizione). Mc Graw Hill.
- Graham Solomons t.W., Craig b. Frigorifero. (2011). Chimica organica. (10a edizione.). Wiley Plus.
- Wikipedia. (2020). Gruppo allilico. Recuperato da: in.Wikipedia.org
- Elsevier b.V. (2020). Composto allilico. Scienceirect. Estratto da: ScienceDirect.com
- Gamini Gunawardena. (5 giugno 2019). Carbonio allilico. Chimica librettexts. Recuperato da: Chem.Librettexts.org
- « Caratteristiche dei costi storici, vantaggi, svantaggi, esempi
- Concetto di riferimenti incrociati, funzioni, esempi »

