Alcool secondario Cosa sono, struttura, proprietà, usi
- 3600
- 524
- Silvano Montanari
Cos'è un alcol secondario?
UN Alcool secondario Ha il carbonio del carbonio del gruppo idrossilico (OH), attaccato a due carboni. Nel frattempo, nell'alcool primario il carbonio in carbonio del gruppo idrossilico è collegato a un atomo di carbonio e nell'alcool terziario attaccato a tre atomi di carbonio.
Gli alcoli sono acidi leggermente più deboli dell'acqua, con la seguente PKA: acqua (15,7); Alcoli metilici (15,2), etil (16), isopropil (alcool secondario, 17) e termici (18). Come si può vedere, l'alcol isopropilico è meno acido degli alcoli di metil ed etilico.
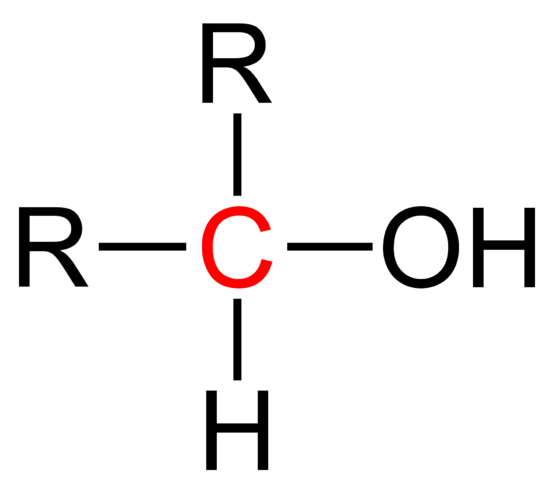
 Formula strutturale di un alcol secondario. Wikimedia Commons
Formula strutturale di un alcol secondario. Wikimedia Commons Nell'immagine superiore viene mostrata la formula strutturale per un alcol secondario. Il carbonio rosso è il portatore di OH ed è collegato a due gruppi alchil (o aril) e un singolo atomo di idrogeno.
Tutti gli alcoli hanno la formula generica ROH; Ma se il carbonio del portatore è osservato in dettaglio, si ottengono gli alcoli primari (RCH2Oh), secondario (r2Choh, cresciuto qui) e terziario (R3COH). Questo fatto fa la differenza nelle sue proprietà fisiche e reattività.
Struttura di un alcol secondario
Le strutture di alcol dipendono dalla natura dei gruppi R. Tuttavia, per gli alcoli secondari, è possibile effettuare qualche esemplificazione, considerando che possono esserci solo strutture lineari con o senza ramificazioni o strutture cicliche. Ad esempio, hai la seguente immagine:
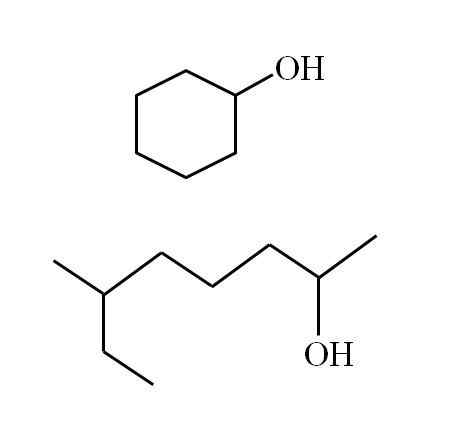 Un alcol secondario ciclico e un'altra catena ramificata. Fonte: Gabriel Bolívar
Un alcol secondario ciclico e un'altra catena ramificata. Fonte: Gabriel Bolívar Si noti che per entrambe le strutture c'è qualcosa in comune: OH è collegato a una "V". Ogni estremità di V rappresenta un gruppo uguale (parte superiore dell'immagine, struttura ciclica) o diversa (parte inferiore, catena ramificata).
In questo modo ogni alcol secondario viene identificato molto facilmente, anche se la sua nomenclatura è affatto sconosciuta.
Proprietà
Punti bollenti
Le proprietà degli alcoli secondari non differiscono troppo dagli altri alcoli. Di solito sono liquidi trasparenti ed essere solidi a temperatura ambiente, deve formare diversi ponti idrogeno e avere una massa molecolare alta.
Può servirti: acido perbromico (HBRO4): proprietà, rischi e usiTuttavia, la stessa formula strutturale R2Choh suggerisce alcune proprietà uniche in generale per questi alcoli. Ad esempio, il gruppo OH è meno esposto e disponibile per le interazioni con ponti idrogeno, R2CH-OH-OHCHR2.
Questo perché i gruppi R, adiacenti al carbonio per auto, possono essere portati e ostacolano la formazione di ponti idrogeno. Di conseguenza, gli alcoli secondari hanno punti di ebollizione più bassi rispetto ai primari (RCH2OH).
Acidità
Secondo la definizione di Brönsted-Lowry, un acido è uno che dona protoni o ioni idrogeno, H+. Quando questo accade con un alcol secondario, hai:
R2Choh + b- => R2Cho- + Hb
Il coniugata Ras2Cho-, Anione di alcossido, il carico negativo deve stabilizzarsi. Per l'alcol secondario, la stabilizzazione è inferiore poiché i due gruppi R hanno una densità elettronica, il che respinge il carico negativo sull'atomo di ossigeno in una certa misura.
Nel frattempo, per l'anione alcossido di un alcol primario, RCH2O-, C'è meno repulsione elettronica con un solo gruppo R e non due. Inoltre, gli atomi di idrogeno non esercitano una repulsione significativa e, al contrario, contribuiscono a stabilizzare il carico negativo.
Pertanto, gli alcoli secondari sono meno acidi degli alcoli primari. Se è così, allora sono più semplici e precisamente per le stesse ragioni:
R2Choh + H2B+ => R2Choh2+ + Hb
Ora, i gruppi R stabilizzano il carico positivo nell'ossigeno dando parte della loro densità elettronica.
Reazioni
Halogenide idrogeno e fosforo trihalogenide
Un alcool secondario può reagire con un alogenuro di idrogeno. L'equazione chimica della reazione tra alcool isopropilico e acido bromoriterico è mostrata in un mezzo di acido solforico e produce bromuro di isopropil:
Cap3Chohch3 + HBr => CH3Chbrch3 + H2O
E puoi anche reagire con un trihalogenuero di fosforo, PX3 (X = br, i):
Può servirti: idrossido di nichel (III): struttura, proprietà, usi, rischiCap3-Choh-ch2-Cap2-Cap3 + Pbr3 => CH3-CHBR-CH2-Cap2-Cap3 + H3Po3
La sostanza chimica di sopra corrisponde alla reazione tra la sezione e la tribromuro di fosforo, causando bromuro di sec-pentile.
Si noti che in entrambe le reazioni c'è un alogenuro alchilico secondario (R2CHX).
Disidratazione
In questa reazione si perdono un H e un OH di carboni vicini, formando un doppio legame tra questi due atomi di carbonio. Pertanto, esiste la formazione di un alchene. La reazione richiede un catalizzatore acido e un alimentazione di calore.
Alcool => Alkene + H2O
Hai ad esempio la seguente reazione:
CycloHexanol => Cyclohexen + H2O
Reazione con metalli attivi
Gli alcoli secondari possono reagire con i metalli:
Cap3-Choh-ch3 + K => Cho3Cho-K+Cap3 + ½ h+
Qui l'alcool isopropilico reagisce con potassio per formare isoproossido di potassio e ioni idrogeno.
Esterificazione
L'alcool secondario reagisce con un acido carbossilico per originare un estere. Ad esempio, l'equazione chimica della reazione di alcol secutilico è mostrata con acido acetico, per produrre semi-butil acetato:
Cap3Chohch2Cap3 + Cap3COOH CH3Coochch3Cap2Cap3
Ossidazione
Gli alcoli primari ossidano gli aldeidi e questi a loro volta ossidano gli acidi carbossilici. Ma gli alcoli secondari ossidano l'acetone. Le reazioni sono generalmente catalizzate dal dicromato di potassio (K2CRO7) e acido cromico (H2CRO4).
La reazione globale è:
R2Choh => r2C = O
Nomenclatura
Gli alcoli secondari sono nominati indicando la posizione del gruppo OH nella catena principale (più a lungo). Questo numero precede il nome o può seguire il nome del rispettivo alcano per detto catena.
Ad esempio, Cho3Cap2Cap2Cap2Chohch3, È il 2-esanolo o da esano-2-a.
Se la struttura è ciclica, non è necessario posizionare un numeratore; a meno che non ci siano altri sostituenti. Ecco perché l'alcol ciclico della seconda immagine si chiama cicloesanolo (l'anello è esagonale).
Può servirti: ammineE per l'altro alcol della stessa immagine (il ramificato), il suo nome è: 6-etil-eptan-2 -ol.
Applicazioni
-Sec-butanolo viene utilizzato come chimico solvente e intermedio. È presente nei fluidi idraulici per freni, detergenti industriali, lucidatura, pinting, agenti di flottazione minerale e frutta ed essenze di profumo.
-L'alcol isopropanolo è usato come solvente industriale e come anticoagulante. È usato in oli e inchiostri ad asciugatura rapida, come antisettico e sostituto dell'etanolo cosmetico (ad esempio: lozioni della pelle, tonico capillare e alcol di attrito).
-L'isopropanolo è un ingrediente di saponi liquidi, detergenti di cristalli, aromatizzatori sintetici di bevande e cibo non alcoliche. Inoltre, è una sostanza chimica intermedia.
-Il cicloesanolo viene utilizzato come solvente, nella finitura tissutale, nell'elaborazione di pelle in pelle e emulsionali e detergenti sintetici.
-Il metilciclohexanolo è un ingrediente di prodotti chewling basati sul sapone e sui detergenti per i tessuti speciali.
Esempi
2-Octanolo
 Molecola a 2-ortanolo. Fonte: Jü [dominio pubblico], di Wikimedia Commons
Molecola a 2-ortanolo. Fonte: Jü [dominio pubblico], di Wikimedia Commons È un alcol grasso. È un liquido incolore, poco solubile in acqua, ma solubile nella maggior parte dei solventi non polari. Viene utilizzato, tra gli altri usi, nell'elaborazione di sapori e fragranze, dipinti e rivestimenti, inchiostri, adesivi, cure domestiche e lubrificanti.
Estradiolo o 17β-Stradiol
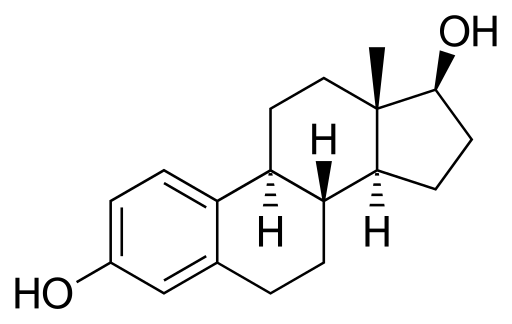 Molecola di estradiolo. Fonte: Neurotoger [dominio pubblico], di Wikimedia Commons
Molecola di estradiolo. Fonte: Neurotoger [dominio pubblico], di Wikimedia Commons È un ormone sessuale steroideo. Ha due gruppi di idrossilli nella sua struttura. È gli estrogeni predominanti durante gli anni riproduttivi.
20-idrossi-leucotrieni
È un metabolita che probabilmente ha origine dall'ossidazione dei lipidi leucotriene. È classificato come un cistinyl. Questi composti sono mediatori del processo infiammatorio che contribuiscono alle caratteristiche patofisiologiche della rinite allergica.
2-eptanolo
È un alcol che si trova in frutta. Inoltre, si trova in olio di zenzero e fragole. È trasparente, incolore e insolubile in acqua. Viene usato come solvente di più resine e interviene nella fase di flottazione nell'elaborazione minerale.
Riferimenti
- Enciclopedia di salute e sicurezza sul lavoro. (S.F.). Alcoli. [PDF]. Recuperato da: insht.È
- Struttura e classificazione degli alcoli. Chimica librettexts. Recuperato da: Chem.Librettexts.org
- « Tlachichinole cosa sono, caratteristiche, vantaggi, applicazione
- La storia e il significato della bandiera dell'Iraq »

