Struttura dell'acetato di ammonio, proprietà, usi e rischi

- 1816
- 352
- Ruth Cattaneo
Lui Acetato di ammonio È un sale inorganico la cui formula chimica è NH4Cap3COOH. Deriva dalla miscela di acido acetico, presente in aceto commerciale a una concentrazione del 5%e nell'ammoniaca. Entrambe le sostanze iniziali hanno odori caratteristici, quindi è possibile avere un'idea del perché questo sale ha un odore di aceto-ammonia.
Tuttavia, il momento clou più di questo sale non è il suo odore, ma il suo basso punto di fusione. È così basso, che in qualsiasi laboratorio potrebbe essere ottenuto nella sua versione liquida, dove gli ioni fluiscono liberamente per trasportare carichi elettrici.
 Cristalli di acetato di ammonio. Fonte: Vidak [dominio pubblico].
Cristalli di acetato di ammonio. Fonte: Vidak [dominio pubblico]. D'altra parte, l'acetato di ammonio è delizioso; cioè, assorbire l'acqua o l'umidità dell'ambiente fino a quando non è completamente sciolto. Ecco perché, sebbene nello stato anidro i loro cristalli sono bianchi, diventano rapidamente luminosi (come quelli nel becher dell'immagine superiore).
Essendo una solida fonte di ammoniaca, deve essere manipolata in modo tale che l'inalazione dei suoi vapori sia ridotta al minimo. Ma, nonostante questa caratteristica negativa, l'NH4Cap3COOH è utile per la preparazione di soluzioni tamponi che mantengono, mentre è un componente di alcuni estrattori di proteine solventi.
[TOC]
Struttura dell'acetato di ammonio
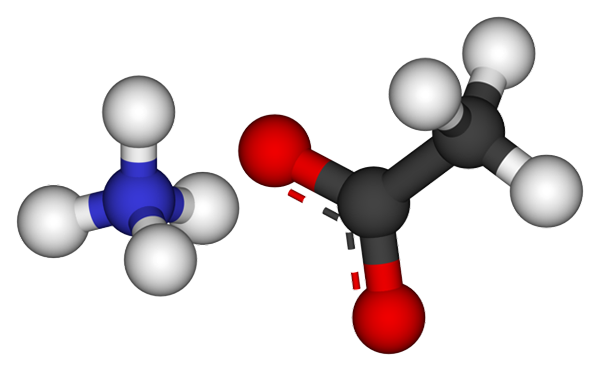 Ioni acetato di ammonio. Fonte: ccoil [CC BY-SA 3.0 (https: // creativeCommons.Org/licenze/by-sa/3.0)]
Ioni acetato di ammonio. Fonte: ccoil [CC BY-SA 3.0 (https: // creativeCommons.Org/licenze/by-sa/3.0)] L'immagine superiore mostra gli ioni che compongono l'acetato di ammonio in un modello di sfere e barre. A sinistra è il catione di geometria tetraedrica, NH4+, Mentre alla tua destra l'anione molecolare con due elettroni democati tra due atomi di ossigeno, CH3COO- (La linea tratteggiata tra le sfere rosse).
Quindi entrambi gli ioni, NH4+ e ch3COO-, Rimangono uniti dalla loro attrazione elettrostatica che, insieme alle repulsioni tra i carichi uguali, finiscono per definire un cristallo. Questo cristallo di acetato di ammonio ha una struttura ortorrombica, che potrebbe essere osservata in campioni microscopici o addirittura dimensioni visibili.
Può servirti: collegamento ionico: caratteristiche, come si forma e esempiNon solo il legame ionico per questo sale è importante, ma anche i ponti idrogeno. Il NH4+ Puoi donare fino a quattro di questi ponti; Cioè, in ciascuno dei vertici del suo tetraedro c'è un atomo di ossigeno da un CHO3COO- vicino (h3N+-H-OCS3).
In teoria, le forze all'interno dei loro cristalli dovrebbero quindi essere molto forti; Ma sperimentalmente si verifica il contrario, poiché si scioglie solo 114 ° C. Pertanto, i ponti di idrogeno non compensano la debolezza del loro legame ionico, né la bassa energia reticolare del vetro NH ortorrombic4Cap3COO.
Altre composizioni e acqua
Si diceva all'inizio che l'acetato di ammonio viene preparato mescolando acido acetico e ammoniaca. Pertanto, il sale può anche essere espresso come: NH3Cap3COOH. Pertanto, a seconda della composizione, è possibile ottenere altre strutture: NH3· 2ch3COOH, O NH3· 5ch3COOH, per esempio.
È stato anche detto che assorbe abbastanza umidità. In tal modo, incorpora molecole d'acqua ai suoi cristalli, che sono idrolizzati dando NH3 o ch3COOH; Ed è per questo che il sale emette un odore di ammoniaca o aceto.
Proprietà
Aspetto fisico
Cristalli bianchi delicuescenti con un odore di aceto e ammoniaca.
Massa molare
77.083 g/mol.
Densità
1.073 g/ml a 25 ° C.
Punto di fusione
114ºC. Questo valore è considerevolmente più basso rispetto ad altri sali o composti ionici. Inoltre, manca di un punto di ebollizione a causa della formazione di ammoniaca, implicando la decomposizione del sale.
Solubilità
143 g/100 ml a 20 ° C. Nota la tua straordinaria solubilità dell'acqua, che dimostra l'affinità che le molecole d'acqua si sentono sugli ioni NH4+ e ch3COO-, Heling li in sfere acquose.
Può servirti: regole di hume-rotheryLa sua solubilità non è tale nei solventi meno polari. Ad esempio, in 100 ml di metanolo a 15 ° C 7,89 g di NH dissolve4Cap3COO.
Stabilità
È delizioso, quindi dovresti evitare di riporre negli spazi bagnati. Inoltre, mentre l'assorbimento dell'acqua libera l'ammoniaca e quindi, si decompone.
PKA
9.9.
Questa costante corrisponde all'acidità dello ione di ammonio:
NH4+ + B nh3 + Hb
Dove hb è un acido debole. Se la base B è l'acqua, la sua reazione di idrolisi sarà una reazione:
NH4+ + H2O nh3 + H3O+
In cui le specie h3O+ Definire il pH della soluzione.
D'altra parte, l'acetato contribuisce anche al pH:
Cap3COO- + H2O ch3COOH + OH-
Quindi, entrambe le specie H3O+ e oh- Sono neutralizzati dando un pH 7, neutro. Tuttavia, secondo Pubchem, le soluzioni altamente concentrate di acetato di ammonio hanno un pH acido; il che significa che l'idrolisi NH predomina4+ Informazioni sulla scelta3COO-.
Entalpia di formazione standard
ΔFH298 = -615 kJ/mol.
Applicazioni
Analitico
Le soluzioni acquose di acetato di sodio consentono di solubilizzare i solfati di piombo, ferro e zinco, per determinare successivamente la loro concentrazione mediante spettroscopia di assorbimento atomico.
Mezzo conducente
Come pasti a bassa temperatura rispetto ad altri sali, il suo liquido può essere utilizzato per guidare la corrente elettrica che gira sul circuito di un bulbo.
Respingente
È possibile regolare i cambiamenti di pH negli intervalli acidi o di base, che viene utilizzato per mantenere un pH costante, ad esempio carni, cioccolatini, formaggi, verdure o altri prodotti alimentari.
Può servirti: molibdenoSul ghiaccio e sui pavimenti
È un sale biodegradabile e relativamente economico, utilizzato per sfogare i percorsi ghiacciati. Inoltre, poiché è una fonte di azoto solubile in acqua, è destinato agli usi agricoli per la determinazione dei livelli di potassio.
Agente precipitante
Questo sale viene utilizzato per precipitare la proteina per eseguire analisi cromatografiche.
Medicinale
L'acetato di ammonio funziona come agente diuretico veterinario ed è anche un sale necessario per la sintesi di insulina e penicillina.
Rischi
Successivamente e infine alcuni rischi o conseguenze negative causate dall'acetato di ammonio:
- Può produrre lievi irritazioni sulla pelle, ma senza assorbire.
- Quando ingerito causano stomaco, diarrea, diuresi, ansia, maggiore necessità di urinare, tremori e altri sintomi legati all'avvelenamento da ammoniaca, nonché danneggiare il fegato.
- La sua inalazione irrita il naso, la gola e i polmoni.
Del resto, non è noto se il cancro può generare e ogni possibile rischio di incendio da parte di questo sale viene scartato (almeno in condizioni di conservazione normali).
Riferimenti
- Inger Nahringbauer. (1967). Studi sul legame idrogeno. Xiv. La struttura cristallina dell'acetato di ammonio. Institute of Chemistry, University of Uppsala, Uppsala, Svezia. Cryst Act. 23, 956.
- Centro nazionale per le informazioni sulla biotecnologia. (2019). Acetato di ammonio. Database PubChem. CID = 517165. Recuperato da: pubchem.NCBI.Nlm.NIH.Gov
- Sullivan Randy. (2012). Conduttività di acetato di ammonio. Recuperato da: Chemdemos.Uoregon.Edu
- Viachem, Ltd. (S.F.). Acetato di ammonio. Recuperato da: viacheminc.com
- Wikipedia. (2019). Acetato di ammonio. Recuperato da: in.Wikipedia.org
- Dipartimento della salute del New Jersey. (2012). Acetato di ammonio: foglio di informazioni su sostanze pericolose. [PDF]. Recuperato da: NJ.Gov
- Xueyanghu. (S.F.). Usi e rischi di acetato di ammonio. Recuperato da: xueyanghu.WordPress.com
- « Caratteristiche di alizarina, preparazione, usi e tossicità
- Struttura, proprietà e usi di idrossido di ferro (III) »

