Assorbimento molare
- 4832
- 948
- Enzo De Angelis
Cos'è l'assorbimento molare?
IL Assorbimento molare È una proprietà chimica che indica quanta luce può assorbire una specie in soluzione. Cioè, è un'unità che misura la capacità di una soluzione di assorbire la luce.
Poiché la luce è costituita da fotoni con energia (o lunghezze d'onda), a seconda della specie o della miscela mista, un fotone può essere assorbito in misura maggiore di un altro. Significa che la luce viene assorbita a determinate lunghezze d'onda caratteristiche della sostanza.
Pertanto, il valore dell'assorbità molare è direttamente proporzionale al grado di assorbimento della luce a una certa lunghezza d'onda. Se la specie assorbe poca luce rossa, il suo valore assorbente sarà basso. Se c'è un pronunciato assorbimento della luce rossa, l'assorbità avrà un valore elevato.
Una specie che assorbe la luce rossa rifletterà un colore verde. Se il colore verde è molto intenso e scuro, significa che c'è un forte assorbimento di luce rossa.
Tuttavia, alcune tonalità verdi possono essere dovute ai riflessi di diverse gamme di giallo e blu, che sono miscelati e percepiti come verde turchese, smeraldo, vetro, ecc.
Equazione assorbente molare
L'assorbità molare è una costante definita nell'espressione matematica della legge di Lambert-Beer e sottolinea semplicemente quanta luce assorbe le specie chimiche o la miscela. L'equazione è:
A = εbc
Dove a è l'assorbanza della soluzione a una lunghezza d'onda λ selezionata, B è la lunghezza della cella in cui è contenuto il campione da analizzare e, quindi, è la distanza che la luce passa attraverso la soluzione, C è il Concentrazione delle specie assorbenti e ε, assorbimento molare.
Può servirti: AlquinosDato λ, espresso in nanometri, il valore di ε rimane costante. Ma modificando i valori di λ, cioè misurando le assorbanze con luci di altre energie, ε cambiamenti, raggiungendo un valore minimo o massimo.
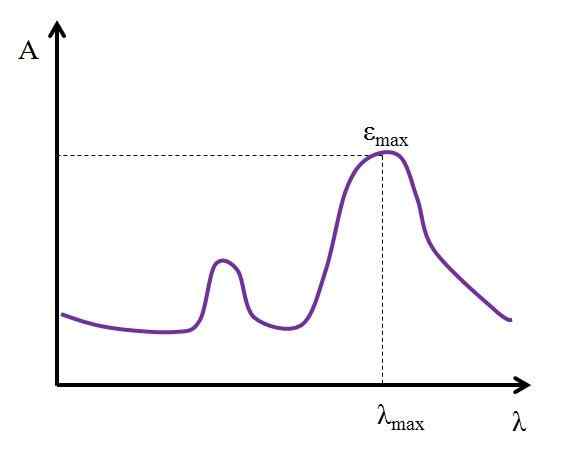
Se è noto il suo valore massimo, εMax, È determinato allo stesso tempo λMax. Cioè, la luce che assorbe di più la specie:
 Grafico in cui sono mostrati i valori di assorbimento della luce massima di una specie chimica. Fonte: Gabriel Bolívar
Grafico in cui sono mostrati i valori di assorbimento della luce massima di una specie chimica. Fonte: Gabriel Bolívar Unità
Per conoscere le unità di ε, dobbiamo sapere che le assorbanze sono valori senza dimensioni e, quindi, la moltiplicazione delle unità B e C deve essere annullata.
La concentrazione delle specie assorbenti può essere espressa in G/L o mol/L e B di solito si esprime in CM o M (perché è la lunghezza della cellula che attraversa il raggio di luce). La molarità è uguale a mol/L, quindi C è anche espresso come m.
Pertanto, si ottiene moltiplicando le unità B e C: M ∙ CM. Le unità che ε devono lasciare il valore di A sono quelle che si moltiplicano.
Clearing u, sei semplicemente ottenuto m-1∙ cm-1, che può anche essere scritto come: l ∙ mol-1∙ cm-1.
In effetti, usa m unità-1∙ cm-1 o l ∙ mol-1∙ cm-1 accelera i calcoli per determinare l'assorbità molare. Tuttavia, di solito è anche espresso con M unità2/mol o cm2/mol.
Se espressi con queste unità, alcuni fattori di conversione devono essere utilizzati per modificare le unità B e C.
Come calcolare l'assorbità molare?
Autorizzazione diretta
L'assorbità molare può essere calcolata direttamente dalla sua compensazione nell'equazione precedente:
Può servirti: acidi e basi nella vita di tutti i giorni: reazioni, usi, esempiε = A/BC
Se è nota la concentrazione delle specie assorbenti, la lunghezza della cellula e ciò che è l'assorbanza ottenuta a una lunghezza d'onda, può essere calcolata ε. Tuttavia, questo modo per calcolare produce un valore inaffermatico e inaffidabile.
Metodo grafico
Se l'equazione della legge di Lambert-Beer viene attentamente osservata, si noterà che ricorda l'equazione di una linea (y = ax+b).
Ciò significa che se i valori dell'asse A sono grafici. Quindi, sarebbe y, x sarebbe C e sarebbe equivalente a εb.
Pertanto, il grafico della linea, basta solo due punti per determinare la pendenza, cioè a. Una volta fatto ciò e la lunghezza della cella, B, è facile cancellare il valore di ε.
A differenza della liquidazione diretta, grafico vs. C Consente di misure di assorbanza media e ridurre l'errore sperimentale, e anche attraverso un singolo punto possono passare dritti infiniti, quindi la clearance diretta non è pratica.
Inoltre, gli errori sperimentali possono fare una linea non passare attraverso due, tre o più punti, quindi viene effettivamente utilizzata la linea ottenuta dopo aver applicato il metodo quadrato minimo (funzione già incorporata nei calcolatori).
Tutto ciò assumendo un'elevata linearità, e quindi, il rispetto della legge di Lamber-Beer.
Esercizi risolti
Esercizio 1
È noto che una soluzione di un composto organico con una concentrazione di 0.008739 m ha presentato un'assorbanza di 0.6346, misurato a λ = 500 nm e con una cella di 0.5 cm di lunghezza. Calcola ciò che è l'assorbimento molare del complesso a detta lunghezza d'onda.
Può servirti: nichel: storia, proprietà, struttura, usi, rischiDa questi dati può essere cancellato direttamente ε:
ε = 0.6346/(0.5 cm) (0.008739 m)
145.23 m-1∙ cm-1
Esercizio 2
Le seguenti assorbimenti misurate a diverse concentrazioni di un complesso metallico a una lunghezza d'onda di 460 nm e con una cella lunga 1 cm: lunghezza:
A: 0.03010 0.1033 0.1584 0.3961 0.8093
C: 1.8 ∙ 10-5 6 ∙ 10-5 9.2 ∙ 10-5 2.3 ∙ 10-4 5.6 ∙ 10-4
Calcola l'assorbità molare del complesso.
Ci sono un totale di cinque punti. Per calcolare ε è necessario graficarli posizionando i valori di A sull'asse y. Una volta fatto ciò, viene determinata la linea dei quadrati minimi e con la sua equazione può essere determinato ε.
In questo caso, i punti grafici e tracciano la linea con un coefficiente di determinazione R2 di 0.9905, la pendenza è pari a 7 ∙ 10-4, cioè, εb = 7 ∙ 10-4.
Pertanto, con b = 1 cm, ε sarà 1428,57 m-1.cm-1 (1/7 ∙ 10-4).
Riferimenti
- Coefficiente di attenuazione molare. Recuperato da.Wikipedia.org
- Struttura scientifica. Assorbimento molare. Recuperato da sciencestruck.com
- Analisi colorimetrica (legge della birra o analisi spettrofotometrica). Chimica recuperata.Ucla.Edu

