Triadi Döbereiner
- 967
- 275
- Lidia Valentini
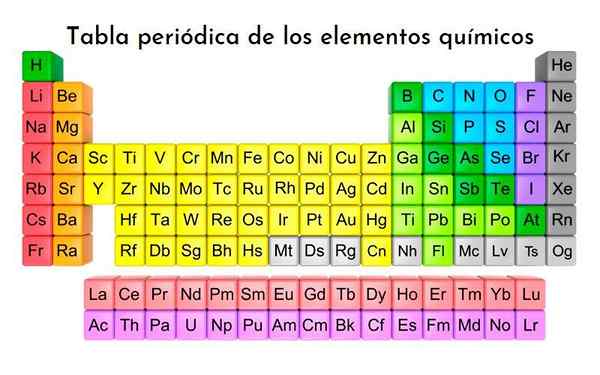
 Tabella periodica degli elementi, tutti gli elementi chimici finora scoperti sono classificati. Con licenza
Tabella periodica degli elementi, tutti gli elementi chimici finora scoperti sono classificati. Con licenza Quali sono le triadi di Döbereiner?
IL Triadi Döbereiner Sono il primo esperimento in cui sono stati raggruppati tre elementi chimici che condividono caratteristiche simili, associandole ai loro pesi atomici. Fanno parte degli 118 elementi chimici, essendo la diversità delle reazioni mostrate e i loro composti il loro aspetto più notevole.
L'idea di classificare gli elementi è quella di affrontare correttamente le loro proprietà chimiche senza sviluppare una serie di regole e teorie per ciascuno di essi.
La sua classificazione periodica ha dato un quadro sistematico immensamente utile per correlarli in base a alcuni modelli molto semplici e logici.
Gli elementi sono sistematicamente disposti in righe e colonne con crescenti numeri atomici e lo spazio per le nuove scoperte è stato riservato.
Nel 1815 erano noti solo circa 30 elementi. Sebbene ci fossero molte informazioni disponibili su questi e sui loro composti, non c'era un ordine apparente.
Sono stati fatti diversi tentativi per trovare l'ordine, tuttavia, è stato difficile.
Scoprire le triadi di döbereiner
Lo scienziato Johann Wolfgang Döbereiner (1780-1849) ha fatto importanti risultati sulla regolarità numerica tra i pesi atomici degli elementi. Fu il primo a notare l'esistenza di diversi gruppi di tre elementi, che chiamava triadi, che mostravano somiglianze chimiche.
Questi elementi hanno rivelato un'importante relazione numerica, poiché una volta ordinata in base al loro peso equivalente o atomico, il peso dell'elemento centrale si è rivelato essere la media approssimativa dei due elementi rimanenti nella triade.
Può servirti: fosfato di sodio: struttura, proprietà, sintesi, usiNel 1817, Döbereiner scoprì che se alcuni elementi fossero combinati con ossigeno nei composti binari, una relazione numerica poteva essere discernente tra i pesi equivalenti di questi composti.
Pertanto, quando sono stati presi in considerazione il calcio, lo stronzio e gli ossidi di bario, il peso equivalente dell'ossido di stronzio era approssimativamente la media di ossido di calcio e ossido di bario. Si dice che i tre elementi in questione, stronzio, calcio e bario formino una triade.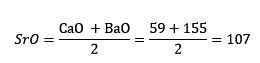
Sebbene Döbereiner abbia lavorato con pesos che erano stati dedotti da piccoli metodi sperimentali rigorosi, ma in vigore per il momento, i loro valori sono molto buoni.
L'osservazione di Döbereiner ha avuto un impatto limitato sul mondo chimico, ma poi è diventata molto influente. Al momento è considerato uno dei pionieri dello sviluppo del sistema periodico.
Dodici anni dopo, nel 1829, Döbereiner aggiunse tre nuove triadi, che sono mostrate di seguito:
Gruppo alogeno
Cloro, bromo e iodio hanno proprietà chimiche simili e formano una triade. Questi elementi sono metalli molto reattivi. Se sono elencati nell'ordine di aumento della massa relativa, sono nell'ordine di diminuire la reattività. Bromo ha una massa atomica intermedia tra cloro e iodio.

La massa atomica del bromo medio.
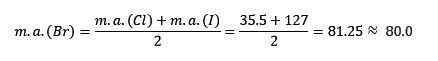
Il valore medio ottenuto è vicino alla massa atomica del bromo (BR).
Somiglianze nelle proprietà chimiche:
1. Sono tutti non metallici.
2. Tutti reagiscono con l'acqua per formare acidi (ad esempio, in: HCL, HBR, HF).
Può servirti: biodiesel: storia, proprietà, tipi, vantaggi, svantaggi3. Ognuno ha un Valencia di uno (ad esempio, in: HCL, HBR, HF).
4. Tutti reagiscono con i metalli alcalini per formare sali neutrali (ad esempio NaCl, Nabab, Nai)
Gruppo di metallo alcalino
Litio, sodio e potassio hanno proprietà chimiche simili e formano una triade. Questi elementi sono morbidi e leggeri ma molto reattivi.
Se sono elencati nell'ordine di aumentare la massa atomica relativa, sono anche in ordine per aumentare la reattività. Il sodio ha la massa atomica intermedia tra litio e potassio.

La massa atomica dell'elemento centrale di sodio (NA) è uguale alla media della massa atomica al litio (Li) e del potassio (K).
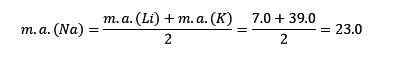
Somiglianze nelle proprietà chimiche:
1. Sono tutti metalli.
2. Tutti reagiscono con l'acqua per formare soluzioni alcaline e gas idrogeno.
3. Ognuno ha un Valencia de One (ad esempio, in: LICL, NaCl, KCL).
4. I suoi carbonati sono resistenti alla decomposizione termica.
Gruppo di calcogeni o anfumo
Sulphur, Selenio e Teluro hanno proprietà chimiche simili e formano una triade. Il selenio ha la massa atomica intermedia tra zolfo e teluro.

La massa atomica dell'elemento di selenio medio (SE) è uguale alle masse atomiche medie di zolfo (s) e teluro (TE).
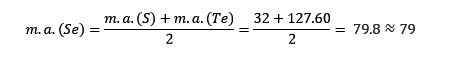
Ancora una volta, il valore medio ottenuto è vicino all'impasto atomico di selenio (SE).
Somiglianze nelle proprietà chimiche:
1. Le combinazioni con gli idrogeni di questi elementi provocano gas tossici.
2. Ognuno di questi elementi ha 6 elettroni di valenza.
3. Le qualità metalliche aumentano all'aumentare del numero atomico.
Döbereiner ha anche avvertito che per essere validi, le triadi hanno dovuto rivelare le relazioni chimiche tra gli elementi, nonché le relazioni numeriche.
Può servirti: clorato di potassio (KCLO3)D'altra parte, ha rifiutato di raggruppare il fluoruro insieme al cloro, bromo.
Era anche riluttante a considerare la comparsa di triadi tra elementi diversi, come azoto, carbonio e ossigeno, sebbene abbiano mostrato una relazione numerica triadica significativa.
Il lavoro di Döbereiner si è concentrato sulle relazioni tra gli elementi di una triade, ma non ha dato idea della relazione tra loro.
Basta dire che l'indagine di Döbereiner ha stabilito la nozione di triadi come un concetto potente, che molti altri prodotti chimici prenderebbero presto in considerazione.
In effetti, i triadi Döbereiner rappresentavano il primo passo per raggruppare gli elementi in colonne verticali all'interno della tabella periodica e quindi stabilire un sistema che spiega le proprietà chimiche e rivela le relazioni fisiche degli elementi.
Espansione delle triadi
Altre sostanze chimiche estese le triadi di Döbereiner per includere più dei tre elementi originali. Ad esempio, il fluoro è stato aggiunto alla parte superiore della triade contenente cloro, bromo e iodio.
Si sono verificate altre "triadi", come uno che conteneva ossigeno, zolfo, selenio e telurio. Ma non c'era un sistema per correlarli come un insieme.
Uno dei principali inconvenienti era che molte masse atomiche relative erano ancora sbagliate per il momento.
Riferimenti
- Johann Wolfgang Döbereiner. Recuperato dalla Britannica.com.
- Cos'è il gruppo 16 della tavola periodica? Come vengono utilizzati quegli elementi? Recuperato da Quora.com.

