Fondazione di reazione xantoproteica, procedura, uso
- 2460
- 640
- Lino Lombardi
IL Reazione xantoproteica È una procedura chimica utilizzata per determinare la presenza o l'assenza di aminoacidi aromatici, come la tirosina e il triptofano, che possono essere liberi o costituiti proteine solubili, peptidi o polipeptidi.
È stato anche usato per rilevare sostanze tossiche a livello di sangue che contengono un gruppo di beancenico nella sua struttura. Questo test è anche noto come reazione di Becher Xantoproteic.
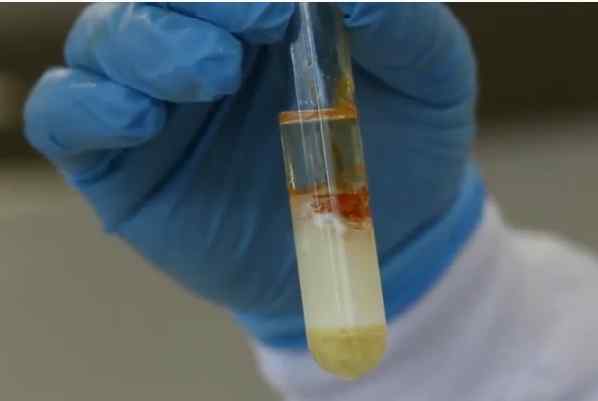
 Fonte di reazione xantoproteica positiva: tratto dal video: https: // youtu.BE/GZGMBW5W4WO
Fonte di reazione xantoproteica positiva: tratto dal video: https: // youtu.BE/GZGMBW5W4WO La reazione xantoproteica utilizza acido nitrico concentrato, calore e alcali neutralizzante. Se, quando neutralizzano la reazione, la soluzione di soluzione da giallo a arancione è considerata positiva. La colorazione osservata è dovuta alla formazione di composti di azoto derivati dalla nitrificazione dei gruppi benzenici.
Se è necessario quantificare la quantità di proteine totali, è necessario utilizzare altri metodi di determinazione delle proteine, come Biuret.
La reazione xantoproteica viene utilizzata principalmente quando vengono analizzate le sostanze a cui non è nota la sua composizione chimica. In generale, questa reazione fa parte di un insieme di test che aiuteranno a determinare la composizione chimica di una sostanza o estratto specifica. Ecco perché, è ampiamente utilizzato dai ricercatori.
D'altra parte, la reazione xantoproteica di Becher viene utilizzata per rilevare sostanze fenoliche e indoli nel sangue, essendo possibile prevedere la comparsa di nefropatia, prima che aumenti altri più parametri.
[TOC]
Base
La reazione rileva sostanzialmente la presenza del gruppo benzenico, sia negli aminoacidi, come nelle proteine e nei peptidi. L'acido nitrico agisce sull'anello bencenico aminoacido che lo possiede, formando nitrocomposioni fenoliche.
La reazione necessita di calore da eseguire, di solito si forma un precipitato che nuvole il mezzo, rendendolo lattigio. Il precipitato può essere bianco o giallo. Infine, richiede una fase di alcalizzazione che accentua il colore. Per questo, viene utilizzata una base come 40% o idrossido di sodio ammoniaca.
La reazione sarà interpretata come positiva se si osserva una forte colorazione gialla durante il riscaldamento scuro o il processo arancione alcalizzando la reazione. Gli aminoacidi rilevati sono principalmente tirosina e triptofano.
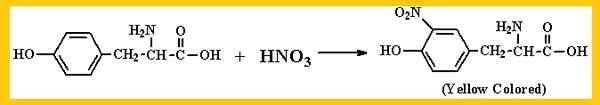 Reazione xantoproteica. Fonte: http: // Esteroisomeras.Blogspot.com/2013/06/caratterizzazione delle proteine.Html
Reazione xantoproteica. Fonte: http: // Esteroisomeras.Blogspot.com/2013/06/caratterizzazione delle proteine.Html Nel caso della fenilalanina, sebbene si tratti di un aminoacidi aromatici, il nucleo di benzene di questo aminoacido è difficile da essere nitriti in una semplice reazione, quindi emetterà o una reazione negativamente o debolmente positiva.
Può servirti: polarità (chimica): cosa è, definizione, esempiIn generale, il test xantoproteico può essere integrato con il test Hopkins-Cole, che serve a identificare specificamente il triptofano. Se il test xantoproteico è positivo e quello di Hopkins-Cole è negativo, la presenza di triptofano viene scartata in quella soluzione, portando alla presenza principalmente di tirosina. Allo stesso modo, può anche essere integrato con la reazione di Millon per il rilevamento della tirosina, tra le altre cose.
Questa reazione può essere utilizzata anche su campioni di sangue, plasma o siero invariato per la diagnosi di uremia o insufficienza renale. In questo caso, ciò che viene richiesto è il rilevamento di sostanze tossiche (fenoliche e indoli) prodotte da marciume intestinale.
Queste sostanze possiedono il gruppo benzenico e quindi danno una reazione xantoproteica positiva, sebbene le sostanze reazionarie non siano né un aminoacido, né una proteina.
Procedura
- Reazione xantoproteica per il rilevamento di aminoacidi con gruppi aromatici
Posizionare 1 ml del campione problematico in un tubo di prova pulito e asciutto.
-Aggiungi 0,5 ml di acido nitrico concentrato.
-Incubare la miscela in un bagno di 70 ° C per 2 minuti. Preparare in precedenza il bagno Maria alla temperatura sopra menzionata.
-Quando prendi il tubo dal bagno di Maria, è possibile osservare che la soluzione è diventata lattiginosa e ha preso un po 'di colorazione bianca giallastra.
-La soluzione viene raffreddata facendo cadere l'acqua fredda alla base del tubo.
-La preparazione è presunta lentamente (caduta per goccia) una soluzione di idrossido di sodio al 40% fino a quando non c'è uno shock a colori.
-Se il test è positivo, si formerà un anello arancione scuro nell'interfaccia liquida.
-Se la reazione è negativa non ci sarà formazione di colore.
- Reazione xantoproteica per rilevare sostanze fenoliche e indoli nel sangue
-Distribuire 5 cc di acido tricloroacetico al 20% su 5 cc di sangue venoso, plasma o siero, quest'ultimo è il più indicato. Mescola bene e filtra.
Può servirti: acido nitrico (HNO3)-2 cc del filtro vengono presi e miscelati con 0,5 cc di acido nitrico. Quindi viene riscaldato ad ebollizione, poiché questo il tubo viene posizionato direttamente sulla fiamma dell'accendino per 30 secondi. Si raffredda con acqua e aggiungi 1,5 di cloruro di sodio al 33%.
È interpretato come segue:
-Risultato negativo: colore giallastro.
-Risultato positivo (+) limone giallo.
-(++) Giallo oro.
-(+++) giallo scuro a marrone
Può anche essere interpretato usando una scala colorimetrica referenziale di Auenrieth, costituita da varie concentrazioni di potassio bicromato. Questo è preparato in diluizioni di 10 su 10 da una soluzione madre dello 0,03874%. Ogni tubo rappresenta una percentuale.
Scale di interpretazione
Esistono due scale di interpretazione chiamate antiche e moderne. I valori normali sono:
Old Table: tra il 75 e l'85%
Tavolo moderno: tra il 15 e il 25%
Se il colore del tubo problematico è nel mezzo di due motivi, viene effettuata una media tra le due misure.
La soluzione di pattern di dicromato di potassio viene preparata come segue: 7 viene misurata.9 ml di dicromato di potassio a 10 N ed è a filo fino a 100 ml in una palla di Aggorado. Per diluizioni viene seguito come mostrato nella tabella colorimetrica di Autenrieth.
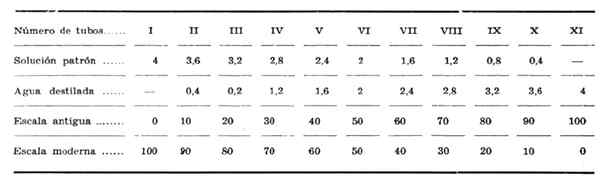 Tabella colorimetrica di Autenrieth. Fonte: Vásquez a. Reazione xantoproteica. Rivista clinica spagnola. 1949; 35 (5): 326-327. Disponibile su: Elsevier
Tabella colorimetrica di Autenrieth. Fonte: Vásquez a. Reazione xantoproteica. Rivista clinica spagnola. 1949; 35 (5): 326-327. Disponibile su: Elsevier Utilizzo
L'uso della reazione xantoproteica fa parte di un insieme di test biochimici che aiutano a conoscere la composizione chimica di una sostanza sconosciuta. Questo test contribuisce all'analisi chimica la rilevazione di proteine contenenti gruppi benzenici nella loro struttura.
Questa reazione è ampiamente utilizzata dai ricercatori in vari studi di sostanze.
In questo senso, Vásquez-Jorge e collaboratori hanno usato questa e altre reazioni per studiare il contenuto proteico dei fluidi estratti dall'ostione di mangrovie (Crassostrea rizophore).
Allo stesso modo, Rojas e collaboratori (2009), hanno usato una serie di test, tra cui la reazione xantoproteica, per analizzare i glycomacropéptidi nei precipitati di Lactosueros de Ricotta.
D'altra parte, la reazione xantoproteica di Becher è stata modificata da Volhard da utilizzare per altri scopi. In questo caso, per il rilevamento di sostanze fenoliche e indoli che possono essere sollevate molto prima (settimane o mesi) che i livelli di urea e azoto residuo nel sangue sono aumentati.
Può servirti: cerio: struttura, proprietà, ottenimento, usiQuesti rifiuti tossici sono formati dal marciume intestinale degli alimenti.
Queste sostanze si accumulano nel sangue quando non sono eliminate correttamente, quindi un test xantoproteico positivo può prevedere la pronta istituzione di insufficienza renale stessa o uno stato di uremia.
Secondo l'intensità del colore, puoi determinare quanto è avanzato. In questo caso il test è quantitativo.
Nelle persone sane questo test dà un leggero colore giallo, corrispondente ai livelli normali di triptofano e tirosina che possono essere nel sangue.
Mentre, nei pazienti renali, la reazione xantoproteica dà fortemente positivo a causa della presenza delle seguenti sostanze: fenolo, indolo, paracresolo, ossi aromatici, tra gli altri.
Precauzioni
Questo test deve essere eseguito da professionisti qualificati. Tutti gli standard di biosicurezza dovrebbero essere considerati, perché i reagenti utilizzati sono acidi e basi corrosive.
Se, per caso, alcune gocce di acido nitrico sulla pelle o sulle unghie cadono, diventeranno gialle, poiché entrambe le strutture contengono proteine. Inoltre, sulla pelle e sulle mucous di cause gravi ustioni.
Se si verifica un contatto con la pelle, il protocollo da seguire deve essere per lavare immediatamente l'area con acqua e sapone per circa 20 minuti.
Se schizzi gli occhi, devi lavarti con molta acqua fresca, cercando di tenere gli occhi aperti.
Riferimenti
- "Reazione Xantoproteica" Wikipedia, Enciclopedia gratuita. 2 settembre 2019, 17:49 UTC. 21 ottobre 2019, 20:31 Wikipedia.org/
- Vásquez-Jorge e, Guerra-Molina L, Quintana-Tamayo J, Ramírez-Arzuaga J, Fernando-Ballesteros R, Vásquez-Jorge e. Caratterizzazione fisico -chimica e contenuto di proteine di estratti fluidi di ostizione di mangrovie (Crassostrea Rizophore). Chimica cubana, 2014; 26 (1): 66-74. Disponibile in Redalyc.
- Rojas E, Valbuena E, Torres G, García A, Piñero M, Galindo L. Isolamento e prestazioni del GMP mediante precipitazione del lattosuero con acido tricloroacetico. Scienziato. (Maracaibo) 2009; 19 (3): 295-302. Disponibile su: VE.Scielo.
- Vásquez a. Reazione xantoproteica. Rivista clinica spagnola. 1949; 35 (5): 326-327. Disponibile su: Elsevier
- Gálvez I, Gárate o. Reazioni di Becher e Andrewes nella chirurgia urinaria. Servizio di urologia dell'ospedale spagnolo. Rivista Argentina di Urologia 395-404

