Cos'è la corrosione e come evitarlo?

- 2289
- 548
- Lino Lombardi
 Metallo corrido
Metallo corrido Cos'è la corrosione?
Sapere Come evitare la corrosione È importante sapere cos'è la corrosione e perché si verifica. Il processo naturale si chiama corrosione in cui un metallo si deteriora gradualmente a causa di reazioni elettrochimiche (o chimiche) con il suo ambiente.
Queste reazioni fanno apparire i metalli raffinati. La corrosione si verifica anche in materiali non metallici come ceramica e polimeri, ma è diverso e di solito è chiamato degrado.
La corrosione è un processo nemico dell'essere umano, poiché questi danni degradano i materiali, cambiano la loro colorazione e indeboliscono, aumentando la possibilità di rottura e aumentando i costi per riparazione e sostituita di essi.
Per questo motivo ci sono interi campi nella scienza dei materiali dedicati alla prevenzione di questo fenomeno, come l'ingegneria della corrosione. I metodi per la prevenzione della corrosione sono vari e dipenderanno dai materiali interessati.
Metodi per evitare la corrosione
Innanzitutto, si dovrebbe prendere in considerazione che non tutti i metalli funzionano alla stessa velocità e alcuni hanno la peculiarità di non essere affatto corrode naturalmente, come nel caso di acciaio inossidabile, oro e platino.
Ciò accade perché ci sono materiali per i quali la corrosione è termodinamicamente sfavorevole (cioè non raggiungono una maggiore stabilità con i processi che li portano a questo) o perché hanno una reazione cinetica così lenta che gli effetti della corrosione richiedono tempo per mostrare.
Può servirti: blu bromotimolAnche così, per gli elementi in esecuzione ci sono una serie di metodi per prevenire questo processo naturale e dare loro più vita:
Zincato
È il metodo di prevenzione della corrosione in cui è coperta una lega di ferro e acciaio con un sottile strato di zinco. L'obiettivo di questo metodo è quello di rendere gli atomi di zinco del rivestimento reagire con le molecole d'aria, ossidando e ritardando la corrosione del pezzo che coprono.
Questa metodologia rende lo zinco un anodo galvanico o un anodo di sacrificio, facendolo esplorare al degrado della corrosione per salvare un materiale più prezioso.
Il zincato può essere ottenuto mediante immersione delle parti metalliche in zinco fuso ad alte temperature, nonché negli strati più sottili che si ottengono con elettrogalvanizzazione.
Quest'ultimo è la metodologia che protegge di più, poiché lo zinco è collegato al metallo dai processi elettrochimici e non solo da processi meccanici come nell'immersione.
Dipinti e copertura
L'applicazione di dipinti, piastre di metallo e smalti è un altro modo per aggiungere uno strato protettivo ai metalli di pronione della corrosione. Queste sostanze o strati generano una barriera di materiale anticorrosivo che viene portato tra l'ambiente dannoso e il materiale strutturale.
Altre coperture hanno proprietà specifiche che le rendono corrosione o inibitori anticorrosivi. Questi vengono aggiunti prima a liquidi o gas, quindi vengono aggiunti sotto forma di metallo sul metallo.
Questi composti chimici sono usati notevolmente nel settore, specialmente nei tubi che trasportano liquidi; Inoltre, possono essere aggiunti all'acqua e ai refrigeranti per garantire che non generino la corrosione nell'attrezzatura e nei tubi attraverso i quali passano.
Può servirti: principio di AufbauAnodizzazione
È una procedura di passivazione elettrolitica; Cioè, il processo attraverso il quale si forma un film un po 'inerte sulla superficie di un elemento metallico. Questo processo viene utilizzato per aumentare lo spessore dello strato di ossido naturale che questo materiale ha sulla sua superficie.
Questo processo ha il grande vantaggio non solo di aggiungere protezione contro la corrosione e lo sfregamento, ma fornisce anche una maggiore adesione per gli strati di vernice e colla rispetto al materiale scoperto.
Nonostante abbia subito cambiamenti e evoluzioni nel tempo, questo processo viene comunemente effettuato introducendo un oggetto in alluminio in una soluzione elettrolitica e passando una corrente continua attraverso questo.
Questa corrente farà rilasciare l'anodo in alluminio a rilasciare idrogeno e ossigeno, generando ossido di alluminio che lo unirà per aumentare lo spessore del suo strato superficiale.
L'anodizzazione genera cambiamenti nella consistenza microscopica della superficie e nella struttura cristallina del metallo, causando la generazione di un'alta porosità nello stesso.
Pertanto, nonostante il miglioramento della resistenza e della resistenza alla corrosione dei metalli, può anche renderlo più fragile, oltre a ridurre la sua resistenza alle alte temperature.
BIIPEL
I bipel sono gruppi di microrganismi che si legano sotto forma di uno strato su una superficie, si comportano come un idrogel ma rappresentano ancora una comunità vivente di batteri o altri microrganismi.
Sebbene queste formazioni siano generalmente associate alla corrosione, negli ultimi anni c'è stato uno sviluppo nell'uso di biofilm batterici per proteggere i metalli in ambienti altamente corrosivi.
Può servirti: relazione di chimica con altre scienzeInoltre, sono stati scoperti biofilm con proprietà antimicrobiche, che fermano gli effetti dei batteri riducono il solfato.
Currenti stampate
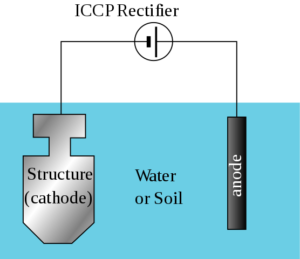
In quelle strutture molto grandi o in cui la resistività degli elettroliti è alta, gli anodi galvanici non possono generare abbastanza corrente per proteggere l'intera superficie, quindi un sistema di protezione catodica viene utilizzato dalle correnti stampate.
Questi sistemi sono costituiti da anodi collegati a una fonte di alimentazione a corrente continua, principalmente un trasformatore-recipiente collegato a una sorgente di corrente alternata.
Questo metodo viene utilizzato principalmente nei mercantili e in altre navi, che richiedono un alto livello di protezione su una superficie più ampia della loro struttura, come eliche, rudges e altri pezzi da cui dipende la navigazione.
Cambiamenti in condizioni ambientali
Infine, il tasso di corrosione può fermare o ridurre con l'alterazione delle condizioni ambientali in cui si trova il materiale metallico.
L'umidità e il contenuto di zolfo, cloruri e ossigeno nei liquidi e nei gas devono essere mantenuti a bassi livelli per aumentare l'aspettativa di vita di un materiale e usare meno soluzione salina e/o acqua dura ha un effetto positivo.
Riferimenti
- Wikipedia. (S.F.). Corrosione. Ottenuto da in.Wikipedia.org
- Equilibrio, t. (S.F.). Protezione da corrosione per i metalli. Ottenuto dal bilanciamento.com
- Eoncoat. (S.F.). Metodi di prevenzione della corrosione. Ottenuto da eoncoat.com
- MetalSuperMarkets. (S.F.). Come prevenire la corrosione. Ottenuto dai metalsupermarkets.com
- Corrosionpedia. (S.F.). Protezione catodica di corrente stampata (ICCP). Ottenuto da Corrosionpedia.com