Metalli
- 3681
- 16
- Baldassarre Ross
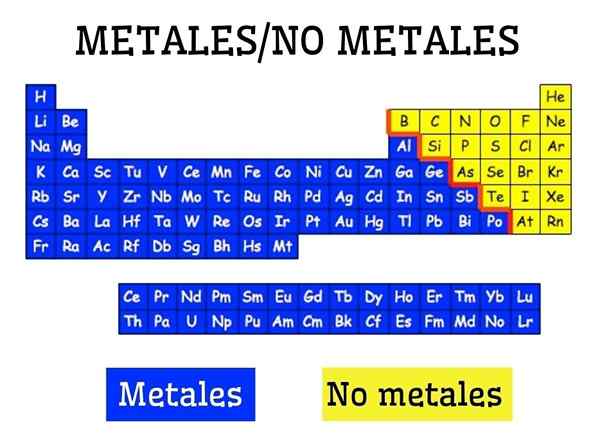
 Metalli e non metalli nella tabella periodica degli elementi
Metalli e non metalli nella tabella periodica degli elementi Cosa sono i metalli?
I metalli sono formati da un gruppo di elementi che si trovano sul lato sinistro, ad eccezione dell'idrogeno non metallico, della tavola periodica. I metalli costituiscono circa il 75 % degli elementi chimici, quindi si può affermare che gran parte della natura è metallica.
I metalli che l'uomo inizialmente perseguiti in preistoria erano i seguenti: oro, argento, rame, stagno, piombo e ferro. Ciò era dovuto al fatto che erano nativi o la facilità della loro elaborazione per eseguire oggetti di utilità.
Sembra una questione di magia che di molte rocce e minerali possano essere estratti corpi brillanti e argentati (con alcune importanti ed eccezionali eccezioni). Tale è il caso di bauxite e alluminio, le cui argilla si rompono questo metallo ridotto in piastre o carte d'argento.
I metalli sono il quadro delle industrie; Il loro cablaggio, reattori, unità, contenitori, tutti in un modo o nell'altro sono composti da metalli e le loro leghe.
Con i metalli sono state realizzate le prime monete, armi, strumenti, armature e quindi utilizzate nei produttori di veicoli, biciclette, navi, aeroplani, computer, tra gli altri oggetti indispensabili nella vita moderna.
Storia
Age di rame
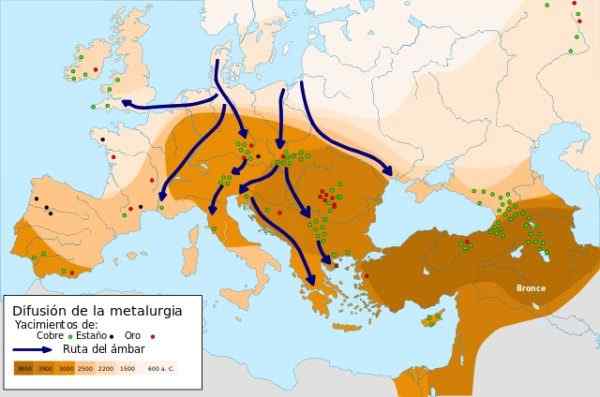 Espansione della metallurgia - Fonte: diffusione metallurgica.SVG sotto la Creative Commons Attribution-Compartirigual 4 Licenza 4.0 internazionale
Espansione della metallurgia - Fonte: diffusione metallurgica.SVG sotto la Creative Commons Attribution-Compartirigual 4 Licenza 4.0 internazionale In 9000 a.C. I primi oggetti metallici di rame forgiati nel Vicino Oriente furono elaborati, quando l'uomo scoprì che quando il rame stava martellando aumentò la sua forza e la sua resistenza, usandolo per la produzione di coltelli. Questa è l'età del rame.
È stato scoperto che il rame poteva essere ottenuto attraverso il riscaldamento di minerali blu, come la Corvellita e la malachite (da 4000-3000 a.C.).
Il periodo calcolitico è un periodo di tempo che precede l'età del bronzo, corrispondente a 5000-3000 a.C. L'uomo iniziò a sperimentare la fusione e la fonderia di rame, per ottenere il rame forgiato dall'ossido di rame.
Età in bronzo (3000-1500 a.C.)
 Materiali dell'età del bronzo - Fonte: Gaguilella sotto l'attribuzione Creative Commons -Shareigual 4 Licenza 4.0 internazionale.
Materiali dell'età del bronzo - Fonte: Gaguilella sotto l'attribuzione Creative Commons -Shareigual 4 Licenza 4.0 internazionale. L'uomo iniziò accidentalmente l'elaborazione di leghe, inizialmente di rame e arsenico, e poi con rame e stagno per ottenere il bronzo nel Vicino Oriente.
Gli articoli in bronzo, corrispondenti a questo momento, avevano l'87 % di rame, 11 % di stagno e piccole quantità di ferro, arsenico, nichel, piombo e antimonio.
Age di ferro (700 a.C.)
L'uomo ha usato la sua esperienza nella produzione di rame forgiato per la produzione di ferro battuto nel Vicino Oriente. In quello stesso periodo di tempo vi fu la granulazione della polvere di Etrusco, Italia.
La prima produzione di acciaio conosciuta, una lega di ferro e carbonio, si è manifestata in pezzi di metallo in un sito archeologico in Anatolia (dal 1800 al 1800.C.)
Può servirti: gravimetria: analisi gravimetrica, metodi, usi ed esempiVerso 1122 d.C., In una data e un luogo sconosciuti, viene introdotta la ghisa. Nel 1440 d.C. La grande campana di Pechino è prodotta, la Cina. Quasi tre secoli dopo, nel 1709 d.C., La ghisa viene prodotta usando la coke come materiale combustibile.
Nel 1779 il ghisa in Inghilterra fu usato come materiale architettonico. Nel 1855, Henry Bessenir usò Arrabio come materia prima per ottenere acciaio morbido. Il brevetto inglese Clark and Wood (1872) una lega, attualmente considerata in acciaio inossidabile.
Proprietà fisiche dei metalli
 Il bronzo di queste antiche campane dimostra l'utilità dei metalli per scopi ornamentali o religiosi. Fonte: pxhere.
Il bronzo di queste antiche campane dimostra l'utilità dei metalli per scopi ornamentali o religiosi. Fonte: pxhere. Tra alcune proprietà fisiche dei metalli abbiamo:
-I metalli sono brillanti e sono in grado di riflettere la luce.
-In generale, sono buoni conduttori di elettricità e calore.
-Hanno elevati punti di fusione e ebollizione.
-Sono malleabili, cioè possono essere martellati per produrre fogli bassi spessi.

-Sono duttili, con loro puoi produrre fili o fibre di pochissimo diametro.
-Sono presentati in uno stato solido, ad eccezione del mercurio che a temperatura ambiente è in stato liquido e il gallio, che si scioglie semplicemente dal serraggio tra le mani nelle mani. Nella seguente immagine puoi vedere un contenitore di mercurio:

-Sono corpi opachi, i loro fogli sottili non sono attraversati dalla luce.
-Hanno una grande durezza, ad eccezione del sodio e del potassio che possono essere tagliati da un coltello.
-Hanno un'alta densità, essendo l'osmio e l'iridio del più alto e il litio della più bassa densità.
Proprietà chimiche dei metalli
Tra alcune delle proprietà chimiche dei metalli che abbiamo:
-Tendono a perdere elettroni e formare cationi metallici, mN+, dove n indica il suo numero di ossidazione, che solo per i metalli alcalini e alcalisti coincide con il suo numero di valenza.
-Le sue elettronegatività sono basse.
-Corrono e subiscono danni all'ossidazione.
-Formano ossidi di base quando reagiscono con ossigeno. Questi ossidi se combinati con acqua formano idrossidi metallici. Gli ossidi metallici reagiscono con acidi per formare sali e acqua.
-Sono buoni agenti riducenti, poiché producono i loro elettroni.
Tipi di metalli
I metalli sono classificati come i seguenti: alcalina, trial alcalina, post-transizionale, transizione e cosiddetta.
Metalli alcalini

Di solito non si trovano liberi in natura perché si ossidano facilmente. Avere una S suborbitale1 Nel suo strato orbitale esterno, quindi hanno uno stato di ossidazione +1. Sono metalli che reagiscono esotermicamente con l'acqua e stanno riducendo fortemente.
Metalli alcalini-térreos
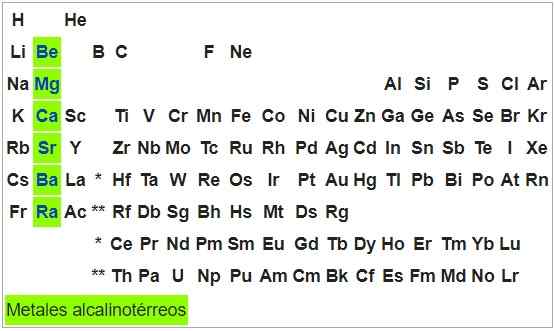
Sono metalli malleabili e duttili. Gli atomi degli elementi di questo gruppo hanno una configurazione S2, Quindi possono produrre due elettroni e il loro stato di ossidazione è +2. Con l'eccezione del berillio, sono ossidabili per l'esposizione all'aria.
Può servirti: allotropi di carbonioMetalli post -trattamento
Sono metalli del blocco P così chiamato, situato tra metalli di transizione e metalloidi nella tabella periodica.
Gli elementi del gruppo 3 hanno stati di ossidazione +1 e +3 come i più comuni, sebbene l'alluminio presenta solo lo stato di ossidazione +3. Fa anche parte dei metalli post -transizionali situati nei gruppi 14 e 15.
Metalli di transizione d
Formano un gruppo tra elementi di formazione base e formatori acidi. Gli orbitali atomici D e F sono incompleti e vengono riempiti. Sebbene il termine metalli di transizione si riferisca ai metalli di transizione d.
I metalli di transizione hanno più di uno stato di ossidazione. Hanno punti di fusione e ebollizione più alti rispetto ad altri gruppi metallici. Transition Metals è un gruppo di metallo molto eterogeneo che include, tra gli altri, ferro, cromo, argento, ecc.
Terra rara
 Minerale delle terre rare
Minerale delle terre rare Questo gruppo di metalli è composto da elementi scandio e ititrio e dagli elementi della serie di Lantanides e Actinids. Il termine "terre rara" si riferisce al fatto che non si trovano in natura negli stati puri e sono attaccabili dagli acidi.
Usi/applicazioni dei metalli
Metalli alcalini
Il litio viene usato come trasferimento di calore significa in alcuni reattori nucleari. È usato in alcune batterie a secco e accumulatori di scarso peso. Il bromuro di cloruro e litio sono composti igroscopici utilizzati nei processi di essiccazione e condizionamento dell'aria industriale.
Il sodio è usato in metallurgia in metallo, come titanio e zirconio. È usato nell'illuminazione pubblica nelle lampade ad arco di sodio. Il cloruro di sodio (NaCl) viene utilizzato come sapore alimentare e conservazione della carne.
Metalli alcalineter
Il magnesio è stato usato in fotografia come luce flash e fuochi d'artificio. Il bario è un componente delle leghe utilizzate in candele a causa della facilità dell'elemento per emettere elettroni. I sali di bario sono usati per limitare il danno causato da raggi x nelle piastre del tratto gastrointestinale.
Il calcio viene utilizzato per eliminare le impurità disciolte nei metalli fusi e nell'eliminazione dei gas residui nei tubi a vuoto. Fa parte dell'intonaco, materiale utilizzato nella costruzione e nel trattamento delle fratture ossee.
Metalli post -trattamento
Alluminio perché è un metallo chiaro viene utilizzato nella costruzione di aeroplani e vasi. Viene anche utilizzato nell'elaborazione di numerosi utensili da cucina. È usato come materia prima nella produzione di deodoranti che limitano la sudorazione.
Può servirti: soluzioni percentualiIl gallio viene utilizzato nei transistor e nei termometri per le alte temperature. L'isotopo 67GA è usato in medicina nel trattamento di alcuni melanomi. Il piombo viene utilizzato nella costruzione di batterie e in protezione contro le radiazioni ionizzanti.
Metalli di transizione
Il rame viene utilizzato nei tubi dell'approvvigionamento idrico, nei frigoriferi e nei sistemi di condizionamento dell'aria. Viene anche usato come parte del meccanismo di dissipazione del calore dei computer. È usato nella conduzione della corrente elettrica, negli elettromagneti e nella colorazione del vetro.
Il nichel viene utilizzato nell'elaborazione di acciaio inossidabile, nonché corde di chitarra e batterie ricaricabili. È anche usato in galvanoplastica nella protezione dei metalli. Viene utilizzato nelle leghe che si trovano in alcune parti di veicoli, come valvole, cuscinetti e freni.
Il nichel è stato usato, per molto tempo nell'elaborazione delle monete.
Lo zinco viene utilizzato nella protezione dei metalli a corrosione, nella produzione di ottoni. L'ossido di zinco e il solfato di zinco sono utilizzati nella produzione di piastre utilizzate in tetti, grondaie e downspout.
Il cromo viene utilizzato nella protezione della corrosione dei metalli e le forniture brillano. È usato come catalizzatore nella reazione di sintesi dell'ammoniaca (NH3). L'ossido di cromo viene utilizzato nella protezione del legno.
Terra rara
Lo scandio è usato in alluminio in alluminio per componenti aerospaziali. È un additivo nelle lampade a vapore di mercurio.
Il Lantano è usato in vetro resistente e resistente alcalino. Inoltre, viene utilizzato nella produzione di lenti delle telecamere e come fluidi catalizzatori per le raffinerie di petrolio.
Cerio è usato come agente chimico. Inoltre, viene utilizzato per la fornitura di un vetro giallo e una colorazione in ceramica, nonché per catalizzatori per i forni auto -impiegati.
Esempi di elementi metallici
Alcalino
Sodio (NA), potassio (K), Cesio (CS), Litio (Li) e Rubidium (Ru).
Alcalino-terraos
Berillio (BE), magnesio (mg), calcio (CA), stronzio (MR), bario (BA) e radio (RA).
Post -Transitional
Alluminio (AL), Gallio (GA), Indian (IN), Talio (TL), Tin (SN) e Lead (PB).
Transitorio
Titanio (Ti), Vanadio (V), Chrome (Cr), Manganese (MN), Iron (Faith), Cobalt (CO), Nickel (Ni), Copper (Cuinc), Zinco (Zn), Zirconio (ZR), Niobio (NB), Molybdenum (MO), Paladio (PD), Silver (Ag), Volframium (W), Renio (Re), Osmio (OS), Iridido (IR),
Platinum (Pt), Gold (Au) e Mercury (Hg).
Terra rara
Scandio (SC), itrio (Y), Lantano (LA), Cerio (CE), Praseodimio (PR), Neodimio (ND), Samarium (SM), Europio (UE), Gadolinio (GD), Holmio (HO), Erbio (ER), Tulio (TM), Iterbio (YB) e Lutcita (Lu).
Riferimenti
- Whitten, Davis, Peck e Stanley. (2008). Chimica. (8 ° ed.). Apprendimento del Cengage.
- SHIVER & ATKINS. (2008). Chimica inorganica. (Quarta edizione). Mc Graw Hill.
- Helmestine, Anne Marie, PH.D. (5 ottobre 2019). Metalli contro non metalli. Recuperato da: Thoughtco.com
- Metalli e loro proprietà-fisiche e chimiche. [PDF]. Recuperato da: CSUN.Edu
- Jonathan Master. (2019). 18 diversi tipi di metallo (fatti e usi). Recuperato da: makeitfmemtal.com

