Ipoclorito di sodio (Naclo)
- 2359
- 752
- Ruth Cattaneo
Spieghiamo cos'è l'ipoclorito di sodio, le sue proprietà, la sintesi e le applicazioni
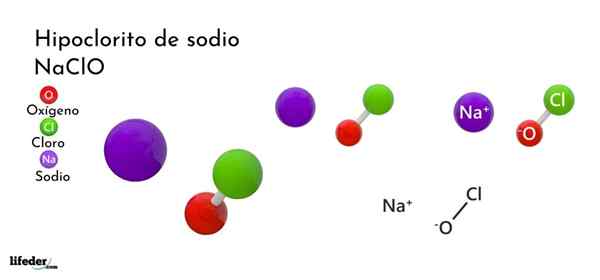
 Formula e struttura dell'ipoclorito di sodio
Formula e struttura dell'ipoclorito di sodio Cos'è l'ipoclorito di sodio?
Lui Ipoclorito di sodio (Naclo) è un sale ternario e inorganico di sodio. Commercialmente si ottiene come soluzioni acquose ed è l'agente attivo di questi prodotti nazionali e industriali. Queste soluzioni sono note con i nomi di cloro più bianco, soda più bianchi, più bianchi o, ancora più raffinato, liquore di giavello.
Nell'acqua l'ipoclorito di sodio mostra le stesse proprietà ossidanti del cloro gassoso, quindi una soluzione di questo sale è equivalente al trasporto di quel composto all'interno di una bottiglia di plastica. In effetti, il cloro disponibile in questi contenitori è un indicatore della concentrazione e della potenza di sbiancamento della soluzione di ipoclorito di sodio.
Questo sale ternario in acqua può essere considerato una semplice soluzione acquosa di cloro; Tuttavia, ci sono anche altre forme disponibili, come solide nel caso dell'ipoclorito di calcio e del cloro liquido. I tre hanno lo stesso potere ossidante e i loro usi dipendono da variabili come comfort, prestazioni o tempo.
Formula
La formula chimica dell'ipoclorito di sodio è NaClo. È costituito da una nazione+ E un anione clo-. Na ioni+ Sentono l'attrazione elettrostatica per i clo ioni-, Quest'ultimo adotta una struttura tetraedrica con un'ibridazione SP3.
La formula indica la proporzione di ioni nello stato di anidride, che è uguale a 1: 1. Tuttavia, si applica solo per l'anidride.
Nel caso dell'ipoclorito di sodio idratato, una delle forme più stabili per questo sale, la formula chimica è NaClo · 5h2O.
Dov'è l'ipoclorito di sodio?
Il NaClo è un prodotto sintetico e, a causa della sua reattività, si trova solo nelle regioni locali in cui viene utilizzato, specialmente nelle acque reflue, nei terreni o persino nelle emanazioni dell'acqua potabile.
Nel corpo umano abbondava gli ioni cloruro, che potrebbero partecipare alle reazioni redox che producono ipoclorito di sodio all'interno dell'organismo.
Può servirti: ossidi di metalloSintesi
Nel corso della storia, NaClo è stato preparato per diversi metodi. Il più semplice è costituito da una soluzione di cloro in acqua o soluzioni NA2Co3 Quella versione co2 Mediante azione dell'acido ipocloroso (HCLO).
Altri metodi usano la salamoia come materia prima attraverso un processo elettrolitico. Sotto efficiente agitazione meccanica, il CL2 e il NaOH generato da NaCl e Water Reage e diventa NaClo:
Cl2(g) + 2Naoh (aq) => NaClo + NaCl + H2O + Q (calore)
Oggi il processo di prostituta produce questo composto su grandi scale, che consiste in una versione migliorata del metodo precedente descritto.
Usi/applicazioni di clorito di sodio
 Una delle principali applicazioni dell'ipoclorito di sodio è quella di candeggiare gli indumenti
Una delle principali applicazioni dell'ipoclorito di sodio è quella di candeggiare gli indumenti Le più comuni applicazioni di ipoclorito di sodio sono:
- L'ipoclorito di sodio è usato come agente sbiancante nei tessuti, nei detergenti che lo incorporano e nell'industria cartacea.
- Il suo uso come agente battericida e disinfettante è molto ampio, usando la purificazione dell'acqua e il trattamento delle acque reflue.
- È nota la sua utilità nel disinfettare l'attrezzatura utilizzata nella preparazione degli alimenti e nella lavorazione della frutta e verdura. Viene anche usato con la stessa funzione disinfettante nella produzione di funghi, bovini, maiali e pollame.
- L'ipoclorito di sodio viene utilizzato nell'industria petrolifera nella fase di raffinazione.
- In casa la capacità di sbiancamento dell'ipoclorito di sodio viene utilizzata per lavare i vestiti bianchi e l'azione disinfettante per pulire bagni, pavimenti, ecc.
- L'ipoclorito di sodio è usato nella terapia endodontica, in particolare nel trattamento della radice del dente. Questo trattamento utilizza la soluzione Dakin (clone allo 0,5 %) che preserva il tessuto dentale vitale durante la dissoluzione del tessuto necrotico.
Proprietà dell'ipoclorito di sodio
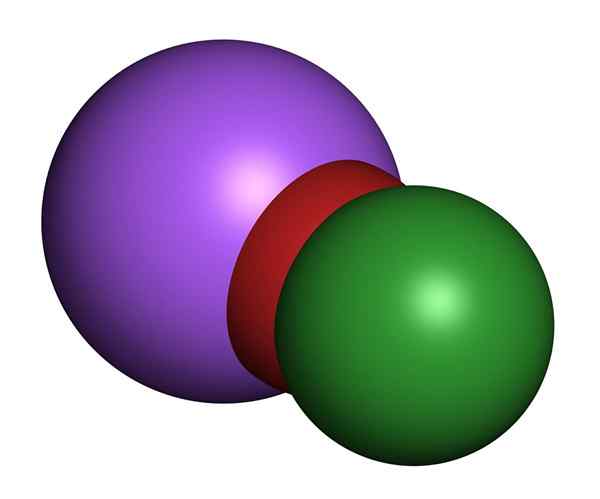 Modello di ipoclorito di sodio 3D. Cloro (verde), ossigeno (rosso), sodio (viola)
Modello di ipoclorito di sodio 3D. Cloro (verde), ossigeno (rosso), sodio (viola) Le soluzioni di ipoclorito di sodio a temperatura ambiente sono incolori e hanno un odore di cloro dolce. Le proprietà fisiche variano a seconda delle concentrazioni di sale disciolte in acqua. Tutti hanno colorazioni gialle.
Attraverso le tecniche di cristallizzazione, queste soluzioni ottengono il NaClo solido · 5h2Oppure, i cui cristalli sono verdi.
Questo sale idratato ha un peso molecolare approssimativo di 164 g/mol, una densità di 1,11 g/ml, è molto solubile in acqua e si decompone a 101 ºC. Il NaClo · 5h2O è anche sensibile alle stesse reazioni dell'anidride.
Perché il sale è pentaidrato? Mentre il Naclo si cristallizza nel suo ambiente acquoso, le molecole d'acqua avvolgono gli ioni in una sfera acquosa.
Si può pensare che tre di queste molecole interagiscono con le coppie di elettroni non condivise del CL: un ponte idrogeno con l'O e l'ultimo è attratto dal NA.
Tuttavia, sono gli studi incentrati sulla struttura cristallina di questo solido che hanno la vera risposta a questa domanda.
Equilibrio acquoso
L'anione clo- Partecipa al seguente equilibrio di idrolisi:
HCLO (AC) + H2O (l) clo-(AC) + H+(AC)
Se l'acidità della soluzione aumenta, l'equilibrio si sposta a sinistra, producendo HCLO.
Questo acido è ancora più instabile dell'ipoclorito e, quindi, la decomposizione riduce la concentrazione dell'agente attivo. Se il pH è di base (maggiore di 11), garantisce l'esistenza del CLO- e il tempo della vita del prodotto.
Tuttavia, l'eccessiva alcalinità innesca altri problemi nelle sue applicazioni. Ad esempio, una soluzione di naillo molto semplice danneggia i vestiti invece di sbiancarli.
Inoltre, in mezzo acquoso l'HCLO viene anche trasformato in cloro, che spiega le colorazioni gialle di queste soluzioni:
Può servirti: concentrazione percentualeHCLO (AC) CL2(g) + H2O (l)
Sproporzione
L'atomo di cloro nell'ipoclorito di sodio ha uno stato di ossidazione di +1, che necessita solo di due elettroni per completare il suo ottetto di Valencia.
D'altra parte, la sua configurazione elettronica è [ne] 3s23p5, Essere in grado di svuotare tutti gli elettroni delle loro "p" orbitali, più energia.
Ciò si traduce nell'ipoclorito soffre di reazioni di sproporzione sugli ioni con stati di ossidazione di +1 e +5:
3cl-(AC) 2Cl-(AC) + CLO3-(AC)
Questa reazione in soluzione acquosa è accelerata con gli aumenti della temperatura e le concentrazioni di ipoclorito. Allo stesso modo, la reazione continua con un meccanismo diverso catalizzato dalla luce e dagli ossidi metallici di rame, nichel e cobalto:
2Naocl (aq) => o2(g) + 2NACL (AQ)
L'anidride NAMENTO è sproporzionato a una velocità molto più veloce, persino esplodendo.
Agente ossidante
L'atomo di cloro può accettare elettroni di specie negative (nucleofilo). L'anidride è un potente agente ossidante, riducendo gli anioni del cloruro (CL-).
Nel caso di NaClo · 5h2Oppure, si pensa che le molecole d'acqua impediscano parzialmente il CLO- Soffrono attacchi nucleofili.
Tuttavia, data la linearità strutturale del CLO-, Queste molecole d'acqua non rallentano abbastanza "attacchi" sull'atomo di CL. È per questo motivo che l'ipoclorito di sodio è un forte agente ossidante.
Riferimenti
- Wikipedia. (2018). Ipoclorito di sodio. Estratto il 7 aprile 2018 da: in.Wikipedia.org
- Francisco J. Arnaiz. (2016). Esperimenti per il laboratorio di chimica inorganica verde. Dipartimento di Chimica, Università di Burgos, Spagna.
- Libro chimico. (2017). Ipoclorito di sodio. Estratto il 7 aprile 2018 da: Chemicalbook.com
- Brian Clegg. (9 marzo 2016). Ipoclorito di sodio. Estratto il 7 aprile 2018 da: ChemistryWorld.com
- Oxychem. (Dicembre 2014). Manuale di ipoclorito di sodio. Estratto il 7 aprile 2018 da: Oxy.com
- PUBCHEM. (2018). Ipoclorito di sodio. Estratto il 7 aprile 2018 da: pubchem.NCBI.Nlm.NIH.Gov.

