Caratteristiche della fucosa, struttura, funzioni
- 3727
- 351
- Rosolino Santoro
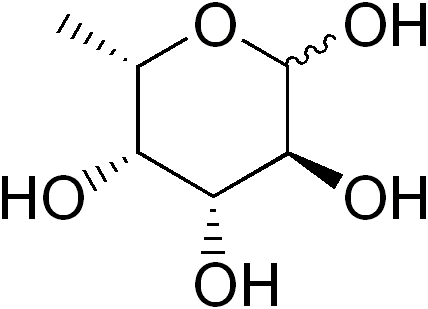
IL Fucosa (fuc abbreviato), o 6-l-denexi-gattosio, è un monosaccaride parzialmente di desossigenado (deossiazúcar) di sei carboni la cui formula empirica è C è C6H12O5. Come altri monosaccaridi, è uno zucchero poliidrossilato.
Quando un gruppo idrossilico viene sostituito da un atomo di idrogeno, viene derivata una deossiazúcar. Sebbene teoricamente questa sostituzione possa influire su qualsiasi gruppo idrossilico di qualsiasi monosaccaride, in natura c'è poca varietà di desiazúcús.
 Fonte: Edgar181 [dominio pubblico]
Fonte: Edgar181 [dominio pubblico] Alcune deossiazúces sono: 1) deossiribosa (2-Disoxxi-D-Libose), derivato dal D-Libosio, che fa parte del DNA; 2) il Ramnosa (6-D-DEXXI-MARSO), derivato dal d-manosa; 3) Fucosa, derivata da L-galattosio. Quest'ultimo è più frequente di D-Fucosa, derivato da D-galattosio.
[TOC]
Caratteristiche e struttura
Fucosa è anche noto con nomi 6-disoxxi-sclact-esosio, fucopirano, galattometil e nomi rodeo.
Sebbene sia normalmente formando polisaccaridi e glicoproteine, isolato come monosaccaride è più dolce del galattosio. Questo perché la sostituzione di un gruppo idrossilico con un atomo di idrogeno aumenta il carattere idrofobico e, quindi, la dolcezza della molecola.
I gruppi idrossilici di fucosa possono sperimentare le stesse reazioni degli altri zuccheri, producendo un'ampia varietà di acetali, glicosidi, eteri ed esteri.
Una biomolecola fucosilata è una a cui, dall'azione di una fucosiltransferasi, si sono unite, da legami glicosidici, molecole di fucosa. Quando l'idrolisi dei legami glicosidici si verifica dall'azione di una fucosidasi, separando così la fucosa, si dice che la biomolecola sia stata defucosilata.
Quando vengono generati glucanos fucosil, glucani più complessi chiamati fucanos, il che può o meno far parte delle glicoproteine. I fucani solfato sono definiti come quei polisaccaridi che contengono residui di solfato di l-fucosa. Sono tipici delle alghe marroni. Come esempi possono essere nominati Ascofilano, Sargasano e Pelvetano.
Uno dei fucanos meglio studiati è il fucoidano, ottenuto dalle alghe marroni Fucus vesiculosus, che è stato commercializzato (Sigma-Aldrich Chemical Company) per decenni.
Può servirti: qual è l'erristoo?Distribuzione in natura
Il d-fucosio è presente nelle sostanze antibiotiche prodotte dai microbi e nei glicosidi vegetali, come concorrenti, charrtreusina, ledienoosida e queirotossina.
Il l-fucosio è un componente dei polisaccaridi delle alghe, i fogli del prugna, le fodere di lino, soia e canola, la gomma tragacanto, le pareti cellulari della patata La corteccia del Ceiba e il mucigel del caliptra di mais, così come altre piante.
L-Fucosa è presente anche nelle uova di riccio di mare e nella gelatina che protegge le uova di rana.
Nei mammiferi, i fucani con l-fucosa formano i ligandi che agiscono nell'adesione leucocita-endoteliale mediata dalla selezione e partecipano a numerosi eventi ontogenetici.
L-Fucosa abbonda nei fucoesfingolipidi dell'epitelio gastrointestinale e del midollo osseo, e appare in piccole proporzioni nella cartilagine e nelle strutture cheratinose.
Nell'uomo, i fucanos con l-fucosa fanno parte di glicoproteine della saliva e succhi gastrici. Fanno anche parte degli antigeni che definiscono i gruppi sanguigni ABO. Sono presenti in diversi oligosaccaridi di latte materno.
Metabolismo della fucosa
Le fucosiltransferasi usano il pin-fucosio, una forma fucosa attivata dai nucleotidi, come donatore di fucosa nella costruzione di oligosaccaridi fucosilati.
Il PIL-Fucosa deriva dal PIL-Manosa per la successiva azione di due enzimi: il PIL-Manasea 4.6-Dydratasa e il GDP-4-Zo-6-Desossimanosa 3.5-Epimerasa-4-Reduttasi.
Uitlizando un cofattore NADP+, il primo enzima catalizza la disidratazione della mania del PIL. La riduzione della posizione 6 e l'ossidazione della posizione 4 produce il GDP-6-Desossi-4-che-Koaming (durante la reazione, l'ibrido viene trasferito dalla posizione 4 a 6 dello zucchero).
Il secondo enzima, che dipende da NADPH, catalizza l'epimerizzazione delle posizioni 3 e 5 e la rete del gruppo 4-ZO, del PIL-6-Desossi-4-Mamosa.
I batteri possono crescere usando la fucosa come singola fonte di carbonio ed energia attraverso un opeone inducibile della fucosa che codifica per gli enzimi catabolici per questo zucchero.
Può servirti: acido carbossilicoIl processo precedente prevede: 1) l'ingresso di Fucosa libera attraverso la parete cellulare con mediazione di una permeasi; 2) isomerizzazione fucosa (un aldosa) per formare una fucul (uno zea); 3) fosforilazione del fucul di formare FUCOLO-1-fosfato; 4) Una reazione aldolasi per formare lattaldeide e diidrossicetone fosfato da Fubulous-1-fosfato.
Funzioni
Carta per il cancro
Tra i sintomi di molti tipi di tumore cancerogeno vi sono la presenza di proteine legate al glucano che si distinguono con una composizione di oligosaccaride alterata. La presenza di questi glucani anormali, tra cui i fucanos, è legata alla malignità e al potenziale metastatico di questi tumori.
Nel carcinoma mammario, le cellule tumorali incorporano la fucosa in glicoproteine e glicolipidi. La fucosa contribuisce alla progressione di questo tumore, favorì l'attivazione delle cellule staminali tumorali, le metastasi ematogene e l'invasione dei tumori attraverso matrici extracellulari.
Nel carcinoma polmonare e nell'epatocarcinogenesi, l'espressione aumentata della fucosa è legata ad alto potenziale metastatico e con bassa probabilità di sopravvivenza.
Come controparte, alcuni fucani solfati sono sostanze promettenti nel trattamento del cancro, come determinato.
Carta in altre malattie
L'espressione aumentata di fucanos nelle immunoglobuline sieriche è stata correlata all'artrite reumatoide giovanile e adulta.
La carenza nell'adesione II è una rara malattia congenita a causa di mutazioni che alterano l'attività di un trasportatore FDP-fucosio situato nell'apparato Golgi.
I pazienti soffrono di ritardo mentale e psicomotorio e soffrono di infezioni batteriche ricorrenti. Questa malattia risponde favorevolmente a dosi di fucosa orale.
Potenziale biomedico
I fucanos di solfato ottenuti da alghe marroni sono importanti serbatoi di composti con potenziale terapeutico.
Può servirti: ititrium: struttura, proprietà, usi, ottenendoHanno proprietà anti -infiammatorie e antiossidanti, inibendo la migrazione dei linfociti nei siti di infezione e favorendo il rilascio di citochine. Aumenta la risposta immunitaria attivando linfociti e macrofagi.
Hanno proprietà anticoagulanti. È stato dimostrato nei pazienti umani che inibiscono per via orale l'aggregazione piastrinica.
Hanno un potenziale antibiotico e antiparasitico e inibiscono la crescita dei batteri patogeni dello stomaco Helicobacter pylori. Uccidi i parassiti Plasmodium spp. (Agente causale della malaria) e Leishmania Donovani (Agente causale della leishmaniosi visi, americana).
Infine, hanno potenti proprietà antivirali, inibendo l'ingresso nella cellula di diversi virus di grande importanza per la salute umana, anche Arenavirus, Citomegalovirus, Hantavirus, Hepadnavirus, HIV, virus dell'herpes simplex e virus dell'influenza.
Riferimenti
- Becker, d. J., Lowe, j. B. 2003. Fucose: biosintesi e funzione biologica nei mammiferi. Glycobiology, 13, 41R-53R.
- Deniaud-Bouët, e., Hodouin, k., Potin, p., Kloareg, b., Hervé, c. 2017. Una revisione sulle pareti cellulari algali marroni e sui polisaccaridi solfati contenenti fucosio: contesto della parete cellulare, proprietà biomediche e sfide di ricerca chiave.Polimeri di carboidrati, http: // dx.doi.org/10.1016/j.Carbol.2017.07.082.
- Fiori h. M. 1981. Chimica e biochimica di D-and L-Fucose. Progressi nella chimica e nella biochimica dei carboidrati, 39, 279-345.
- Listinsky, J. J., Siegal, g. P., Listinsky, c. M. 2011. L'importanza emergente di α-L-Fucosio nel cancro al seno umano: una revisione. SONO. J. Trasgr. Manzo., 3, 292-322.
- Murray, r. K., et al. 2003. Biochimica illustrata di Harper. McGraw-Hill, New York.
- Pereira, l. 2018. Usi terapeutici e nutrizionali delle alghe. CRC Press, Boca Raton.
- Staudacher, e., Altmann, f., Wilson, i. B. H., März, l. 1999. Fucose in N-glicani: dalla pianta all'uomo. Biochimica et Biophysica Acta, 1473, 216-236.
- Tanner, w., Loewus, f. A. 1981. Carboidrati vegetali ii. Carboidrati extracellulari. Springer, New York.
- Vanhooren, p. T., Vandamme, e. J. 1999. L-Fucosio: occorrenza, ruolo fisiologico, sintesi chimica, enzimatica e microbica. Journal of Chemical Technology and Biotechnology, 74, 479-497.
- « Posizione del cerchio polare antartico, caratteristiche, flora e fauna
- Fasi di chemosintesi, organismi, differenze con la fotosintesi »

