Sintesi dell'acido fenossiacetico, procedura, usi, rischi
- 3588
- 858
- Rufo Longo
Lui Acido fenossiacetico È una sostanza organica, formata dalla reazione tra fenolo e acido monocloroacetico in presenza di una soluzione di idrossido di sodio. La procedura utilizzata per ottenere questo prodotto è chiamata sintesi di eteri di Williamson.
L'acido fenossiacetico sintetizzato è un precipitato bianco o incolore, formato da cristalli a forma di ago, praticamente insolubile in acqua (solubilità dell'acqua 12 g/l L-1), Ma solubile in acido acetico, fenolo e dieta etere.
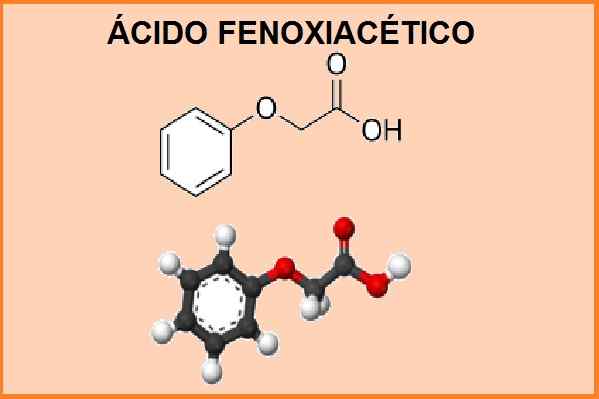
 Struttura chimica dell'acido fenossiacetico. Fonte: "Acido fenossiacetico". Wikipedia, Enciclopedia gratuita. 13 maggio 2014, 17:21 UTC. 13 maggio 2014, 17:21 in.Wikipedia.org. Design dell'immagine modificato.
Struttura chimica dell'acido fenossiacetico. Fonte: "Acido fenossiacetico". Wikipedia, Enciclopedia gratuita. 13 maggio 2014, 17:21 UTC. 13 maggio 2014, 17:21 in.Wikipedia.org. Design dell'immagine modificato. Il suo nome chimico è 2-fenossietanoico e la sua formula molecolare è C8 H8 O3. La massa molecolare è di 152,15 g.mol-1. Questo prodotto si comporta come un acido debole e ha un punto di fusione tra 98 e 100 ° C e un punto di ebollizione di 285 ° C.
L'acido fenossiacetico è un prodotto intermedio nella sintesi di sostanze con le proprietà degli erbicidi. Di per sé, l'acido fenossiacetico ha proprietà antifungine di fronte a Candida albicans e Trichophyton rubrum. È anche utile come esfoliativo della pelle, eliminando la cheratina in eccesso nei calli.
È necessario avere precauzioni per la gestione perché quando riscaldati emette gas tossici che sono corrosivi. Tra i gas c'è l'idrogeno cloruro.
L'esposizione diretta con questo prodotto potrebbe causare lieve pelle o irritazione mucosa, sebbene non di grande importanza tranne che per l'affetto della mucosa oculare può essere grave. Produce anche irritazione del tratto respiratorio se viene inalato e del percorso gastrico se viene ingerito.
È una sostanza non infiammabile e abbastanza stabile a temperatura ambiente, tuttavia, ad alte temperature o pressioni, potrebbe perdere la sua stabilità, e di fronte all'acqua può rilasciare una certa quantità di energia ma non lo farà violentemente.
[TOC]
Sintesi di acido fenossiacetico
Il fenolo è un alcol e come tale si comporta come un acido debole, motivo per cui perde facilmente il protone acido (H+) di fronte a un alcali (idrossido di sodio) per diventare un alcossido (fenolato). Ciò successivamente, attraverso una sostituzione nucleofila bimolecolare, formerà etere.
Può servirti: ossido di boro (B2O3): cosa è, struttura, proprietà, usiAlcossido funziona come un nucleofilo, cioè è in grado di rinunciare a 2 elettroni che sono liberi per un'altra sostanza. Nel caso della reazione a portata di mano, è l'alogenuro alchilico (acido monocloroacetico), in modo tale da unire fortemente attraverso legami covalenti con esso, formando una nuova sostanza che in questo caso è l'etere.
Durante la reazione si verifica uno spostamento dello ione alogenido, che viene sostituito dall'anione alcossido. Questa reazione è conosciuta come la sintesi di Williamson's Eteres.
La quantità di prodotto ottenuta e la velocità con cui viene prodotto dipenderà dalla concentrazione dei reagenti coinvolti, poiché si tratta di una reazione cinetica di secondo ordine, in cui la collisione delle molecole (nucleofilo + alogenuro alchil) ne determina l'efficacia.
Procedura
Passo 1
Per iniziare la sintesi dell'acido fenossiacetico, 0,5 gr di fenolo è molto attento e posizionato in un pallone a forma di pera e una sola bocca, con una capacità di 50 ml. 2,5 ml di idrossido di sodio (NaOH) vengono aggiunti al 33% (p/v) per dissolverlo.
Controllare l'alcalinità della soluzione con una carta indicatore di pH. Metti un coperchio di sughero al pallone e per 5 minuti si mescolano fortemente. Per la miscela è possibile utilizzare un agitatore magnetico.
Passo 2
Successivamente, aggiungere 0,75 g di acido monocloroacetico e ripetere la procedura di miscelazione per 5 minuti.
Nel caso in cui la miscela cerchi di indurirsi o diventare pastosa, si può aggiungere acqua (tra 1 e 3 ml), ma ciò viene gradualmente aggiunto fino a quando non ritorna alla contesto precedente, senza diluire troppo.
Passaggio 3
Scopri il pallone e posizionalo all'interno di un bagno Maria che possiede un sistema di reflusso per 10 minuti. Se il sistema di flusso non è disponibile per 40 minuti.
Passaggio 4
Lascia raffreddare la soluzione e aggiungi 5 ml di acqua, quindi acidificare con una soluzione HCL concentrata fino a raggiungere il pH 1. (Misurare il pH con un documento a questo scopo).
Può servirti: cloruro di ammonio (NH4Cl)Passaggio 5
Passare la miscela con cura attraverso l'imbuto di separazione e rimuovere tre volte, usando 5 ml di etere etilico in ciascuna procedura.
Uno organico estrae e sostituire nell'imbuto di separazione per eseguire un'acqua triplicata, usando 5 ml di acqua in ogni lavaggio.
Le frazioni acquose sono separate per essere scartate.
Passaggio 6
Successivamente, la frazione organica viene estratta con 3 ml di carbonato di sodio (NA2Co3) 15% tre volte.
L'estratto acquoso alcalino ottenuto viene posizionato nel bagno di ghiaccio ed è acidificato con HCl fino a pH = 1, che genera precipitazione del prodotto. La fase di acidificazione deve essere eseguita con molta attenzione aggiungendo caduta per goccia, poiché la reazione genera schiuma e se viene bruscamente aggiunta.
Il solido è ottenuto dalla filtrazione del vuoto, il precipitato viene lavato e lasciato asciugare.
Passaggio 7
Il prodotto ottenuto è una pesatura e si vede le prestazioni e il punto di fusione.
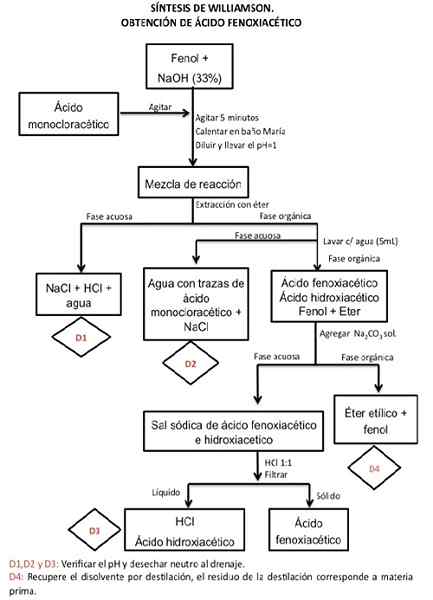 Fonte: Sandoval M. (2015). Pratiche di laboratorio chimico organico Manuale II. Facoltà di chimica della National Autonomous University of Mexico.
Fonte: Sandoval M. (2015). Pratiche di laboratorio chimico organico Manuale II. Facoltà di chimica della National Autonomous University of Mexico. Applicazioni
Il solo acido fenossiacetico ha un'attività fungicida contro alcuni funghi, come Candida albicans e Trichophyton rubrum. Questa azione è stata descritta in un'indagine condotta da González e collaboratori.
Il lavoro ha rivelato che la concentrazione minima inibitoria o fungista (CMI) e la concentrazione minima di fungicida (CMF) era la stessa (2,5 mg/ml) per 13 specie di specie Candida albicans Da campioni clinici, in particolare da pazienti affetti da onicomicosi.
Mentre una tensione di Candida albicans ATCC 10231 ha presentato un CMI di 2,5 mg/mL e un CMF di 5,0 mg/ml. Per la sua parte, Trichophyton rubrum ha presentato un CMI di 0.313 mg/ml e un CMF di 1.25 mg/ml in 8 ceppi analizzati da chiodi infetti.
Inoltre, l'acido fenossiacetico è molto utile come esfoliativo della cheratina, quindi è in grado di ridurre al minimo i calli o i cereali sulla pelle interessata con queste caratteristiche.
D'altra parte, l'acido fenossiacetico è materia prima per la sintesi dei pesticidi, in particolare gli erbicidi, come l'astix e il duposan.
Può servirti: acido solfuro (H2S): struttura, proprietà, usi, importanzaRischi
Se il prodotto viene ingerito accidentalmente, causerà irritazione delle mucose in tutto il tratto gastrointestinale (bocca, esofago, stomaco e intestino).
Se viene inalato, produrrà l'irritazione della mucosa respiratoria, causando insufficienza respiratoria e tosse.
Sul pelle può causare lieve irritazione. Mentre l'irritazione della mucosa per gli occhi sarà più grave. In questi casi si raccomanda di lavare l'area interessata con abbondante acqua e acqua.
Questo prodotto è stato associato come fattore predisponente per la condizione o l'aspetto dei tumori adiposi. Questi tumori di solito si sviluppano più frequentemente negli arti o nell'addome.
D'altra parte, questo prodotto è classificato come non pericoloso per il trasporto secondo i criteri descritti dai regolamenti di trasporto.
I pesticidi derivati dall'acido fenossiacetico se sono generalmente tossici per l'ambiente e sono stati correlati a mutazioni genetiche, in particolare alla traslocazione T presente nel linfoma non hodgkin nell'uomo.
Precauzioni
- Questo prodotto deve essere tenuto lontano da forti agenti e basi ossidanti che possono reagire violentemente.
- È importante evitare di riscaldare questo prodotto.
- Manipolare usando misure di protezione, come guanti, abito, lenti di sicurezza.
Riferimenti
- González G, Trujillo R. Acido fenossiacetico, identificazione e determinazione della sua azione antifungina In vitro contro Candida albicans e Trichophyton rubrum. Rev. Peruviano della Facoltà di Farmacia, 1998; 34 (109). Disponibile in: UNMSM.Edu
- "Acido fenossiacetico". Wikipedia, Enciclopedia gratuita. 13 maggio 2014, 17:21 UTC. 13 maggio 2014, 17:21 Wikipedia.org
- Merck Laboratories. Scheda di sicurezza. 2017. Disponibile su: TES.Uabc.mx/
- Aventis Laboratories. Avventis Safety Data Sheet. 2001. Disponibile su: Affa.Cl
- Gutiérrez m. Fenossiacetico nelle emergenze tossicologiche. Informazioni e consigli di ciatox toxox. Università nazionale della Colombia. Disponibile su: Enforn.com
- Sandoval m. (2015). Pratiche di laboratorio chimico organico Manuale II. Facoltà di chimica della National Autonomous University of Mexico.
- Merck Laboratories. Scheda dati di sicurezza in base al regolamento CE n. 1907/2006. 2015 disponibile su: ESE.Uabc.mx/
- Berzal-Calejo M, Herranz-Torrubian A, Cuenca-González C. Tumore adiposo con sintomi di allarme. Rev Clín Med Fam 2015, 8 (3): 246-250. Disponibile su: scielo.Isciii.È/scielo.
- Matheus T, bolaños a. Micronúcleos: biomarker di genotossicità esposto ai pesticidi. Salus, 2014; 18 (2): 18-26. Disponibile su: VE.Scielo.org
- « +380 detti cileni tipici e popolari
- Caratteristiche del parco nazionale di Cozumel Arreciphes, tempo, flora, fauna »

