Struttura, proprietà e usi butanone
- 2728
- 798
- Zelida Gatti
IL Butanone È un composto organico, in particolare un chetone, la cui formula chimica è Cho3Cap2Coch3. Il suo aspetto è quello di un liquido incolore usato fondamentalmente come solvente. Ha simile alle proprietà dell'acetone, ma fa bollire a una temperatura più elevata ed evapora più lentamente.
È prodotto dalla deidrogenazione catalitica del 2-butanolo (composto chirale). Tuttavia, è nello stato naturale nella composizione di alcuni frutti. Fa parte delle emanazioni dei tubi di scarico dei veicoli ed è un componente del fumo del tabacco.
 Molecola di butanone. Fonte: Pixabay.
Molecola di butanone. Fonte: Pixabay. È dopo l'acetone il più semplice di questa famiglia di composti organici. Butnonone provoca irritazione negli occhi e nel naso. In una dose insolitamente alta può causare irritazione della mucosa polmonare. D'altra parte, questo liquido è considerato un agente precursore dei narcotici.
Butanone ha una grande solubilità in acqua; Ma è anche molto solubile in solventi organici come etanolo, etere, acetone, benzene e cloroformio. Ciò potrebbe essere spiegato perché il suo valore del log P (0,29) per il coefficiente di partizione di ottano/acqua è basso.
[TOC]
Struttura butanone
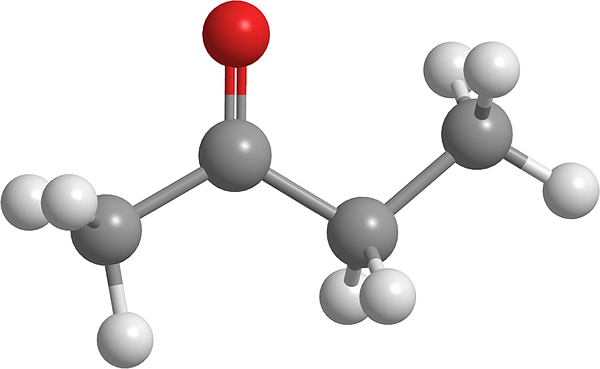
Nell'immagine superiore, la molecola di butanone viene mostrata con un modello di sfere e barre. L'atomo di ossigeno del gruppo carbonilico (sfera rossa) può essere visto nel secondo carbonio. Questo gruppo, C = O, è responsabile del conferimento di un momento di dipolo permanente alla molecola.
Butanone, Strutturally View, non è altro che un acetone a cui è stato aggiunto un gruppo di metilene, CH2. Avendo più carboni, il momento di dipolo è più piccolo rispetto a quello dell'acetone; Ma la sua più grande massa molecolare fa bollire a una temperatura più elevata.
Questa molecola, come altri chetoni, manca della possibilità di formare ponti idrogeno; E quindi, le loro interazioni dipolo-dipolo non sono così forti.
Può servirti: emulsionante: processo di emulsione, aspetti molecolari, applicazioniEcco perché è un liquido volatile. Quando la temperatura scende (-86,6 ° C), i suoi dipoli deboli sono quelli che guidano le loro molecole per formare un cristallo. Oltre a ciò, si può anche commentare che il butanone è strutturalmente asimmetrico.
Proprietà
Formula molecolare
C4H8O ch3Coch2Cap3
Nomi
- Butanone.
- 2-butanone.
- Butan -2 -ona.
- Methyl Etil Cetona.
Massa molare
72.107 g/mol.
Descrizione fisica
Liquido incolore.
Odore
Fragrante alla menta, moderatamente forte.
Punto di ebollizione
79,59 ºC a 760 mmHg.
Punto di fusione
-86.6 ºC.
punto di accensione
-9 ºC (tazza chiusa).
Solubilità dell'acqua
29 g /100 ml a 20 ºC. Mentre il suo momento di dipolo è inferiore a quello dell'acetone, può ancora interagire in modo eccellente con molecole d'acqua. Da loro riceve ponti idrogeno: (CH3) (Ch2Cap3) C = o-hah. Per questo motivo è molto solubile in acqua.
Solubilità nei solventi organici
Solubile in benzene, alcol ed etere; Manibile con oli, etanolo, etere, acetone, benzene e cloroformio. Si noti che il butanone è solubile in un'ampia varietà di solventi.
Densità
0,7997 g/cm3 a 25 ºC.
Densità del vapore
2,41 (in relazione all'acqua = 1).
Pressione del vapore
90,6 mmHg a 25 ºC.
Coefficiente di partizione ottanolo/acqua
Log p = 0,29
Temperatura di auto -Identizione
505 ºC.
Decomposizione
Si decompone per processi fotochimici per ossidazione mediante radicale idrossile libero. Se riscaldato alla decomposizione emette un fumo di acri.
Sostanza vischiosa
0,40 cpoise a 25 ºC.
Calore a combustione
2.444,1 kJ/mol a 25 ° C.
Calore di vaporizzazione
31,30 kJ/mol nel punto di ebollizione; e 34,79 kJ/mol a 25 ° C.
Può servirti: legge generale del gasTensione superficiale
23,97 mn/m a 25 ºC.
Potenziale di ionizzazione
0,54 eV.
Soglia di odore
Basso odore: 0,735 mg/m3.
Alto odore: 147,5 mg/m3.
Indice di rifrazione
Da 1.788 a 20 ºC.
Costante di dissociazione
PKA = 14.70.
Stabilità
Stabile, ma altamente infiammabile. Incompatibile con agenti ossidanti, basi e forti agenti riducenti. L'umidità dovrebbe essere evitata.
Applicazioni
Solvente
Il butanone è usato come solvente nell'elaborazione di rivestimenti superficiali, fabbricazione di polvere senza fumo, elaborazione delle resine colorate e nell'eliminazione dell'accumulo di grassi prodotti dai lubrificanti.
Inoltre, viene utilizzato nell'elaborazione di:
- Pelle artificiale.
- Gomas.
- Lacas.
- Vernici.
- Colla.
- Solventi.
- Posta di verniciatura.
- Adesivi.
- Cementi di plastica.
- Sigillanti.
- Nastri magnetici.
- Carta trasparente.
- Inchiostri di stampa.
- Cosmetici e prodotti farmaceutici.
Viene anche utilizzato come solvente per la defazione di superfici metalliche, detergenti per apparecchiature elettroniche ed estrazione di grassi. Serve per l'estrazione del legno duro e l'olio vegetale.
È un ingrediente inerte nell'elaborazione dei pesticidi e nella produzione di acetato e nitrato di cellulosa.
Viene usato come solvente di estrazione nella trasformazione degli alimenti e negli ingredienti alimentari; Ad esempio, nel frazionamento di grassi e oli, nonché nel processo decaffeinato del caffè. Viene anche usato come solvente nei marcatori utilizzati nelle schede bianche.
Reagente
- Butanone è usato come fotoiniciatore solubile in acqua.
- Condensa con la formaldeide per produrre isopropenil chetone.
- Sperimenta l'autocodensa per la produzione di etil amylo cetona.
- Reagisce con citrali per ottenere componenti del profumo come il metilpseudoionone.
Può servirti: calore di reazione- Interviene come catalizzatore nella produzione di idraccina.
- Inoltre, è un precursore del perossido di metil etil cetona, che è un catalizzatore per alcune reazioni di polimerizzazione.
Cemento di plastica
Butanone ha l'applicazione come agente di saldatura in plastica, con l'uso nell'assemblaggio di modelli in scala di polistirene. Butnonone dissolve il polistirene, permettendo ai bordi di unirsi quando si verifica una nuova polimerizzazione. Questo comportamento è di cemento e non di colla.
Altri usi
Il butanone è usato come sterilizzante delle spore di batteri in strumenti di chirurgia, aghi, iniettori ipodermici e strumenti dentali.
È usato come agente aromatizzato di cibo in concentrazioni molto basse; Ad esempio, nelle bevande alcoliche la concentrazione è di 20 ppm; in prodotti al forno, 12,7 ppm; Le carni hanno circa 26,5 ppm; gomma da masticare, 0,63 ppm; e in grassi e oli, 1,0 ppm.
E infine, il butanone è usato nella separazione dell'apoproteina del gruppo di emoproteine nelle emoproteine.
Riferimenti
- Morrison, r. T. e Boyd, r, n. (1987). Chimica organica. 5ta Edizione. Editoriale Addison-Wesley Inter-American.
- Carey f. (2008). Chimica organica. (Sesta edizione). Mc Graw Hill.
- Graham Solomons t.W., Craig b. Frigorifero. (2011). Chimica organica. Ammine. (10thEdizione.). Wiley Plus.
- Centro nazionale per le informazioni sulla biotecnologia. (2019). Database di metil etil chetonici pubchem. CID = 6569. Recuperato da: pubchem.NCBI.Nlm.NIH.Gov
- Wikipedia. (2019). Butanone. Recuperato da: in.Wikipedia.org
- Royal Society of Chemistry. (2015). Butanone. Chemspider. Recuperato da: Chemspider.com
- Arlem Cheprasov. (2019). Cos'è Butanone? Formula e uso. Studio. Recuperato da: studio.com
- Ben Verve. (17 maggio 2017). Butanone. Mondo chimico. Recuperato da: Chemistryworld.com

