Bisulfita di sodio (NAHSO3) Struttura, proprietà, usi, ottenendo
- 650
- 29
- Baldassarre Ross
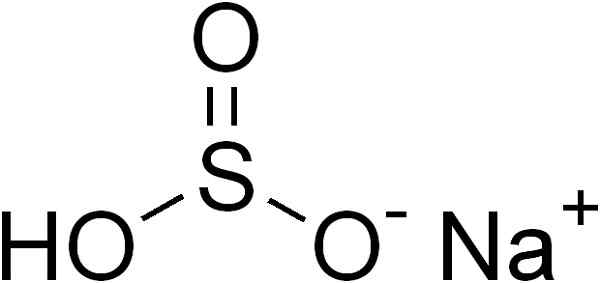
Lui bisolfito di sodio È un solido inorganico formato da un sodio ione Na+ e uno ione Bisulfite HSO3-. La sua formula chimica è nahso3. È un solido bianco cristallino e per le sue proprietà antiossidanti è ampiamente usato come conservante alimentare (ad esempio in alcune marmellate).
Il nahso3 È un composto chimico riducente, che è l'opposto dell'ossidazione, e per questo motivo agisce come antiossidante in molte delle sue applicazioni, come i prodotti commestibili, poiché impedisce il suo deterioramento.
 Alcune marmellate commerciali contengono bisogni di sodio nahso3. Autore: vettori di OpenClipart. Fonte: Pixabay.
Alcune marmellate commerciali contengono bisogni di sodio nahso3. Autore: vettori di OpenClipart. Fonte: Pixabay. Tuttavia, questo uso è stato messo in discussione perché i casi di asma sono stati segnalati nelle persone dopo aver mangiato alimenti contenenti bisolfito di sodio. Si dice persino distruggere la vitamina B1 di questi.
Le organizzazioni sanitarie internazionali hanno limitato il loro utilizzo alle microconità negli alimenti.
Tuttavia, il bisolfito di sodio ha molti altri usi, come nell'ottenimento di iodio, come antidecfezione, ai tessuti candeggini, per la digestione del legno durante la preparazione della polpa di carta, come disinfettante di botti di birra e vino, ecc.
[TOC]
Struttura chimica
Il bisolfito di sodio è formato da una na catione di sodio+ e un anione HSO bisolfito3-.
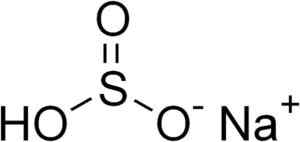 Struttura chimica del bisolfito di sodio3. EDGAR181 [dominio pubblico]. Fonte: Wikimedia Commons.
Struttura chimica del bisolfito di sodio3. EDGAR181 [dominio pubblico]. Fonte: Wikimedia Commons. Nelle soluzioni acquose il bisolfito forma 4 specie. In soluzione diluita c'è un equilibrio tra le strutture mostrate di seguito:
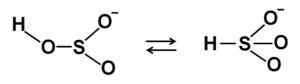 Strutture a ioni Bisulfito HSO3- In soluzione acquosa diluita. Autore: Marilú Stea.
Strutture a ioni Bisulfito HSO3- In soluzione acquosa diluita. Autore: Marilú Stea. Quando la concentrazione aumenta, due molecole di bisolfito interagiscono tra loro formando lo ione pirosolfito s2O52-:
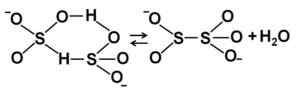 Strutture di ioni bisolfito in soluzione acquosa concentrata. Autore: Marilú Stea.
Strutture di ioni bisolfito in soluzione acquosa concentrata. Autore: Marilú Stea. Nomenclatura
-Bisolfito di sodio
-Idrogenosolfito di sodio
-Idrosolfito di sodio.
Proprietà
Stato fisico
Solido bianco cristallino.
Peso molecolare
104,06 g/mol
Punto di fusione
Si decompone.
Densità
1,48 g/cm3 a 20 ºC.
Solubilità
Solubile in acqua: 29 g/100 g di acqua.
ph
Le sue soluzioni sono acide, con un pH tra 2,5 e 5,5.
Proprietà chimiche
In soluzione acquosa bisolfito di sodio3 è separato nei suoi ioni: il catione di sodio na+ e l'anione HSO bisolfito3-.
Se il bisolfito di sodio è esposto all'aria perde un po '2 e ossida lentamente il solfato2SW4.
Può servirti: acido gallico: struttura, proprietà, ottenimento, usiSe riscaldato fino a quando la sua decomposizione emette ossidi di zolfo e monossido di sodio.
È un agente riducente, che è l'opposto dell'ossidante. E per questo motivo può comportarsi come antiossidante.
Ha un leggero odore di zolfo. Non è infiammabile.
Rischi
Bisulfita di sodio Nahso3 È una forte pelle e tessuto irritante. La polvere irrita gli occhi, il naso e la gola. Per ingestione irrita lo stomaco. Dosi grandi possono causare crampi violenti, diarrea, depressione e morte.
Non è carburante ma è riscaldato produce gas irritanti e tossici.
Ottenimento
Viene preparato saturando una soluzione di carbonato di sodio Na2Co3 Con biossido di zolfo così2 e cristallizza nella soluzione.
Applicazioni
Nell'industria della polpa e della carta
Il nahso3 È usato nella digestione del legno, in modo che possa quindi diventare carta. Funge anche da pasta più bianca.
Viene anche usato per eliminare il cloro quando la polpa di carta è stata sbiancata con questo.
Nell'industria alimentare
Il bisolfito di sodio per la sua proprietà riducente funge da antiossidante.
Viene usato come conservante in una grande quantità di cibo e bevande, tra cui vino e birra, per prevenirne il deterioramento e migliorare il sapore.
Serve a cannare il cibo, come alcuni amidi commestibili.
Riduce o impedisce il deterioramento del cibo, consente di condizionare l'impasto usato negli alimenti al forno e serve ad ammorbidire i cereali di mais durante la macinazione a umido, tra gli altri usi.
Oltre a controllare la fermentazione di vino e birra, funge da antisettico nella sua elaborazione perché funge da sterilizzazione e fungicida in botti e denti.
 Le botti di vino o di birra sono talvolta disinfettate con bisolfito di sodio3. Autore: clker-free-vector-images. Fonte: Pixabay.
Le botti di vino o di birra sono talvolta disinfettate con bisolfito di sodio3. Autore: clker-free-vector-images. Fonte: Pixabay. Nei frutti essiccati è in concentrazioni superiori a 100 ppm (ppm significa "parti per milione"), in molti altri alimenti è in concentrazioni tra 10 e 100 ppm, come patate, sottaceti, salse e marmellate surgelate e secche.
 Gli alimenti in salamoia commerciale contengono spesso bisolfito di sodio nahso3. Autore: mix di foto. Fonte: Pixabay.
Gli alimenti in salamoia commerciale contengono spesso bisolfito di sodio nahso3. Autore: mix di foto. Fonte: Pixabay. Controversia sul suo uso nel cibo
C'è stata qualche preoccupazione per gli effetti tossici sia immediati che a lungo termine di bisolfito di sodio negli alimenti. Ci sono opinioni divergenti.
Può servirti: ferrocianuro di potassioCi sono segnalazioni di reazioni avverse di pazienti con asma, che è una malattia respiratoria, dopo l'ingestione di generi alimentari con NAHSO3. Altre fonti indicano che lo ione bisolfito può distruggere la vitamina B1 o la tiamina.
 Ragazza che aspira una medicina per alleviare l'asma. Autore: vettori di OpenClipart. Fonte: Pixabay.
Ragazza che aspira una medicina per alleviare l'asma. Autore: vettori di OpenClipart. Fonte: Pixabay. Tuttavia, alcuni ricercatori nel 1985 hanno scoperto che il bisolfito di sodio serve a proteggere dagli agenti chimici e inibisce o impedisce la trasformazione delle cellule in cancro. Le dosi basse sono le migliori.
Questo effetto protettivo è stato spiegato in base alle sue proprietà riducenti o antiossidanti e che in questo modo potrebbe attaccare i radicali liberi.
D'altra parte, l'Organizzazione mondiale della sanità o che (per il suo acronimo per l'inglese Organizzazione mondiale della sanità), raccomanda come un livello accettabile di assunzione giornaliera di circa 0,7 mg/kg della persona.
Ciò significa che si consiglia di non superare tale importo.
La Food and Medicine Administration degli Stati Uniti o USFDA (acronimo inglese US Food and Drug Administration), ha classificato il bisolfito di sodio come "generalmente riconosciuto come assicurazione".
In applicazioni agricole
Utilizzato a basse concentrazioni il NAHSO3 Serve come regolatore di crescita delle piante, per migliorare la fotosintesi e promuovere le prestazioni delle colture.
Questo obiettivo è stato testato in vari tipi di piante come la fragola e le piante da tè.
 Le piante alla fragola migliorano le loro prestazioni con piccole quantità di Nahso3 Nell'irrigazione. Autore: Alyssapy. Fonte: Pixabay.
Le piante alla fragola migliorano le loro prestazioni con piccole quantità di Nahso3 Nell'irrigazione. Autore: Alyssapy. Fonte: Pixabay. È l'ingrediente attivo di molti pesticidi e biocidi.
In ambienti acquatici può anche accelerare la trasformazione di alcuni erbicidi in prodotti meno tossici eliminando il cloro.
Nel ottenere iodio
Il nahso3 È il composto riducente utilizzato per rilasciare iodino di naio di sodio3. Questo è uno dei modi per ottenere iodio da fonti come il cileno Nitro o alcune acque di Salinas.
Dopo aver cristallizzato il nitrato di sodio della soluzione di nitrato del Cile lordo, esiste una soluzione NAIO3 che è trattato con bisolfito di sodio3, generare iodio gratuito.
2 Naio3 + 5 Nahso3 → 3 Nahso4 + N / a2SW4 + Yo2
Nell'industria dei mobili e del legno
Il nahso3 È stato testato per modificare le proteine di soia e migliorare le sue proprietà di adesione con legno con l'obiettivo di pezzi di legno in pasta l'uno dall'altro per prepararsi ad esempio agglomerati, cartone di legno o cartone in pietra, formulazione, ecc. Tutto per mobili o schede, tra diverse applicazioni.
Può servirti: idrossido di litio (Lioh) Agglomerato di schegge o resti di legno. Autore: Titus Tschardke [dominio pubblico]. Fonte: Wikimedia Commons.
Agglomerato di schegge o resti di legno. Autore: Titus Tschardke [dominio pubblico]. Fonte: Wikimedia Commons. Questo viene fatto per sostituire gli adesivi tradizionali in base alla formaldeide perché sia nel loro processo di produzione che durante l'uso tendono a formalizzare liberamente l'atmosfera, che è un composto tossico.
Il bisolfito di sodio migliora il contenuto solido dell'adesivo proteico di soia e riduce la viscosità di questo miglioramento della sua fluidità in modo che penetri.
Adesivo proteico di soia modificata con Nahso3 Ha una buona resistenza all'acqua e un'eccellente stabilità di conservazione a causa dell'azione antiossidante del bisolfito di sodio.
Ciò conferma che ha modificato gli adesivi proteici di soia con Nahso3 Sono paragonabili agli adesivi basati sulla formaldeide e possono essere utilizzati nell'industria dei mobili e del legno, essendo meno inquinanti.
In varie applicazioni
Ha più usi, generalmente in base alle sue proprietà riducenti (che è l'opposto dell'ossidante). Ecco alcune applicazioni.
-In fotografia.
-Nel conciatore in pelle, per rimuovere i capelli dalle pelli.
-Usi terapeutici: anti -infettivo. È usato come antiossidante in alcune gocce per -ojos.
-Nell'estrazione di gas naturale mediante frattura idraulica.
-Nella colorazione in fibra viene utilizzato per la preparazione di bagni di vasca calda o fredda, per solubilizzare determinati coloranti o coloranti.
-Come riduzione del bucato o sbiancamento, per cannare la lana, la seta e le fibre di pianta.
-In chimica laboratori per rimuovere la pelle e le macchie di abbigliamento. Nei laboratori biochimici come conservante fluido o soluzioni che possono essere deteriorate nel tempo. Come reagente chimico.
-Per coagulazione in lattice in gomma.
-Nell'industria cosmetica come antiossidante.
-Disinfettante e candeggina.
-Nel trattamento delle acque reflue per eliminare il cloro utilizzato nella fase finale della disinfezione ed essere in grado di scaricare le acque già trattate nell'ambiente.
 Serbatoio di bisolfito di sodio in un impianto di trattamento delle acque reflue in California, dove viene utilizzato per eliminare il cloro in eccesso prima che le acque purificate vengano scaricate nell'ambiente. Grendelkhan [CC BY-SA 3.0 (https: // creativeCommons.Org/licenze/by-sa/3.0)]. Fonte: Wikimedia Commons.
Serbatoio di bisolfito di sodio in un impianto di trattamento delle acque reflue in California, dove viene utilizzato per eliminare il cloro in eccesso prima che le acque purificate vengano scaricate nell'ambiente. Grendelkhan [CC BY-SA 3.0 (https: // creativeCommons.Org/licenze/by-sa/3.0)]. Fonte: Wikimedia Commons. Riferimenti
- O.S. Biblioteca nazionale di medicina. (2019). Bisolfito di sodio. Recuperato da Pubchem.NCBI.Nlm.NIH.Gov.
- Qi, g. et al. (2013). Adesione e proprietà fisico -chimiche della proteina Ser modificata dal bisolfito di sodio. J Am Oil Chem Soc (2013) 90: 1917-1926. Recuperato da AOC.Biblioteca online.Wiley.com.
- Borek, c. et al. (1985). Il bisolfito di sodio protegge dalla trasformazione radiogogenica e indotta chimicamente nell'embrione di criceto e nelle cellule C3H/10T-1/2. Tossicolo IND Health 1985Sep; 1 (1): 69-74. Recuperato dalle riviste.Sagepub.com.
- Friedler, e. et al. (2015). Un approccio di monitoraggio attivo continuo per identificare le connessioni incrociate tra acqua potabile e sistemi di distribuzione degli effluenti. Environment Monit Assess (2015) 187: 131. Link recuperato.Springer.com.
- Cotone, f. Albert e Wilkinson, Geoffrey. (1980). Chimica inorganica avanzata. Quarta edizione. John Wiley & Sons.
- Programma Sunnyvale Cleanwater. (2019). Piano generale dell'impianto di controllo dell'inquinamento idrico. Recuperato da Sunnyvalecleanwater.com.
- Barros Santos, C. (2008). Additivi nell'alimentazione degli spagnoli e nella legislazione che regola la loro autorizzazione e uso. Visione dei libri. Recuperato dai libri.Google.co.andare.

