Anfoter che sono, tipi ed esempi
- 2953
- 344
- Kayla Serr
IL Anfostri Sono i composti o gli ioni che hanno la peculiarità di essere in grado di comportarsi come acido o come base, secondo la teoria Bronsted e Lowry. Il suo nome viene dalla parola greca Anfoteroi, il che significa "entrambi".
Molti metalli formano ossidi di anfoteros o idrossidi, tra cui rame, zinco, stagno, piombo, alluminio e berillio. La caratteristica anfoter di questi ossidi dipende dagli stati di ossidazione dell'ossido in questione. Alla fine dell'articolo sono inclusi esempi di queste sostanze.

Gli ossidi metallici che possono reagire con acidi e basi per produrre sali e acqua sono noti come ossidi di anfoteros. Gli ossidi di piombo e zinco sono ottimi esempi, tra gli altri composti.
[TOC]
Cosa sono l'anfoter?
Secondo la teoria della base acida di Bronsted e Lowry, gli acidi sono quelle sostanze che donano protoni, mentre le basi sono quelle che accettano o prendono i protoni.
Una molecola chiamata amfotato avrà reazioni in cui acquisisce protoni, in quanto avrà anche la capacità di donarli (anche se non è sempre così, come si vedrà nella prossima sezione).
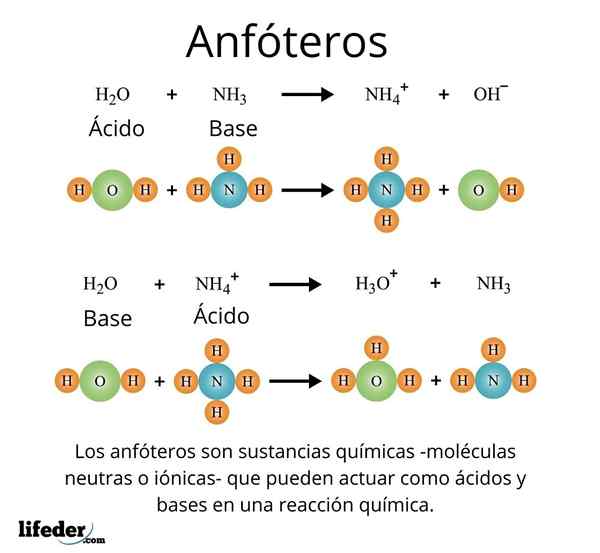
Un caso importante e ben noto è quello del solvente universale, acqua (H₂O). Questa sostanza reagisce facilmente con gli acidi, ad esempio in reazione con l'acido cloridrico:
H2O + HCl → H3O+ + Cl-
Ma a sua volta, non ha nemmeno problemi a reagire con una base, come nel caso dell'ammoniaca:
H2O + NH3 → NH4 + OH-
Con questi esempi si può osservare che l'acqua agisce pienamente come una sostanza anfotata.
Tipi di anfoter
Anche se le sostanze anfotese possono essere molecole o ioni, ci sono molecole che dimostrano meglio le caratteristiche anfotenti e aiutano a studiare meglio questo comportamento: sostanze anfrofrotiche. Queste sono molecole che possono donare specificamente o accettare un protone per agire come acido o base.
Può servirti: rodio: storia, proprietà, struttura, usi, rischioDovrebbe essere chiarito che tutte le sostanze anfotiche sono anfotiche, ma non tutte le anfoter sono anfiprtiche; Ci sono anfotori che non hanno protoni, ma possono comportarsi come acidi o basi in altri modi (come la teoria di Lewis).
Tra le sostanze anfiprtiche ci sono acqua, aminoacidi e ioni di bicarbonato e solfato. A loro volta, le sostanze anfrofotiche sono anche sottoclassificate in base alla loro capacità di donare o produrre protoni:
Sostanze protogeniche o di acido anfipritico
Sono quelli che hanno una maggiore tendenza a dare un protone che ad accettarne uno. Tra questi ci sono acido solforico (h2SW4) e acido acetico (Cho3Cooh), tra gli altri.
Sostanze protofili o anfotiche di base
Sono quelli per i quali accettare un protone è più comune che cederlo. Tra queste sostanze puoi trovare ammoniaca (NH3) ed etilendiamide [c2H4(NH2)2".
Sostanze neutre
Hanno la stessa facilità o capacità di accettare un protone da rinunciare. Tra questi ci sono acqua (h2O) e alcoli minori (-roh), principalmente.
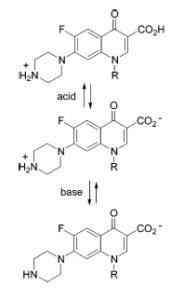 Carattere ampotero di chinolones
Carattere ampotero di chinolones Esempi di sostanze anfotenose
 Tensione anfotero
Tensione anfotero Ora, hai già descritto le sostanze anfotenti che è necessario indicare gli esempi di reazioni in cui sono presentate queste caratteristiche.
Lo ione dell'acido carbonico presenta un caso base di una sostanza anfiprtica; Quindi le loro reazioni sono rappresentate quando agisce come un acido:
HCO3- + OH- → CO32- + H2O
La reazione successiva si verifica quando funge da base:
HCO3- + H3O+ → H2Co3
Ci sono anche molte altre sostanze. Di questi sono i seguenti esempi:
Ossidi di anfoteros
L'ossido di zinco, come già accennato, è un anfotero ma non una sostanza anfiprtica. Successivamente, è dimostrato perché.
Può servirti: Justus von LiebigComportarsi come acido:
ZnO + H2SW4 → Znso4 + H2O
Comportarsi come base:
ZnO + 2NaOH + H2O → na2[Zn (OH)4"
Ossido di piombo (PBO), alluminio (AL2O3) e Tin (SNO) hanno anche le loro caratteristiche anfotenti:
Comportarsi come acidi:
PBO + 2HCL → PBCL2 + H2O
Al2O3 + 6HCl → 2alcl3 + 3h2O
Sno + hcl ↔ sncl + h2O
E come basi:
PBO + 2NaOH + H2O → na2[PB (OH)4"
Al2O3 + 2Naoh + 3H2O → 2na [al (OH)4"
Sno + 4Naoh + H2O ↔ na4[Sn (Oh)6"
Ci sono anche ossidi di anfoteros dalla Gallia, dall'India, dallo Scandio, dal Titanio, dal Cironium, dal Vanadio, dal Chrome, dal ferro, dal Cobalto, dal rame, dall'argento, dall'Oro, dall'antimo, dall'antimonio, dall'antimonio, dall'antimo e il Telurio.
Idrossidi anfoter
Gli idrossidi possono anche presentare caratteristiche anfotenti, come in caso di idrossido di alluminio e berillio. Di seguito sono riportati entrambi gli esempi:
Idrossido di alluminio come acido:
Al (Oh)3 + 3HCL → ALCL3 + 3h2O
Idrossido di alluminio come base:
Al (Oh)3 + NaOH → Na [al (OH)4"
Berillio idrossido come acido:
Essere (oh)2 + 2HCL → BECL2 + H2O
Berillio idrossido come base:
Essere (oh)2 + 2Naoh → Na2[Essere (oh)4"
Differenze tra anfoteros, anfiprici, anfoliti e apraticics
È necessario sapere come differenziare il concetto di ogni termine, poiché la sua somiglianza può diventare confusa.
È noto che gli anfotori sono sostanze che si comportano come acidi o basi in una reazione che produce sale e acqua. Possono farlo per la donazione o la cattura di un protone o semplicemente accettando una coppia elettronica (o dandolo) secondo la teoria di Lewis.
D'altra parte, le sostanze anfotiche sono quegli anfoter che agiscono come acidi o basi con la donazione o la raccolta di un protone, secondo la legge di Bronsted-Lowry. Tutte le sostanze anfotiche sono anfotiche.
Può servirti: benzoine: struttura, proprietà, usi e rischiI composti ampolitici sono molecole anfotese che esistono come zwitterioni e hanno ioni dipolo in alcuni phyes di pH. Sono usati come agenti di smorzamento in soluzioni tampone.
Infine, i solventi della stretta sono quelli che non hanno protoni da cedere e non possono accettarli neanche.
Riferimenti
- Anfoterico. (2008). Wikipedia. Ottenuto da in.Wikipedia.org
- Anne Marie Helmestine, P. (2017). Cosa significa anfotero in chimica?. Ottenuto da ThoughtCo.com
- Bicpuc. (2016). Composti anfoterici. Ottenuto da Medum.com
- Chemicool. (S.F.). Definizione anfoterica. Ottenuto da Chemicool.com.
- « La colombia tipica più popolare
- Scelta dell'argomento della ricerca come, l'importanza, gli esempi sono fatti »

